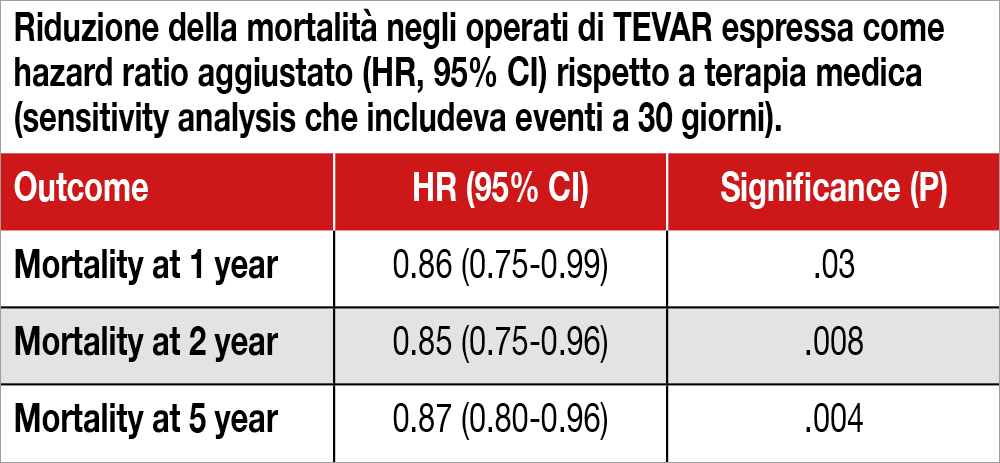
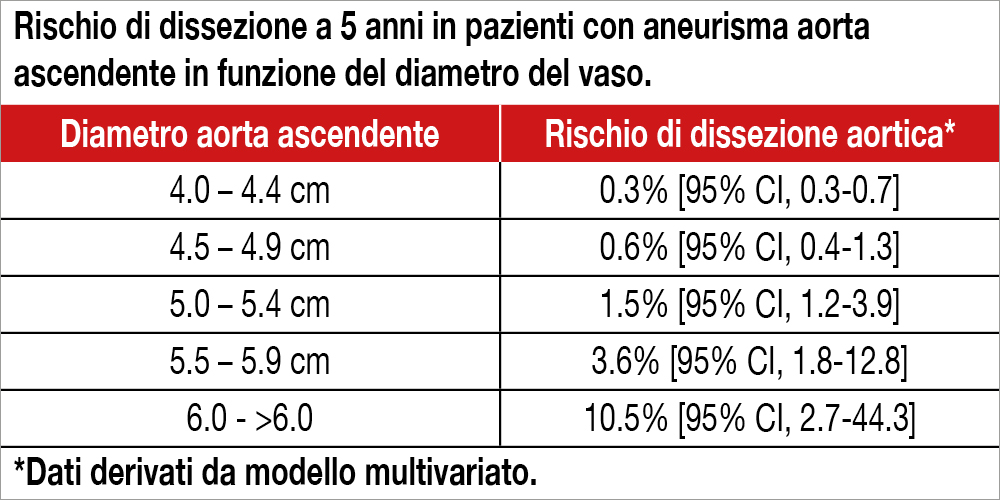
L’intervento di riparazione transcatetere della valvola tricuspide (TTVI), affetta da insufficienza severa, è effettuato con sempre maggior frequenza ed è associato a una migliore qualità di vita rispetto alla solaterapia medica. La valutazione del rischio operatorio e la previsione del successo procedurale eclinico dell’intervento sono molto importanti prima di sottoporre a TTVI. Il TRISCORE è uno scoreintrodotto per predire la mortalità operatoria nei pazienti sottoposti a chirurgia isolata della valvolatricuspide, un intervento gravato da alta mortalità...