Stefano De Servi, Università degli Studi di Pavia
Inquadramento
La morte improvvisa (SD) costituisce circa il 20% delle cause di decesso ed è elevata soprattutto nei pazienti con esiti di infarto miocardico[1]Wellens HJJ, Schwartz PJ, Lindemans FW, Buxton AE, Goldberger JJ, Hohnloser SH, et al. Risk stratification for suddencardiac death: current status and challenges for the future. Eur Heart J … Continua a leggere. Benché l’utilizzo del defibrillatore impiantabile rappresenti un passo notevole verso la riduzione della SD, il suo impatto risulta limitato per l’incapacità attuale di individuare ì pazienti à rischio di SD. L’attuale criterio di impianto di ICD rimane la riduzione del valore di frazione di eiezione del ventricolo sinistro (LVEF), ma vi è necessità di una nuova stratificazione del rischio di SD, perché essa può colpire pazienti con FE conservata o moderatamente depressa, mentre molti pazienti con FE ≤35% hanno una prognosi molto buona seguendo le direttive di trattamento farmacologico raccomandate dalle linee guida.
Lo studio in esame
L’analisi presente raggruppa 20 dataset che includevano globalmente 140.204 pazienti con esiti di infarto miocardico (MI). Sono stati esclusi i pazienti che già avessero ricevuto prima di MI un ICD, oppure un impianto per resincronizzazione miocardica o ancora un ICD entro 40 giorni da MI indice avessero una cardiomiopatia non ischemica associata.
Sono stati considerati tre gruppi:
gruppo 1) pazienti con ICD impiantato in prevenzione primaria per un valore di LVEF 35% (n = 7.543, et media 63.8 anni);
gruppo 2) pazienti senza ICD pur avendo LVEF 35% (n = 25.058, et media 72.6 anni);
gruppo 3) pazienti senza impianto di ICD è LVEF >35% (n = 107.603, et media 68.3 anni).
L’outcome primario (SD nei pazienti senza ICD impiantato, corretto intervento di ICD se questo era stato impiantato) si verificato in 1.326 pazienti del gruppo 1 a un follow-up medio di 30 mesi (17.4%); in 1.193 pazienti del gruppo 2 a un follow-up medio di 46.5 mesi (7.34%) è in 1.567 pazienti del gruppo 3 ad un follow-up medio di 57.6 mesi (1.89%).
Gli autori hanno sviluppato e validato internamente due modelli per predire la SD a 1 è 3 anni nei tre gruppi: il primo ha utilizzato solo la LVEF come misura continua, il secondo ha considerato altre variabili demografiche, cliniche ed elettrocardiografiche.
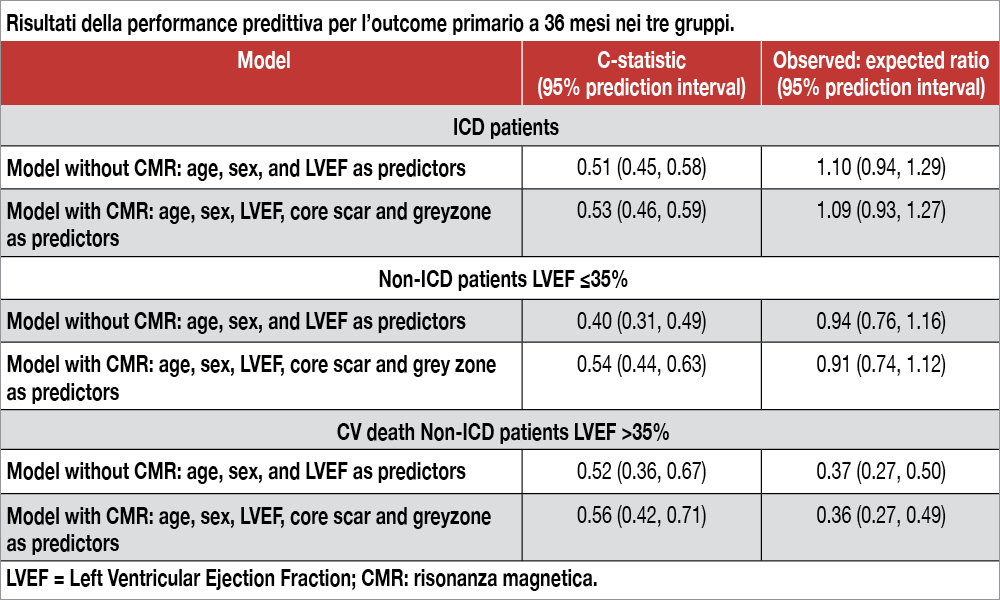
In tutti questi gruppi, la capacità predittiva di SD sulla base dei due modelli stata piuttosto bassa (c-statistics circa 0.50 nei tre gruppi). Utilizzando anche i dati della risonanza magnetica, disponibili in 2.076 pazienti, in un modello che includeva, oltre a LVEF, anche età, sesso, estensione della fibrosi miocardica e della cosiddetta “grey zone” (area commista di fibrosi e miocardio vitale), i valori di c-statistics rimanevano pressoché invariati (vedi Tabella).
Take home message
La presente analisi, basata sull’utilizzo di LVEF e altri potenziali predittori di morte improvvisa, non ha permesso di ottenere una più accurata stratificazione del rischio dopo un infarto miocardico, così come non ha individuato pazienti a basso rischio tra quelli con LVEF depressa o a rischio alto tra quelli con LVEF preservata.
Interpretazione dei dati
Lo scopo del lavoro era sicuramente lodevole, cioè di valutare se alcuni marker non invasivi fossero in grado di individuare i pazienti a elevato rischio di morte improvvisa, testando anche valori di LVEF differenti dai limiti soglia definiti nelle linee guida. E’ noto che il cutoff di 35% di LVEF deriva dagli studi storici di riferimento per l’impianto di defibrillatore, i trial MADIT II(4) e SCD HeFT[2]Bardy GH, Lee KL, Mark DB, Poole JE, Packer DL, Boineau R, et al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med 2005; 352:22537. … Continua a leggere. Peraltro, vent’anni di esperienza hanno chiarito che oltre la metà dei decessi per morte improvvisa avviene in pazienti con LVEF >40%[3]Waks JW, Buxton AE. Risk stratification for sudden cardiac death after myocardial infarction. Annu Rev Med 2018;69:14764. https://doi.org/10.1146/annurev-med-041316- 090046. e che la maggior parte dei pazienti trattati con defibrillatore non riceve mai un intervento del dispositivo durante la loro vita.
Il problema diviene di difficile soluzione e di maggiore complessità se si considerano casistiche un pò datate (come quella in esame) nelle quali la rivascolarizzazione stata eseguita in una percentuale limitata di pazienti (meno di un quarto dei pazienti che non hanno ricevuto l’ICD e meno della metà di quelli in cui un ICD era stato impiantato). Con il miglioramento delle terapie farmacologiche nei pazienti scompensati il rischio di morte improvvisa si dimezzato tra la metà degli anni 90 (6.5%) e il 2020 (~3%)[4]Shen L, Jhund PS, Petrie MC, Claggett BL, Barlera S, Cleland JGF, et al. Declining risk of sudden death in heart failure. N Engl J Med 2017;377:4151. https://doi.org/10.1056/ NEJMoa1609758..
Le risposte che lo studio fornisce sono deludenti per il clinico. La stratificazione del rischio di morte improvvisa sia nei pazienti con LVEF depressa che tra i pazienti con LVEF conservata, appare difficile utilizzando modelli basati su variabili non invasive, inclusa la valutazione continua della LVEF e il risultato della risonanza magnetica.
A tal proposito, è da sottolineare che il numero di pazienti con questa tipologia di informazione era ridotto (poco più dell’1% dell’intera casistica) e il numero esiguo di eventi può aver fortemente limitato l’individuazione di un potenziale ruolo di questa tecnologia.
A tal proposito si segnala che in corso lo studio CMR GUIDE che sta arruolando pazienti con disfunzione lieve-moderata della funzione ventricolare sinistra per cardiopatia ischemica o non-ischemica (LVEF 36%-50%) ed evidenza di fibrosi miocardica alla risonanza magnetica, randomizzandoli a ICD o terapia medica. L’arruolamento terminerà nel 2025.
Bibliografia[+]
| ↑1 | Wellens HJJ, Schwartz PJ, Lindemans FW, Buxton AE, Goldberger JJ, Hohnloser SH, et al. Risk stratification for suddencardiac death: current status and challenges for the future. Eur Heart J 2014;35:164251. https://doi.org/10.1093/ eurheartj/ehu176.; Myerburg RJ, Junttila MJ. Sudden cardiac death caused by coronary heart disease. Circulation 2012;125:1043-52.https://doi.org/10.1161/CIRCULATIONAHA.111.023846. |
|---|---|
| ↑2 | Bardy GH, Lee KL, Mark DB, Poole JE, Packer DL, Boineau R, et al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med 2005; 352:22537. https://doi.org/10.1056/NEJMoa043399. |
| ↑3 | Waks JW, Buxton AE. Risk stratification for sudden cardiac death after myocardial infarction. Annu Rev Med 2018;69:14764. https://doi.org/10.1146/annurev-med-041316- 090046. |
| ↑4 | Shen L, Jhund PS, Petrie MC, Claggett BL, Barlera S, Cleland JGF, et al. Declining risk of sudden death in heart failure. N Engl J Med 2017;377:4151. https://doi.org/10.1056/ NEJMoa1609758. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

