Inquadramento
Il rilascio di troponina, dopo un episodio certo di ischemia miocardica, è sempre stato considerato come espressione di una necrosi miocardica anche minima. Tuttavia, alcuni dati recenti in un modello sperimentale porcino hanno messo in dubbio questo assunto[1]Weil BR, Young RF, Shen X, Suzuki G, Qu J, Malhotra S and Canty JM, Jr. Brief Myocardial Ischemia Produces Cardiac Troponin I Release and Focal Myocyte Apoptosis in the Absence of Pathological … Continua a leggere. Mancano al riguardo dati corrispondenti nell’uomo. L’argomento non è solo speculativo, perchè incrementi di troponina sono frequentemente riscontrati dopo procedure di angioplastica coronarica, il cui significato clinico non è ancora completamente chiarito.
Lo studio in esame
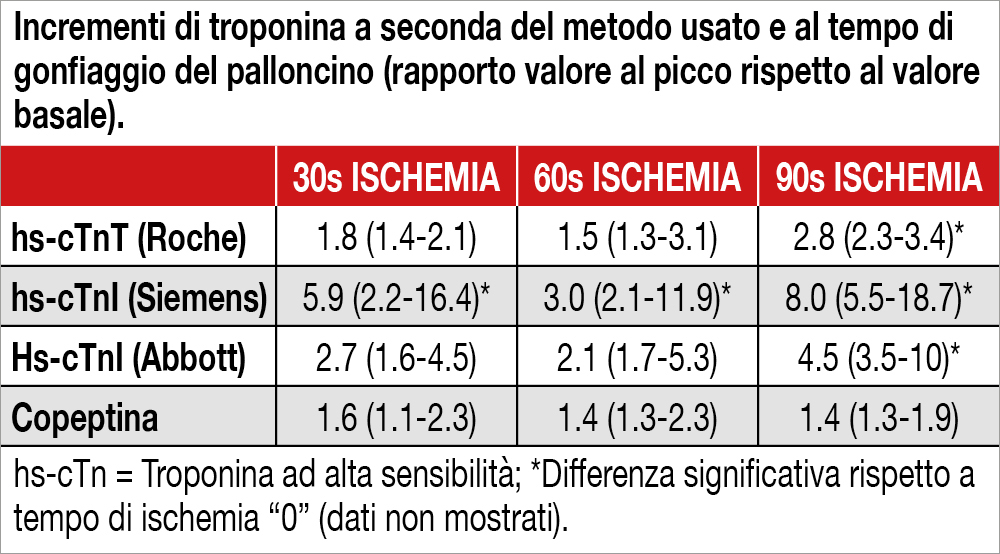
Gli Autori hanno studiato 34 pazienti (mediana di età 60 anni) sottoposti a coronarografia per un sospetto di malattia coronarica, e risultati essere indenni da lesioni ateromasiche. Al termine dell’esame diagnostico, un palloncino è stato gonfiato sino a 4 atmosfere per tempi prestabiliti (0”, 30”,60”, 90”) nella arteria discendente anteriore, tra il primo e secondo ramo diagonale. Sono stati eseguiti prelievi per la determinazione di troponina T (hs-TnT Roche) e I (hs-TnI con metodi Siemens e Abbott) e di copeptina a intervalli di 15 minuti per le prime 3 ore, e a intervalli di 30 minuti per le successive 3 ore. Incrementi di TnI (Siemens) erano già presenti dopo 90 secondi di ischemia, con picchi più elevati di quelli riscontrati con gli altri metodi. Criteri per diagnosticare un infarto miocardico (incrementi superiori al 99.mo percentile secondo la 4a definizione universale) erano presenti dopo 90” di ischemia nel 63% dei pazienti utilizzando hs-TnT, nel 25% per hs-TnI Siemens e 11% per hs-TnI Abbott. Non si riscontravano mai incrementi significativi di copeptina.
Take home message
I metodi per la determinazione della TnI appaiono più sensibili di quelli utilizzati per la TnT per episodi di ischemia miocardica di durata molto breve, con ogni verosimiglianza non associati a necrosi miocardica. Ciò nonostante, i criteri indicati dalla 4a definizione universale come indicativi di infarto miocardico venivano soddisfatti in percentuali anche ampie di pazienti, a seconda del metodo impiegato.
Interpretazione dei dati
Il risultato più interessante dello studio risiede nella dimostrazione che anche una ischemia miocardica di breve durata (inferiore ai 5 minuti, il limite che gli studi sperimentali indicano come necessario perchè si produca necrosi miocardica[2]Heyndrickx GR, Millard RW, McRitchie RJ, Maroko PR and Vatner SF. Regional myocardial functional and electrophysiological alterations after brief coronary artery occlusion in conscious dogs. The … Continua a leggere) dà origine a un incremento significativo di troponina. Ci sono due potenziali ricadute cliniche: la prima è che limiti più ampi dovrebbero essere posti agli incrementi di troponina perchè si possa porre una diagnosi clinica di infarto miocardico. La seconda è che il gonfiaggio del palloncino, durante angioplastica coronarica, determina di per sè un incremento di troponina. Procedure complesse e lunghe, che richiedono gonfiaggi ripetuti e/o prolungati, si accompagnano inevitabilmente ad aumenti, anche ampi, di troponina che non devono essere considerati come un effetto collaterale negativo dell’intervento, tanto meno una sua complicanza.
L’opinione di Federico Versaci
UOC UTIC, Emodinamica e Cardiologia Ospedale Santa Maria Goretti, Latina
La domanda che ci possiamo porre è, quindi, se un’ischemia molto breve, nell’ordine dei 30 secondi, possa causare la necrosi dei cardiomiociti, oppure se altri meccanismi diversi possano indurre il rilascio di troponine. In modelli animali, in cui è stata indotta ischemia anche fino a 10 minuti, l’innalzamento delle troponine è avvenuto entro un’ora in assenza di evidenza di miocardionecrosi, ma con rilievo di fenomeni di apoptosi focale riguardanti singoli miociti; in tali cellule miocardiche vitali un pool intracellulare di troponina, non legata al complesso actina-miosina e libera nel citoplasma, può essere rilasciata in circolo in risposta a uno stress ischemico insufficiente a produrre necrosi[3]Alpert JS, Thygesen K, Antman E, Bassand JP. Myocardial infarction redefined–a consensus document of The Joint European Society of Cardiology/American College of Cardiology Committee for the … Continua a leggere. È importante sottolineare come questo rilascio di troponine, meno fortemente legate all’apparato contrattile actina-miosina o libere nel citoplasma, avvenga secondo un meccanismo di apoptosi e secondo una cinetica di rilascio più rapida rispetto alla controparte legata. Sono stati proposti anche altri meccanismi per spiegare questo fenomeno, come l’alterata permeabilità della membrana dei cardiomiociti, la formazione di blebs di membrana o rilascio di frammenti degradati mediante proteolisi[4]Jaffe AS. Another unanswerable question. JACC Basic Transl Sci. 2017;2:115–117. doi: 10.1016/j.jacbts.2017.03.002.. L’ipotesi apoptosi caspasi-mediata potrebbe spiegare il perché dell’andamento di rapido rialzo e discesa delle troponine plasmatiche nel torrente ematico rilevato utilizzando i saggi ad alta sensibilità nei maratoneti e nei soggetti sani sottoposti a pacing, fenomeni già descritti in letteratura[5]Dawson EA, Whyte GP, Black MA, et al. Changes in vascular and cardiac function after prolonged strenuous exercise in humans. J Appl Physiol 2008;105:1562–8.[6]Turer AT, Addo TA, Martin JL, et al. Myocardial ischemia induced by rapid atrial pacing causes troponin T release detectable by a highly sensitive assay: insights from a coronary sinus sampling … Continua a leggere.
Il rilascio delle troponine, in queste condizioni non sarebbe quindi ascrivibile a necrosi dei miocardiociti, un meccanismo che prevede la distruzione della membrana del sarcolemma, la necrosi a bande di contrazione e il rilascio di proteine intracellulari come le troponine nel circolo coronarico. Una considerazione importante, derivante dallo studio, riguarda la variabilità che caratterizza i diversi saggi disponibili in commercio. È stato osservato, infatti, quanto questi possano restituire diverse informazioni sulla cinetica di rilascio delle troponine nel circolo e questo fenomeno può essere spiegato, parzialmente, dal fatto che i diversi anticorpi dei saggi vadano a legare epitopi localizzati in differenti regioni dei frammenti di troponine. Le implicazioni cliniche del rapido rilascio di troponine ad alta sensibilità potrebbero, quindi, ridefinire questi marker come criterio oggettivo di diagnosi nell’ambito, per esempio, di condizioni quali l’angina instabile, introducendo un parametro oggettivo laboratoristico che possa irrobustire una diagnosi a oggi solamente guidata dal sintomo. Ampliando la conoscenza fisiopatologica e biologica del meccanismo di rilascio delle troponine si potrebbe pensare, quindi, nel futuro di riclassificare le sindromi coronariche acute in modo più preciso. In conclusione, sebbene la fisiopatologia della cinetica del rilascio delle troponine sia stata indagata in modo innovativo in questo studio, rimane incertezza riguardo la traslazione di questi risultati nella pratica clinica in quanto lo studio è stato condotto su un numero esiguo di pazienti, in condizioni sperimentali controllate, su soggetti con coronarie indenni e quindi privi di pre-condizionamento ischemico o circoli collaterali, condizioni tipiche di chi ha una patologia coronarica ostruttiva; per questo motivo, il rilascio di troponine potrebbe essere stato quantitativamente maggiore e la cinetica del rilascio più rapida in questi soggetti privi di patologia coronarica.
Bibliografia[+]
| ↑1 | Weil BR, Young RF, Shen X, Suzuki G, Qu J, Malhotra S and Canty JM, Jr. Brief Myocardial Ischemia Produces Cardiac Troponin I Release and Focal Myocyte Apoptosis in the Absence of Pathological Infarction in Swine. JACC Basic Transl Sci. 2017;2:105-114. doi: 10.1016/j.jacbts.2017.01.006. |
|---|---|
| ↑2 | Heyndrickx GR, Millard RW, McRitchie RJ, Maroko PR and Vatner SF. Regional myocardial functional and electrophysiological alterations after brief coronary artery occlusion in conscious dogs. The Journal of clinical investigation. 1975;56:978-985. |
| ↑3 | Alpert JS, Thygesen K, Antman E, Bassand JP. Myocardial infarction redefined–a consensus document of The Joint European Society of Cardiology/American College of Cardiology Committee for the redefini- tion of myocardial infarction. J Am Coll Cardiol. 2000;36:959–969.doi:10.1016/s0735-1097(00)00804-4. |
| ↑4 | Jaffe AS. Another unanswerable question. JACC Basic Transl Sci. 2017;2:115–117. doi: 10.1016/j.jacbts.2017.03.002. |
| ↑5 | Dawson EA, Whyte GP, Black MA, et al. Changes in vascular and cardiac function after prolonged strenuous exercise in humans. J Appl Physiol 2008;105:1562–8. |
| ↑6 | Turer AT, Addo TA, Martin JL, et al. Myocardial ischemia induced by rapid atrial pacing causes troponin T release detectable by a highly sensitive assay: insights from a coronary sinus sampling study. J Am Coll Cardiol 2011;57:2398–405. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

