Inquadramento
Le Linee Guida stabiliscono una durata di 6 mesi nei pazienti con coronaropatia stabile, tuttavia nei pazienti ad alto rischio emorragico (HBR) la durata può essere ridotta. Gli studi XIENCE Short DAPT hanno dimostrato che nei pazienti HBR sottoposti ad impianto di DES a piattaforma in cobalto-cromo e rilascio di everolimus, una DAPT di 1/3 mesi è risultata non inferiore per quanto riguarda gli eventi ischemici e ha ridotto il bleeding rispetto ad una DAPT di 6/12 mesi[1]Mehran R, Cao D, Angiolillo DJ, et al. 3 or 1-month DAPT in patients at high bleeding riskundergoing everolimus-eluting stent implantation. J Am Coll Cardiol Intv. 2021;14:1870–1883.. Non esistono invece studi di confronto tra strategie di DAPT abbreviata (1 mese verso 3 mesi) nei pazienti HBR.
Lo studio in esame
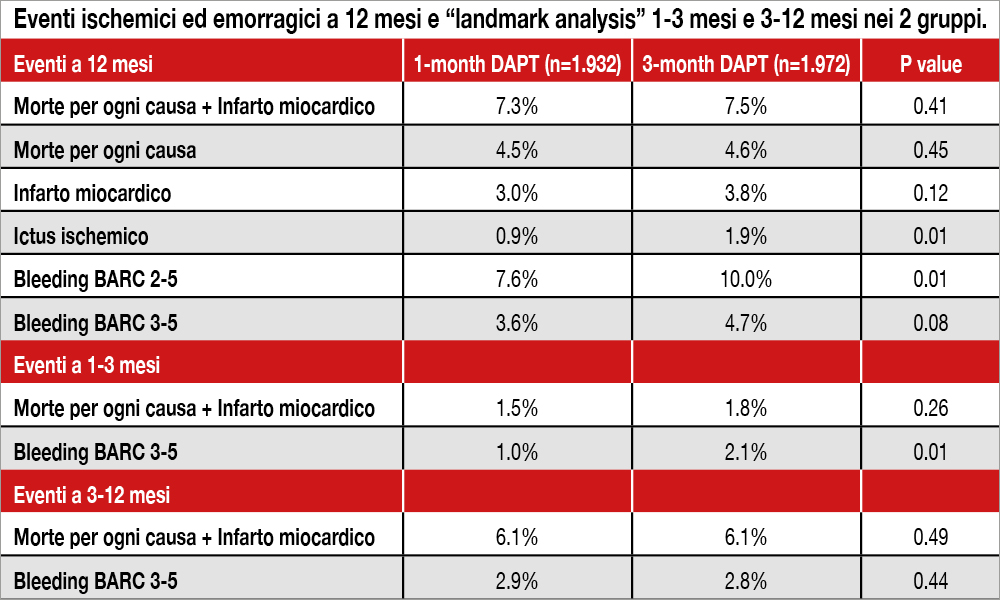
L’analisi confronta i risultati ottenuti in tre studi che hanno arruolato pazienti HBR (con almeno 1 dei seguenti criteri: età ≥75 anni, storia di bleeding maggiore nei 12 mesi precedenti, terapia anticoagulante in atto, nefropatia cronica, anemia, trombocitopenia, disturbi della coagulazione) sottoposti ad impianto DES XIENCE (età media 75 anni, due terzi con coronaropatia stabile, un terzo sindromi coronariche acute esclusi STEMI). I pazienti per essere inclusi nello studio dovevano aver superato il primo mese di trattamento senza complicanze. Il confronto riguardava i dati dello studio XIENCE 90, eseguito in 101 centri USA, che ha incluso 1.972 pazienti trattati con DAPT di 3 mesi (clopidogrel nell’86.5% dei casi + ASA, seguita da ASA in monoterapia) versus i dati globalmente analizzati di XIENCE 28 USA e XIENCE 28 GLOBAL che hanno arruolato 1.392 pazienti con DAPT di 1 mese (clopidogrel nell’81.7% dei casi + ASA seguita da ASA in monoterapia). Gli eventi considerati (ischemici ed emorragici) erano quelli occorsi tra il secondo e il dodicesimo mese di follow-up. Poichè lo studio non era randomizzato, i dati sono stati analizzati mediante stratificazione con propensity score. L’endpoint primario (mortalità per ogni causa, infarto miocardico) è risultato simile tra i due gruppi a 12 mesi (7.3% vs 7.5%; differenza 0.2%; 95% CI: 2.2% to 1.7%; p=0.41) mentre il bleeding secondo scala BARC 2-5 è risultato significativamente inferiore nei pazienti con DAPT di 1 mese rispetto a DAPT di 3 mesi. Il bleeding maggiore (BARC 3-5) tuttavia non è risultato significativamente differente a 12 mesi (vedi Tabella) pur essendo significativamente inferiore a 3 mesi dalla PCI nel gruppo DAPT di 1 mese.
Take home message
I pazienti HBR sottoposti a PCI con impianto di stent XIENCE e trattati con DAPT di un solo mese hanno avuto meno complicanze emorragiche (BARC 2-5) senza aumento di eventi ischemici rispetto ai pazienti trattati con DAPT di 3 mesi.
Interpretazione dei dati
Nella discussione gli autori puntualizzano che gli eventi occorsi nel primo mese di trattamento con DAPT non sono stati considerati nell’analisi al fine di eliminare eventuali differenze procedurali tra i due gruppi considerati, in quanto lo studio non era randomizzato. Inoltre, essi sottolineano come i dati di questa ricerca non possano applicarsi ai pazienti sottoposti a PCI complessa: infatti i pazienti con biforcazioni trattate con due stent, stent in “overlapping” o con più di tre lesioni “target” erano esclusi dallo studio. Un altro limite è rappresentato da una classificazione HBR differente da quella dell’Academic Research Consortium (ma gli studi erano stati disegnati prima che quella classificazione fosse proposta). Discutibile, comunque, l’inserimento dei pazienti in terapia anticoagulante: è ovvio che una DAPT più prolungata in questi pazienti li esponga a un rischio di bleeding maggiore. Peraltro, le Linee Guida sono ormai chiare in proposito: la triplice terapia antitrombotica deve essere di breve durata a meno che vi sia un rischio trombotico molto elevato.
L’opinione di Giancarlo Vitrella
Dipartimento Cardiotoracovascolare, Divisione di Cardiologia, Università di Trieste, Trieste
La gestione della terapia antiaggregante nei pazienti sottoposti a procedure di interventistica coronarica non può prescindere da un attento bilancio tra il rischio di eventi ischemici da una parte e il rischio di sanguinamento dall’altra. Il bilancio è particolarmente delicato nei pazienti ad alto rischio di sanguinamento (HBR: High Bleeding Risk, ovvero, secondo la definizione dell’Academic Research Consortium [ARC], pazienti a rischio di emorragia intracranica ≥1% all’anno o pazienti con rischio di sanguinamento BARC 3 o 5 [sanguinamenti con calo di Hb ≥3g/dL o intracranici e sanguinamenti fatali] ≥4% all’anno)[2]Urban P, Mehran R, Colleran R et al. Defining High Bleeding Risk in Patients Undergoing Percutaneous Coronary Intervention. A Consensus Document From the Academic Research Consortium for High … Continua a leggere, in quanto alcuni fattori di rischio emorragico, tra cui l’età, l’insufficienza renale o l’anemia, sono anche fattori associati ad aumento del rischio di eventi ischemici. Tuttavia, in questa popolazione, è dimostrato come l’aumentato rischio emorragico associato al prolungarsi del periodo di doppia antiaggregazione (DAPT) sia più accentuato rispetto al beneficio sugli eventi ischemici nei pazienti HBR, e l’attuale orientamento delle Linee Guida è di dare la priorità al rischio emorragico, accorciando nei limiti del possibile la DAPT in questa popolazione[3]Steg PG, Huber K, Andreotti T et al. Bleeding in acute coronary syndromes and percutaneous coronary interventions: position paper by the Working Group on Thrombosis of the European Society of … Continua a leggere[4]Collet JP,Thiele H, Barbato E et al. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the … Continua a leggere. Lo studio di Valgimigli e coll. ha confrontato 3 casistiche prospettiche di pazienti HBR sottoposti a PCI e successiva DAPT breve: XIENCE 90 (sottoposti a DAPT per 3 mesi), XIENCE 28 USA e XIENCE 28 Global (sottoposti a DAPT per 1 mese). L’endpoint primario di morte e infarto si è verificato in uguale misura (rispettivamente 7,3 vs 7,5%, p=0,41) mentre l’endpoint secondario di sanguinamenti BARC 2-5 si è verificato in minor misura (7,6 vs 10%, p=0,012) nella casistica trattata con 1 mese di DAPT rispetto alla casistica trattata con 3 mesi di DAPT. Questo studio ha il merito di aggiungere diversi tasselli importanti alla nostra pratica clinica. Suggerisce una sostanziale equivalenza in termini di rischio ischemico dei 2 regimi di DAPT abbreviata e un ridotto rischio emorragico nei pazienti HBR con durata di 1 mese rispetto ai 3 mesi, fornendo così ulteriori dati a supporto della DAPT abbreviata nei pazienti HBR. Nella lettura di questo studio colpisce l’importanza di un approccio globale al paziente HBR, mirato ad ottenere una riduzione complessiva degli eventi in questi pazienti. Gli stent a rilascio di farmaco di seconda generazione, come quelli utilizzati in questo studio, grazie a una maggior biocompatibilità, hanno dimostrato di essere associati a un ridotto rischio di eventi nei pazienti HBR rispetto agli stent a rilascio di farmaco di prima generazione o agli stent non medicati[5]Tada T, Byrne RA, Simunovic I et al. Risk of stent thrombosis among bare-metal stents, first-generation drug-eluting stents, and second-generation drug-eluting stents: results from a registry of … Continua a leggere. Inoltre, dal lato procedurale, si è cercato di limitare tecniche interventistiche associate a un aumentato rischio di trombosi dello stent: nei pazienti inclusi nello studio era ammesso il trattamento fino a 3 lesioni target, non più di 2 lesioni per vaso epicardico, venivano esclusi gli stent in overlap e l’impiego di tecniche a 2 stent per il trattamento delle biforcazioni. Pertanto, la limitata durata della DAPT va letta in un contesto più ampio di strategia di riduzione del rischio nei pazienti HBR, che comprende il trattamento di un numero limitato di lesioni, la scelta di stent medicati di seconda generazione, impiantati evitando overlap e tecniche di biforcazione con 2 stent. La direzione attuale è quella di un trattamento su misura per il paziente, dove a un estremo ci sono i pazienti HBR in cui è favorita la DAPT abbreviata, all’altro i pazienti ad alto rischio ischemico, in cui è auspicabile il prolungamento della DAPT oltre l’anno[6]Bonaca MP, Bhatt DL, Cohen M et al. Long-Term Use of Ticagrelor in Patients with Prior Myocardial Infarction. N Engl J Med 2015; 372:1791-1800.. I limiti di questo studio sono oggettivi, correttamente indicati dagli autori. In primis non si tratta di un confronto randomizzato prospettico, ma di 3 casistiche prospettiche indipendenti, seppur con i medesimi criteri di inclusione. Le popolazioni hanno alcune differenze tra di loro (differenti prevalenze di razza bianca, insufficienza renale, presentazione con NSTEMI, tipo di P2Y12 utilizzato) e l’aggiustamento del rischio post-hoc con il propensity score matching potrebbe essere soltanto parziale. Infine, lo studio ha definito i pazienti HBR in epoca antecedente ai criteri ARC (il criterio HBR più rappresentato era l’età ≥75 anni, che è un criterio ARC minore, da solo insufficiente a definire un paziente HBR), pertanto una quota di pazienti arruolati in questo studio potrebbe non essere considerata HBR secondo i criteri ARC, attuale benchmark. Come correttamente indicato dagli autori, questo studio è un’analisi post-hoc ed è da considerarsi “hypothesis generating”. Ciononostante, i risultati sono analoghi a quelli dello studio MASTER DAPT, pubblicato recentemente[7]Valgimigli M, Frigoli E, Heg D et al. Dual Antiplatelet Therapy after PCI in Patients at High Bleeding Risk. N Engl J Med 2021; 385:1643-1655.un confronto prospettico randomizzato e controllato di 1 mese vs 3 mesi di DAPT in pazienti HBR (definiti secondo gli stessi criteri) sottoposti a PCI con impianto di stent medicato. Sarà importante verificare in futuro se questi risultati siano applicabili ai pazienti HBR definiti secondo i criteri ARC. Altre domande a cui i futuri studi dovranno rispondere riguardano la scelta di sospendere l’ASA o l’inibitore P2Y12 al termine del periodo di DAPT, l’eventuale ruolo della DAPT con P2Y12 a dosaggio ridotto (ticagrelor 60 mg x 2 o prasugrel 5 mg/die), l’utilizzo di FFR nella scelta delle lesioni da trattare, l’impiego sistematico di Imaging intracoronarico per ottimizzare l’impianto dello stent nei pazienti HBR e la durata ottimale della DAPT in caso di stenting di lesioni coronariche complesse.
Bibliografia[+]
| ↑1 | Mehran R, Cao D, Angiolillo DJ, et al. 3 or 1-month DAPT in patients at high bleeding riskundergoing everolimus-eluting stent implantation. J Am Coll Cardiol Intv. 2021;14:1870–1883. |
|---|---|
| ↑2 | Urban P, Mehran R, Colleran R et al. Defining High Bleeding Risk in Patients Undergoing Percutaneous Coronary Intervention. A Consensus Document From the Academic Research Consortium for High Bleeding Risk. Circulation. 2019;140:240–261. |
| ↑3 | Steg PG, Huber K, Andreotti T et al. Bleeding in acute coronary syndromes and percutaneous coronary interventions: position paper by the Working Group on Thrombosis of the European Society of Cardiology. Eur Heart J. 2011;32(15):1854-64. |
| ↑4 | Collet JP,Thiele H, Barbato E et al. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2021; 42(14):1289–1367. |
| ↑5 | Tada T, Byrne RA, Simunovic I et al. Risk of stent thrombosis among bare-metal stents, first-generation drug-eluting stents, and second-generation drug-eluting stents: results from a registry of 18,334 patients. JACC Cardiovasc Interv. 2013;6(12):1267-74. |
| ↑6 | Bonaca MP, Bhatt DL, Cohen M et al. Long-Term Use of Ticagrelor in Patients with Prior Myocardial Infarction. N Engl J Med 2015; 372:1791-1800. |
| ↑7 | Valgimigli M, Frigoli E, Heg D et al. Dual Antiplatelet Therapy after PCI in Patients at High Bleeding Risk. N Engl J Med 2021; 385:1643-1655. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

