Abstract
Background: Acute kidney injury (AKI) after transcatheter aortic valve replacement (TAVR) is associated with increased mortality. However, it is controversial whether AKI affects prognosis per se, being linked to baseline chronic kidney disease (CKD) and bleeding complications. The aim of this study was to disentangle, applying mediation analysis, the association between AKI and clinical outcome, considering CKD and bleedings.
Methods and Results: Consecutive patients undergoing TAVR were prospectively enrolled at 5 high-volume centers in Italy. AKI was defined according to Valve Academic Research Consortium-3 consensus, whereas bleeding with Bleeding Academic Research Consortium. Primary outcome was all-cause mortality after 1-year follow-up. Among 2.621 patients undergoing TAVR, AKI occurrence was associated with 1-year mortality. This association of AKI with the primary end points remained significant after adjusting for baseline risk estimators, either Society of Thoracic Surgeons score (hazard ratio [HR], 2.78 [95% CI, 1.95-3.80], P<0.001) or EuroSCORE-II (HR, 1.85 [95% CI, 1.35-2.56], P<0.001). Both AKI and CKD significantly and independently affected primary outcome (HR, 3.06 [95% CI, 2.01-4.64], P<0.001 and HR, 1.82 [95% CI 1.27-2.65], P<0.01, respectively). The estimated proportion of the total effect of CKD mediated via AKI was, on average, 15%, 95% CI, 4%- 29%, P<0.001. The significant effect of Bleeding Academic Research Consortium 2-5 bleedings on the primary outcome was not mediated by AKI.
Conclusions: AKI occurs in 1 out of 6 patients and significantly mediates one fifth of the effect of baseline CKD on all-cause mortality after TAVR. Our analysis supports a systematic effort to prevent AKI during TAVR, which may potentially translate into improved patients’ 1-year survival.
Intervista a Gabriele Crimi
Unità di Cardiologia, Dipartimento Cardiotoracico e Vascolare (DICATOV) IRCCS, Ospedale Policlinico San Martino, Genova
Dottor Crimi quali sono i dati salienti della vostra analisi?
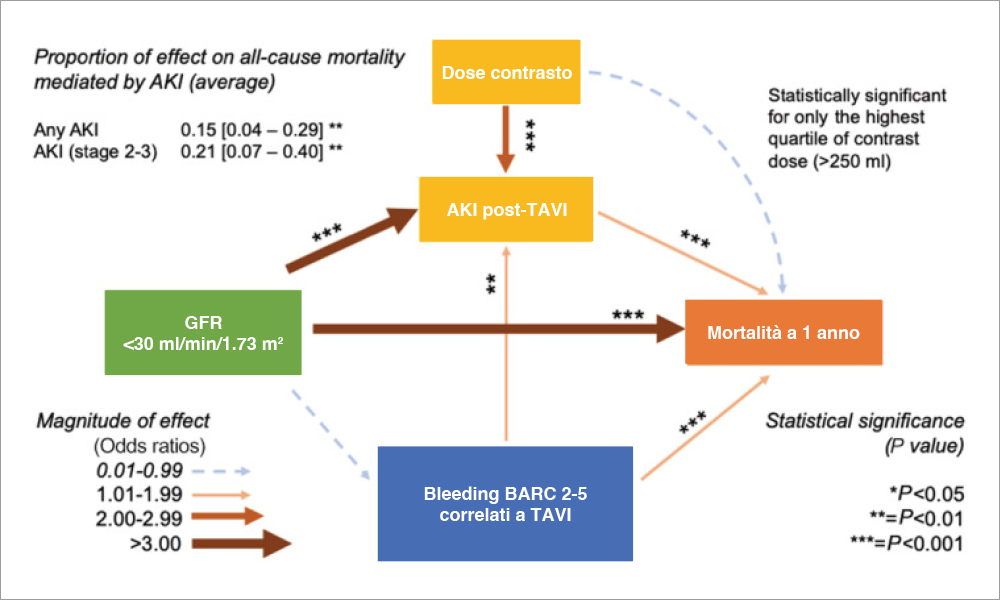
La sostituzione della valvola aortica con metodica trans-catetere (TAVR) è diventato uno standard nella gestione dei pazienti sintomatici con stenosi aortica severa, a rischio operatorio intermedio-alto e si sta sempre più affermando come valida alternativa nei pazienti a basso rischio. Espandere le indicazioni nei pazienti a rischio più basso, vuol dire ridurre al minimo le complicanze della procedura. Nella nostra analisi ci siamo focalizzati su una di queste complicanze, ovvero sul danno renale acuto (AKI) espresso come rialzo di creatinina post-procedurale. L’AKI è una complicanza relativamente frequente, specialmente nei pazienti nefropatici con funzione renale ridotta al basale ed è associata a incremento di mortalità e morbilità. I risultati salienti del nostro studio sono espressi nella figura (modificata rispetto all’originale).
Qual è il contributo di originalità del vostro studio rispetto alla letteratura precedente?
In letteratura è ben nota l’associazione tra AKI e prognosi sfavorevole in vari contesti clinici, compreso quello dei pazienti sottoposti a TAVR. Tuttavia, non è facile enucleare il ruolo indipendente di AKI sulla prognosi, essendo questa complicanza più frequente nei pazienti con nefropatia cronica che per se è un marker di severità di patologia, di conseguenza non modificabile. Uno spunto originale della nostra analisi è stato quello di utilizzare una analisi multivariata di mediazione; questi modelli statistici permettono di enucleare e quantificare il ruolo indipendente di AKI sulla prognosi, rispetto al ruolo della nefropatia di base. Nell’analisi sono stati inseriti 2.621 pazienti sottoposti a procedura di TAVR nei Centri più importanti di Italia. Si conferma un dato già noto in letteratura, ovvero che AKI è una complicanza comune, che si verifica in circa un paziente ogni sei sottoposto a TAVR e che AKI si lega a un aumento di due volte del rischio di morire dopo un anno di follow-up. I risultati più importanti e originali sono riassunti nella figura sottostante: si apprezza che sia la nefropatia di base (espressa come eGFR <30 ml/min/1.73 mq) che AKI si legano a un incremento di mortalità per tutte le cause a un anno di follow-up. AKI media circa un quinto dell’impatto prognostico della nefropatia di partenza. Questo dato ha dei risvolti clinici importanti, perché ridimensiona e quantifica l’impatto prognostico potenzialmente prevenibile con metodiche che riducono incidenza di AKI.
L’evenienza di AKI si associa, nei vostri pazienti, a una maggior quantità di mezzo di contrasto utilizzato durante la procedura. Questo dato (come ben osservate nella discussione) potrebbe rappresentare un indice di complessità della procedura. Pensa, quindi, che il rischio di mortalità connesso ad AKI potrebbe essere, almeno in parte, ascrivibile alla presenza di variabili anatomiche sfavorevoli non facilmente quantificabili in una analisi multivariata?
In parte potrebbe essere legato alla complessità della procedura, anche se mi aspetterei che questo aspetto possa esprimersi con un aumento di mortalità precoce, misurabile a 30 giorni, invece le curve di sopravvivenza continuano a divaricarsi con un rischio proporzionale fino a un anno di follow-up, questo è spiegabile non solo dalla complessità tecnica della TAVR, ma da una serie di variabili, in parte non misurabili, che caratterizzano una maggiore severità di patologia basale; tra queste variabili c’è sicuramente la nefropatia cronica per cui abbiamo corretto nel modello. Inoltre, AKI si associa anche agli eventi emorragici, questo dato è interessante perché slegato dalla nefropatia di base come si vede nel grafico. Ne consegue che ridurre gli eventi emorragici durante TAVR sia funzionale anche a ridurre incidenza di AKI.
Nella discussione del vostro lavoro, AKI viene definita come un fenomeno prevenibile. Quali sono gli strumenti utili al riguardo (infusione di liquidi, utilizzo di sistemi di infusione correlati alla diuresi, CVVH nella nefropatia più avanzata) e quali i pazienti target?
Riguardo alla prevenzione di AKI, sicuramente la metodica principale è quella di limitare il mezzo di contrasto iodato. Nelle serie più moderne si apprezza una netta riduzione della dose rispetto all’inizio della curva di apprendimento e nel mondo reale abbiamo visto come la maggior parte delle procedure possono essere condotte con meno di 100 cc di mezzo di contrasto. Un altro aspetto fondamentale è mantenere il più possibile lo stato euvolemico, limitando l’uso di diuretici pre-procedura, una strategia per massimizzare l’espansione volemica senza eccedere con il riempimento. La strategia che si è dimostrata efficace nel setting di interventistica coronarica è quella di utilizzare la pressione telediastolica del ventricolo sinistro (studio POSEIDON) come guida per modulare il volume in entrata. Infine, l’espansione volemica massimale controllata, ottenuta mediante utilizzo del dispositivo RenalGuard o la CVVH può essere una strategia da testare nei pazienti a maggiore rischio. Riguardo ai pazienti target, nella nostra analisi si evidenzia come ci sia un incremento dell’impatto prognostico per valori di eGFR <45-30 ml/min/1.73 mq, valori per cui esiste un incremento esponenziale del rischio di sviluppare AKI. Pertanto credo che nel mondo reale i pazienti con eGFR compreso tra 15 e 45 ml/min/1.73 mq siano il subset più adeguato per sperimentare metodiche di prevenzione AKI.
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

