Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Le linee guida raccomandano di sottoporre a rivascolarizzazione solo le stenosi coronariche epicardiche che siano fisiopatologicamente significative, cioè capaci di limitare il flusso in condizioni di massima vasodilatazione (positive quindi alla valutazione della riserva frazionale di flusso) o che causino una sindrome coronarica acuta[1]Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS guidelines on myocardial revascularization.Eur Heart J 2019; 40: 87–165; Lawton JS, Tamis-Holland JE, Bangalore S, et al. 2021 ACC/AHA/SCAI … Continua a leggere. Una serie di studi prospettici ha tuttavia dimostrato come placche coronariche, che non limitino significativamente il flusso, ma posseggano alcune caratteristiche morfologiche all’imaging intravascolare, quali l’area luminale minima <=4·0 mm², un “burden” di placca >70%, un ampio core lipidico, un cap fibroso sottile (“placche vulnerabili”) siano inclini a fenomeni di fissurazione o rottura, innescando un quadro di instabilizzazione clinica[2]Gallone G, Bellettini M, Gatti M, et al. Coronary plaque characteristics associated with major adverse cardiovascular events in atherosclerotic patients and lesions: a systematic review and … Continua a leggere. Un intervento di PCI con stenting potrebbe indurre un fenomeno di “passivazione” di queste placche e avere effetti benefici: infatti è stato osservato dopo PCI un aumento del diametro intraluminale e un ispessimento del cap fibroso a 2 anni di follow-up[3]Stone GW, Maehara A, Ali ZA, et al. Percutaneous coronary intervention for vulnerable coronary atherosclerotic plaque. J Am Coll Cardiol 2020; 76: 2289–301., ma attualmente non sono a disposizione dati provenienti da trial randomizzati che dimostrino l’efficacia clinica di un trattamento interventistico rispetto a una terapia medica ottimale.
Lo studio in esame
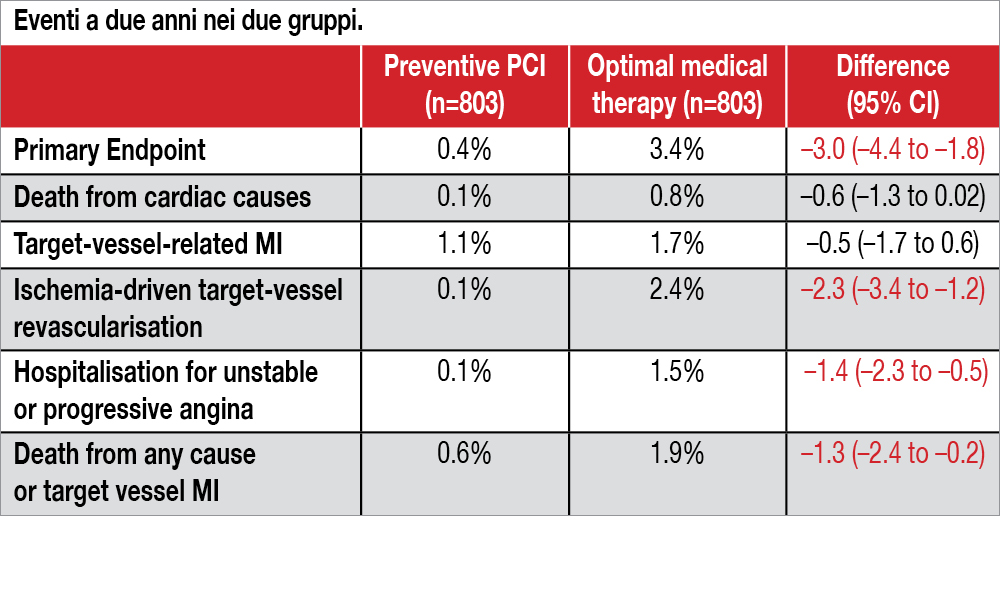
Lo studio, condotto in Sud Corea, Giappone e Nuova Zelanda, ha arruolato 1.606 pazienti, per lo più con coronaropatia stabile (83%) e con almeno una lesione coronarica non ischemizzante (FFR negativa, mediana 0.86), ma con aspetti di vulnerabilità (“lesione target” con almeno due di queste caratteristiche all’imaging intracoronarico: plaque burden >70%, area luminale minima-MLA- <4 mm2, ampio core lipidico all’indagine spettroscopica a raggi infrarossi, cap fibroso sottile all’OCT o all’IVUS a radiofrequenza). Essi sono stati randomizzati a PCI con stenting preventivo (n=803) o a “standard care” (n=803). Nei 1.606 pazienti arruolati erano state individuate 1.672 lesioni target. Le caratteristiche delle lesioni erano per lo più derivate dall’IVUS (97% dei pazienti aveva MLA <4 mm2, il 96% “plaque burden” >70%, 11% core lipidico ampio alla spettroscopia a infrarossi, 5% cap fibroso sottile all’OCT). L’età mediana era 64 anni. In due terzi circa dei pazienti di entrambi i gruppi (36%) veniva eseguita una PCI su una lesione critica. La randomizzazione veniva stratificata per la presenza di diabete e di PCI su lesione critica. Inizialmente gli stent utilizzati erano riassorbibili (33% dei pazienti), successivamente al loro ritiro dal mercato sono stati utilizzati stent medicati a rilascio di everolimus. L’endpoint primario (target vessel failure = morte cardiaca, infarto miocardico o rivascolarizzazione del target vessel, ospedalizzazione per instabilizzazione clinica) a due anni di follow-up è stato significativamente ridotto dalla PCI rispetto alla terapia medica ottimale (0.4% dei pazienti PCI e nel 3.4% dei pazienti standard of care (differenza assoluta –3.0% [95% CI –4.4 a –1.8] P=0.0003). Le differenze nelle singole componenti dell’endpoint sono riportate nella Tabella. Da segnalare che anche l’endpoint composito morte cardiaca e infarto miocardico, correlato al target vessel, risultava significativamente differente nei due gruppi a 2 anni di follow-up (0·3% versus 1.4%, differenza assoluta –1.1 % [95% CI –2.0 to –0.2]). A 7 anni, la differenza numerica nel primary endpoint risultava analoga a quella osservata a 2 anni, ma non risultava statisticamente significativa (6·5% versus 9·4% differenza (–2.9; –7.3 a 1.5).
Take home message
Nei pazienti che presentano alla coronarografia placche non critiche, ma con caratteristiche morfologiche all’imaging intracoronarico che le definiscono come vulnerabili, una PCI preventiva ha ridotto gli eventi cardiaci maggiori rispetto alla standard of care.
Interpretazione dei dati
Lo studio ha indubbiamente alcuni pregi. È il primo ad aver confrontato gli effetti della PCI con impianto di stent, rispetto alla terapia medica ottimale sull’outcome di pazienti con stenosi non critiche (FFR negativa, valore mediano 0.86), ma con caratteristiche di vulnerabilità, valutata in base ai risultati di indagini di imaging intracoronarico. Per la prima viene infranto il dogma in base al quale l’esecuzione della PCI non produce benefici (o addirittura arreca danno) quando praticata su stenosi coronariche che non limitano il flusso. Il numero di pazienti potenziali fruitori di un trattamento interventistico non sarebbe circoscritto, in quanto la ricerca sistematica effettuata dagli autori del PREVENT trial, attraverso metodiche di imaging coronarico, ha individuato come ben il 45% di pazienti con stenosi intermedie nelle quali l’esito della FFR risultava negativo, mostrasse caratteristiche di vulnerabilità. Tuttavia detto questo, non si può nascondere che l’entusiasmo con cui gli autori presentano i loro risultati (la frase finale dell’abstract recita testualmente “…questi dati supportano una espansione delle indicazioni della PCI che includa le placche vulnerabili non limitanti il flusso”) debba essere temperato da alcune riflessioni critiche. Innanzitutto il trial non includeva un protocollo specifico di valutazione delle placche lasciando ampia libertà riguardo alla metodica da utilizzare: di gran lunga la maggior parte dei pazienti è stata studiata con l’IVUS e solo una minoranza con tecniche più adatte a individuare alcuni aspetti rilevanti delle placche vulnerabili, come il contenuto lipidico (la spettroscopia a raggi infrarossi è stata applicata nel 42% dei casi) e lo spessore del cap fibroso (l’OCT è stato utilizzato solo nel 5% dei casi). Inoltre gli eventi, per quanto lungo fosse il follow-up (4.4 anni la mediana) sono risultati molto inferiori rispetto alle attese (il calcolo della numerosità del campione prevedeva a 2 anni nel gruppo in terapia medica un’incidenza dell’endpoint primario del 12%, mentre è stata osservata una percentuale di eventi molto inferiore, 3.4%). La componente dell’endpoint, che maggiormente ha contribuito al risultato favorevole alla PCI, è stata la necessità di rivascolarizzazione (0.1% versus 2.4%). Poichè lo studio era in aperto, questa differenza va considerata con molta cautela, per l’assenza nel gruppo in terapia medica di una “sham procedure”, come lo studio ORBITA ci ha insegnato[4]Al-Lamee R, Thompson D, Dehbi HM, et al. ORBITA investigators. Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial. Lancet. 2018 ;391:31-40. … Continua a leggere. Inoltre, va ricordato che la significatività statistica dell’endpoint primario viene persa sia a 4 che a 7 anni di follow-up. Peraltro il merito dello studio è stato quello di aver inaugurato un nuovo campo di ricerca clinica che potrebbe modificare radicalmente il percorso diagnostico invasivo nel paziente sottoposto a coronarografia: infatti se i risultati del PREVENT trial fossero confermati, la lesione nella quale l’FFR risultasse negativa dovrebbe essere sottoposta a imaging intracoronarico e a PCI, una volta documentata la vulnerabilità. Sono tuttora in corso quattro studi condotti con metodologia simile al PREVENT, tre dei quali in pazienti con infarto miocardico recente.
Editoriale: “PCI “preventiva” per le placche vulnerabili non emodinamicamente significative: una rivoluzione rimandata”
A cura di: Felice Gragnano, Università degli Studi della Campania “Luigi Vanvitelli” Caserta e Paolo Calabrò, A.O.R.N. “Sant’Anna e San Sebastiano, Caserta
Le placche coronariche “vulnerabili” sono lesioni aterosclerotiche che facilmente possono andare incontro a rottura, esponendo i pazienti a un elevato rischio di eventi coronarici e determinando complicanze trombotiche potenzialmente fatali[5]Bentzon JF, Otsuka F, Virmani R, Falk E. Mechanisms of plaque formation and rupture. Circ Res 2014;114(12):1852–66. doi:10.1161/CIRCRESAHA.114.302721. Le placche vulnerabili sono tipicamente costituite da un ampio core necrotico, da un cappuccio fibroso sottile (e.g., con spessore inferiore a 75 μm) e da un arco lipidico con estensione circonferenziale >180°, caratteristiche che identificano un fenotipo ad alto rischio di complicanze[6]Prati F, Romagnoli E, Gatto L, et al. Relationship between coronary plaque morphology of the left anterior descending artery and 12 months clinical outcome: the CLIMA study. Eur Heart J … Continua a leggere. Numerosi studi hanno dimostrato come la rottura acuta delle placche vulnerabili sia responsabile di oltre il 70% di tutti gli eventi trombotici coronarici fatali, indicandone un impatto determinante sulla prognosi dei pazienti con malattia coronarica[7]Falk E, Nakano M, Bentzon JF, Finn AV, Virmani R. Update on acute coronary syndromes: the pathologists’ view. Eur Heart J 2013;34(10):719–28. doi:10.1093/eurheartj/ehs411.. Inoltre, l’utilizzo di tecniche avanzate di imaging intravascolare coronarico ha permesso di dimostrare come la rottura di placca rappresenti la principale causa delle sindromi coronariche acute[8]Toutouzas K, Benetos G, Karanasos A, Chatzizisis YS, Giannopoulos AA, Tousoulis D. Vulnerable plaque imaging: updates on new pathobiological mechanisms. Eur Heart J 2015;36(45):3147–54. … Continua a leggere. In questo contesto, l’identificazione e il trattamento delle placche vulnerabili rimane estremamente importante per migliorare la gestione e la prognosi dei pazienti con cardiopatia ischemica. L’angiografia coronarica rimane, oggi, il gold standard per la diagnosi di malattia coronarica. Questa procedura presenta però una serie di limitazioni, tra cui la bassa sensibilità e specificità, l’elevata variabilità intra- e interoperatore, e l’incapacità di identificare in modo accurato la presenza di placche vulnerabili[9]Falk E, Nakano M, Bentzon JF, Finn AV, Virmani R. Update on acute coronary syndromes: the pathologists’ view. Eur Heart J 2013;34(10):719–28. doi:10.1093/eurheartj/ehs411.. Allo studio angiografico, infatti, la morfologia delle lesioni coronariche appare spesso “benigna”, e in assenza di una sindrome coronarica acuta o di una stenosi emodinamicamente significativa (con compromissione del flusso), queste lesioni non ricevono un trattamento di tipo interventistico. Tuttavia, rimane dibattuto quale sia la migliore strategia di trattamento di una placca vulnerabile non ostruttiva (che non determini ischemia). L’idea che le lesioni coronariche con morfologia vulnerabile, ma non emodinamicamente significative, abbiano un decorso favorevole è contraddetta dai dati di studi clinici che dimostrano come in pazienti con lesioni negative alla riserva frazionale di flusso (FFR), la presenza di un fibroateroma con cappuccio sottile (TCFA) si associ a un rischio di eventi cardiovascolari 5 volte superiore rispetto a quello dei pazienti senza TCFA[10]Kedhi E, Berta B, Roleder T, et al. Thin-cap fibroatheroma predicts clinical events in diabetic patients with normal fractional flow reserve: the COMBINE OCT-FFR trial. Eur Heart J … Continua a leggere. Per questo motivo, oltre all’angiografia coronarica, l’utilizzo di metodiche di imaging intracoronarico (ecografia intravascolare [IVUS] e tomografia a coerenza ottica [OCT]) risulta oggi essenziale per identificare le lesioni coronariche non emodinamicamente significative ma morfologicamente vulnerabili, con potenziali implicazioni per il follow-up e il trattamento dei pazienti. In questo contesto sicuramente complesso, si inseriscono i risultati del PREVENT trial, uno studio clinico multicentrico, open-label, randomizzato e controllato, recentemente pubblicato su The Lancet[11]Park S-J, Ahn J-M, Kang D-Y, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT): a … Continua a leggere. Lo studio ha arruolato 1.606 pazienti con placche vulnerabili all’imaging intravascolare ma non emodinamicamente significative (FFR >0.80). I pazienti venivano randomizzati (1:1) a un gruppo sperimentale, che riceveva un’angioplastica coronarica percutanea (PCI) “preventiva” con impianto di stent più terapia medica ottimale, e un gruppo di controllo, trattato con la sola terapia medica ottimale. L’età mediana della popolazione era di 65 anni; il 27% dei pazienti erano di sesso femminile e il 31% aveva una diagnosi di diabete. La presentazione clinica era un’angina stabile nell’84% dei pazienti e solo il 3% dei casi presentava un infarto acuto del miocardio. Nel gruppo sperimentale, il 67% dei pazienti eseguiva una PCI preventiva con drug-eluting stent (DES) mentre il restante 33% riceveva uno scaffold vascolare bioriassorbibile (BVS)(6). L’endpoint primario era un composito di morte per cause cardiache, infarto acuto del miocardio del vaso target, rivascolarizzazione del vaso target guidata da ischemia, oppure ospedalizzazione per angina instabile o progressiva, valutato a un follow-up di 2 anni. L’analisi principale è stata effettuata con un approccio “intention-to-treat”. A 2 anni di follow-up, l’endpoint primario si verificava in 3 pazienti (0.4%) nel gruppo trattato con PCI preventiva e in 27 pazienti (3.4%) nel gruppo trattato con sola terapia medica ottimale, con una differenza assoluta tra i due gruppi di -3.0% che risultava statisticamente significativa (95% CI: da -4.4 a -1.8; P=0.0003). Il beneficio della PCI preventiva era direzionalmente consistente per ciascuna delle componenti individuali dell’endpoint primario e si osservava fino a un follow-up a lungo termine di 7 anni[12]Park S-J, Ahn J-M, Kang D-Y, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT): a … Continua a leggere. La PCI preventiva riduceva, inoltre, l’endpoint composito “patient-oriented” di morte per tutte le cause, infarto acuto del miocardio, o rivascolarizzazione a 2 anni (differenza assoluta: -2.2%; 95% CI: da -4.1 a -0.2). Il profilo di sicurezza delle due strategie di trattamento risultava complessivamente simile. Le analisi per sottogruppi confermavano come il beneficio della PCI preventiva fosse indipendente dalle caratteristiche cliniche al basale (e.g., età, sesso, diabete, presentazione clinica)[13]Park S-J, Ahn J-M, Kang D-Y, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT): a … Continua a leggere. Il PREVENT trial segna un sostanziale passo in avanti nella nostra comprensione delle strategie di trattamento della placca vulnerabile, suggerendo il possibile beneficio clinico di una PCI preventiva. Nonostante i risultati del PREVENT trial siano di particolare interesse scientifico e clinico, lo studio presenta una serie di limitazioni, tra cui il disegno openlabel e la bassa incidenza di eventi clinici, che riflette l’inclusione di una popolazione a basso rischio e in larga misura costituita da pazienti con sindrome coronarica cronica[14]Park S-J, Ahn J-M, Kang D-Y, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT): a … Continua a leggere. Lo studio è stato inoltre condotto in soli 4 paesi (Korea del Sud, Giappone, Taiwan e Nuova Zelanda); per questo motivo la generalizzabilità dei risultati nella popolazione europea e americana rimane non chiara e dovrà essere valutata in studi successivi. In conclusione, il PREVENT è il primo trial clinico randomizzato volto a indicare la possibilità che pazienti selezionati con sindrome coronarica cronica e placche vulnerabili (non emodinamicamente significative) possono beneficiare di una PCI preventiva in aggiunta alla terapia medica ottimale. Questi risultati hanno importanti implicazioni per la gestione dei pazienti con malattia coronarica nella pratica clinica contemporanea e per il disegno di ulteriori studi clinici che dovranno definire, con maggiore chiarezza, qual è la migliore strategia terapeutica nell’ampia popolazione di soggetti con placche vulnerabili ad alto rischio di eventi cardiovascolari.
Bibliografia[+]
| ↑1 | Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS guidelines on myocardial revascularization.Eur Heart J 2019; 40: 87–165; Lawton JS, Tamis-Holland JE, Bangalore S, et al. 2021 ACC/AHA/SCAI guideline for coronary artery revascularization: a report of the American. College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation 2022; 145: e18–114 |
|---|---|
| ↑2 | Gallone G, Bellettini M, Gatti M, et al. Coronary plaque characteristics associated with major adverse cardiovascular events in atherosclerotic patients and lesions: a systematic review and meta-analysis. JACC Cardiovasc Imaging 2023; 16: 1584–604.; Stone GW, Maehara A, Lansky AJ, et al. A prospective naturalhistory study of coronary atherosclerosis. N Engl J Med 2011;364: 226–35. |
| ↑3 | Stone GW, Maehara A, Ali ZA, et al. Percutaneous coronary intervention for vulnerable coronary atherosclerotic plaque. J Am Coll Cardiol 2020; 76: 2289–301. |
| ↑4 | Al-Lamee R, Thompson D, Dehbi HM, et al. ORBITA investigators. Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial. Lancet. 2018 ;391:31-40. doi:10.1016/S0140-6736(17)32714-9. |
| ↑5 | Bentzon JF, Otsuka F, Virmani R, Falk E. Mechanisms of plaque formation and rupture. Circ Res 2014;114(12):1852–66. doi:10.1161/CIRCRESAHA.114.302721 |
| ↑6 | Prati F, Romagnoli E, Gatto L, et al. Relationship between coronary plaque morphology of the left anterior descending artery and 12 months clinical outcome: the CLIMA study. Eur Heart J 2020;41(3):383–91. doi:10.1093/eurheartj/ehz520 |
| ↑7, ↑9 | Falk E, Nakano M, Bentzon JF, Finn AV, Virmani R. Update on acute coronary syndromes: the pathologists’ view. Eur Heart J 2013;34(10):719–28. doi:10.1093/eurheartj/ehs411. |
| ↑8 | Toutouzas K, Benetos G, Karanasos A, Chatzizisis YS, Giannopoulos AA, Tousoulis D. Vulnerable plaque imaging: updates on new pathobiological mechanisms. Eur Heart J 2015;36(45):3147–54. doi:10.1093/eurheartj/ehv508. |
| ↑10 | Kedhi E, Berta B, Roleder T, et al. Thin-cap fibroatheroma predicts clinical events in diabetic patients with normal fractional flow reserve: the COMBINE OCT-FFR trial. Eur Heart J 2021;42(45):4671–9. doi:10.1093/eurheartj/ehab433. |
| ↑11, ↑12, ↑14 | Park S-J, Ahn J-M, Kang D-Y, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT): a multicentre, open-label, randomised controlled trial. Lancet 2024;403(10438):1753–65. doi:10.1016/S0140-6736(24)00413-6. |
| ↑13 | Park S-J, Ahn J-M, Kang D-Y, et al. Preventive percutaneous coronary intervention versus optimal medical therapy alone for the treatment of vulnerable atherosclerotic coronary plaques (PREVENT): a multicentre, open-label, randomised controlled trial. Lancet 2024;403(10438):1753–65. doi:10.1016/S0140-6736(24)00413-6. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

