Inquadramento
Uno dei dilemmi tuttora irrisolti della terapia antipiastrinica dopo impianto di stent è la durata della doppia terapia antipiastrinica, soprattutto in una popolazione ad alto rischio emorragico. Recentemente l’Academic Research Consortium (ARC) ha proposto una definizione di “high bleeding risk” (HBR), basata sulla presenza di criteri maggiori e minori[1]Urban P., Mehran R., Colleran R., et al. Defining high bleeding risk in patients undergoing percutaneous coronary intervention: a consensus document from the Academic Research Consortium for High … Continua a leggere. Journal Map ha già dedicato spazio e commenti a questo tema (vedi numero 5). Tuttavia alcuni di questi criteri ARC-HBR si associano non solo a un alto rischio emorragico, ma anche a un rischio ischemico elevato. Quale sia poi la mortalità successiva al verificarsi di un evento emorragico o ischemico in questa popolazione non è noto.
Lo studio in esame
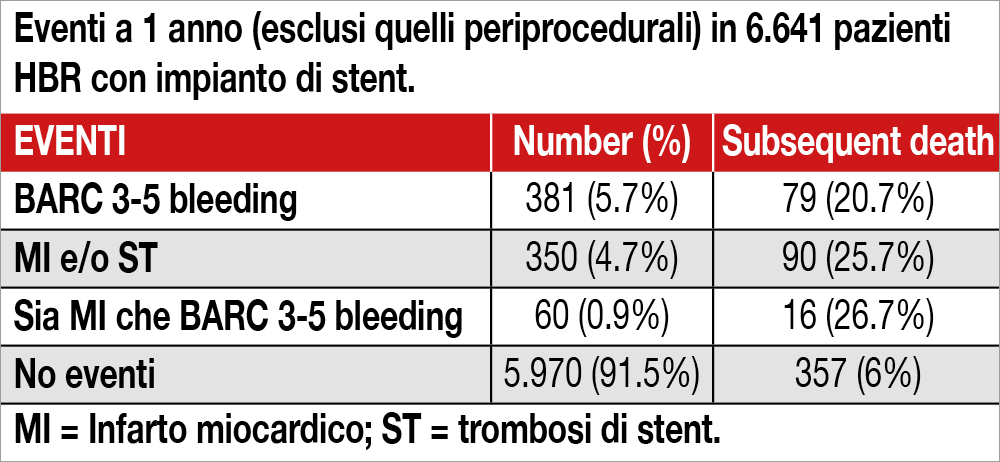
Gli Autori hanno analizzato i dati individuali di 6.641 pazienti sottoposti a impianto di stent, definiti “HBR” secondo la definizione ARC, inclusi in 6 studi condotti tra il 2009 e il 2017 (età media 78 anni, 68% dei pazienti con età >75 anni), per sviluppare e validare modelli di rischio emorragico e ischemico in questa popolazione. Gli eventi emorragici (bleeding BARC 3-5) e ischemici (infarto miocardico -MI- e trombosi dello stent) a 1 anno (con l’esclusione di quelli peri-procedurali) sono riportati nella Tabella. Rispetto ai pazienti senza eventi, l’hazard ratio per la mortalità è stato 3.7 (95% CI 2.9-4.8) dopo un bleeding e 6.1 (95% CI 4.8-7.7) dopo un MI. I modelli prognostici sia per BARC 3-5 bleeding (C-statistics 0.68) che per MI (C-statistics 0.69) sono stati costruiti su 8 variabili ciascuno, di cui 4 comuni per BARC 3-5 bleeding e MI (anemia, insufficienza renale, PCI complessa, fumo). Calcolando rischio ischemico ed emorragico in ogni paziente, in poco meno della metà (44%) prevaleva il rischio ischemico, nel 23% prevaleva il rischio emorragico, mentre nei rimanenti pazienti (33%) i due tipi di rischio risultavano simili.
Take home message
In una ampia coorte di pazienti sottoposti a impianto di stent e giudicati ad alto rischio emorragico secondo i criteri ARC-HBR, sono stati costruiti modelli prognostici che permettono di calcolare per ogni paziente il rischio di futuri eventi ischemici ed emorragici, consentendo di individualizzare tipo e durata di terapia antitrombotica.
Interpretazione dei dati
Lo studio offre interessanti spunti di riflessione. Sicuramente singolare il fatto che questa analisi consideri, partendo da una casistica di oltre 12.000 pazienti, solo coloro che, secondo la definizione ARC-HBR, sarebbero stati ad alto rischio emorragico. Tuttavia, quando la popolazione veniva stratificata in base agli eventi registrati a 1 anno, in gruppi a prevalente rischio ischemico od emorragico, oltre il 40% dei pazienti risultava essere a elevato rischio ischemico, mentre soltanto nel 23% dei pazienti il rischio emorragico era preminente. Inoltre l’incidenza di mortalità risultava essere circa il doppio dopo un evento ischemico (MI, trombosi di stent) rispetto a un evento emorragico (vedi Tabella). Il dato è discrepante rispetto ad analisi precedenti[2]Valgimigli M., Costa F., Lokhnygina Y., et al. Trade-off of myocardial infarction vs. bleeding types on mortality after acute coronary syndrome: lessons from the Thrombin Receptor Antagonist for … Continua a leggere che mostravano un analogo peso prognostico di bleeding e infarto miocardico.
L’opinione di Claudio Montalto
Cardiologia Interventistica, Ospedale Niguarda, Milano
Le più recenti Linee Guida ESC sull’infarto miocardico senza sopraslivellamento del tratto ST consigliano di individuare i pazienti a rischio emorragico particolarmente elevato (HBR) utilizzando uno score di rischio tra il PRECISE-DAPT e ARC-HBR[3]Collet J-P., Thiele H., Barbato E., et al. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the … Continua a leggere. Tuttavia, se è facile individuare i pazienti a rischio maggiore, più complesso è bilanciare durata e intensità della duplice terapia antitrombotica (DAPT) nella pratica clinica. Infatti, molto spesso i fattori che predispongono allo sviluppo di una complicanza emorragica o ischemica sono sovrapponibili e sovrapposti nello stesso paziente e uno strumento che permetta una stratificazione adeguata è da sempre un Sacro Graal nella ricerca in ambito DAPT. Di recente, Urban e colleghi hanno analizzato un dataset di 6.641 pazienti HBR secondo i criteri ARC[4]Urban P., Mehran R., Colleran R., et al. Defining high bleeding risk in patients undergoing percutaneous coronary intervention: a consensus document from the Academic Research Consortium for High … Continua a leggere ampiamente validati nella pratica clinica. Nonostante aver usato dati provenienti da trial randomizzati e 1 registro prospettico, si tratta di pazienti “veramente” HBR, visto che, a un anno, l’occorrenza di sanguinamenti maggiori è di 5.7% (sopra la soglia teorica del 4% per definire popolazione ad HBR). Il primo dato interessante di questa analisi è confermare che i pazienti HBR sono intrinsecamente anche a elevato rischio di eventi ischemici con una occorrenza di infarto miocardico e stent thrombosis del 5.3% a un anno. Inoltre, tra questi pazienti HBR, quelli che hanno avuto un evento di sanguinamento presentavano un rischio di morte maggiore di 3.7 volte rispetto alla popolazione HBR senza eventi avversi. Invece, quelli che hanno avuto un evento ischemico presentavano un rischio di morte 6.1 volte maggiore: se ne evince che un evento ischemico, nel contesto dei pazienti HBR, è associato a un rischio di mortalità che è maggiore di oltre una volta e mezzo rispetto a un evento emorragico. La novità del paper sta proprio in questa considerazione: avendo gli eventi ischemici una maggiore importanza prognostica, gli Autori propongono una soglia sotto la quale il rischio di sanguinamento, pur superando numericamente il rischio ischemico, concorre a una mortalità aggiuntiva minore rispetto a quella associata al rischio ischemico. Un’altra soglia invece definisce il punto in cui, incrementando molto il rischio emorragico, la mortalità aggiunta da un eventuale sanguinamento supera quella aggiunta da un eventuale evento ischemico. Tra le due soglie, vi è un’area in cui la mortalità aggiunta da un evento ischemico o emorragico è la stessa. Ad esempio, un paziente che ha un rischio di sanguinamento del 5%, e un rischio ischemico del 1.25%, avrà un rischio di morte collegata a sanguinamento maggiore rispetto a quello collegato al rischio ischemico. Al contrario, per un paziente con lo stesso rischio emorragico ma un rischio ischemico del 5%, o per un altro con rischio ischemico del 10%, la mortalità aggiunta dall’eventuale sanguinamento sarebbe uguale o inferiore rispetto a quella aggiunta dall’eventuale evento ischemico. In questo senso gli Autori propongono una soglia di “trade-off”, ovvero una soglia di compromesso tra la mortalità collegata ai due eventi avversi, come ulteriore parametro da considerare per calibrare la DAPT nei pazienti HBR. Meritevolmente, gli Autori hanno incorporato questi calcoli in una applicazione (“ARC portal”) disponibile gratuitamente su smartphone e che permette, in primis, di individuare i pazienti ad alto rischio di sanguinamento secondo i criteri ARC e, in secundis, tra questi di individuare il rischio di mortalità collegato a eventi ischemici e di sanguinamento e da quale lato della bilancia far pendere il suddetto “trade-off”. Pur arricchendo la galassia ARC-HBR di un nuovo tool diagnostico, è necessario considerare alcune limitazioni, tra cui il fatto che gli stessi criteri ARC-HBR sono stati riadattati a seconda delle informazioni disponibili in dataset raccolti antecedentemente. Questo mette in luce il più grosso limite di questa definizione che, nata per scopi di ricerca e trialistica, è complessa e farraginosa da applicare rigorosamente nella pratica clinica, a differenza del più snello PRECISE-DAPT score[5]Costa F., van Klaveren D., James S., et al. Derivation and validation of the predicting bleeding complications in patients undergoing stent implantation and subsequent dual antiplatelet therapy … Continua a leggere. Quest’ultimo, a sua volta, individua pazienti a elevato rischio di sanguinamento che non beneficiano di durata della DAPT prolungata. Tuttavia informazioni riguardo un eventuale “trade-off” in termini di mortalità in quest’area di applicazione non sono ancora disponibili.
Bibliografia[+]
| ↑1, ↑4 | Urban P., Mehran R., Colleran R., et al. Defining high bleeding risk in patients undergoing percutaneous coronary intervention: a consensus document from the Academic Research Consortium for High Bleeding Risk. Eur Heart J 2019;40(31):2632–53. Doi: 10.1093/eurheartj/ehz372. |
|---|---|
| ↑2 | Valgimigli M., Costa F., Lokhnygina Y., et al. Trade-off of myocardial infarction vs. bleeding types on mortality after acute coronary syndrome: lessons from the Thrombin Receptor Antagonist for Clinical Event Reduction in Acute Coronary Syndrome (TRACER) randomized trial. Eur Heart J 2017;38:804–10. Doi: 10.1093/eurheartj/ehw525. |
| ↑3 | Collet J-P., Thiele H., Barbato E., et al. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: The Task Force for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J 2021;42(14):1289–367. Doi: 10.1093/eurheartj/ ehaa575. |
| ↑5 | Costa F., van Klaveren D., James S., et al. Derivation and validation of the predicting bleeding complications in patients undergoing stent implantation and subsequent dual antiplatelet therapy (PRECISE-DAPT) score: a pooled analysis of individual-patient datasets from clinical trials. Lancet 2017;389:1025–34. Doi: 10.1016/S0140-6736(17)30397-5. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

