Inquadramento
L’obesità è spesso presente nei pazienti con scompenso cardiaco a frazione di eiezione conservata, rappresentando anche una condizione di scarsa risposta alla terapia e prognosi peggiore[1]Obokata M, Reddy YNV, Pislaru SV, Melenovsky V, Borlaug BA. Evidence supporting the existence of a distinct obese phenotype of heart failure with preserved ejection fraction. Circulation 2017;136:6-19. Tuttavia, non vi sono documentazioni che la riduzione dell’obesità, utilizzando farmaci specifici, possa migliorare i sintomi e la capacità funzionale in questi pazienti.
Lo studio in esame
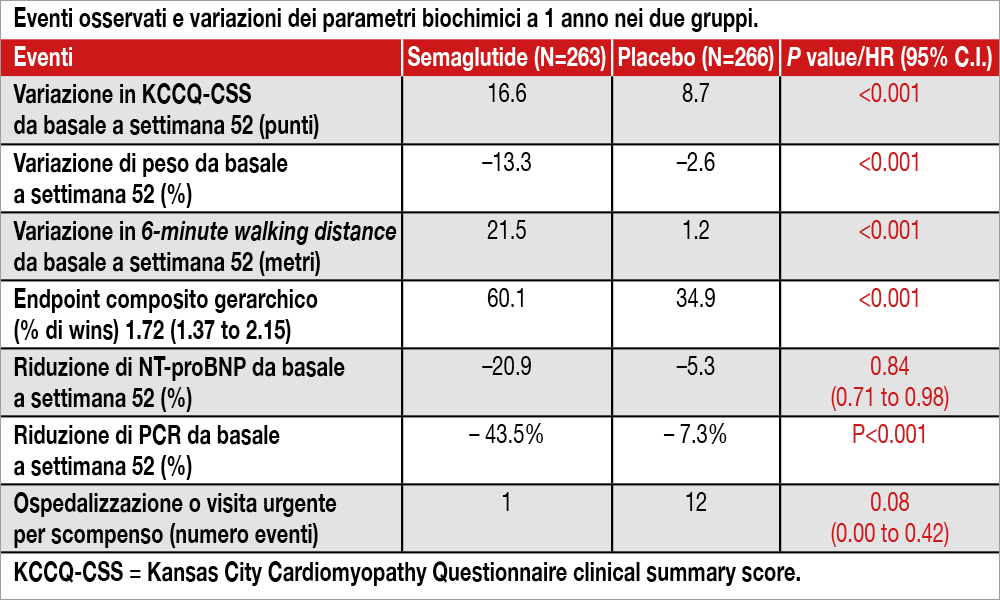
Studio multicentrico internazionale (condotto in 96 centri di 13 Paesi in Asia, Europa – di cui 2 italiani –, Nord e Sud America) che ha randomizzato in doppio cieco 529 pazienti con scompenso cardiaco a frazione di eiezione preservata (HFpEF) e indice di massa corporea (BMI) ≥30 a semaglutide 2.4 mg una volta alla settimana s.c. (n=263) o placebo (n=266) per 52 settimane. Il duplice primary endpoint era rappresentato dal cambiamento rispetto al basale del Kansas City Cardiomyopathy Questionnaire clinical summary score (KCCQCSS, riguardante la qualità di vita, i sintomi e le limitazioni fisiche) e il cambiamento del peso. I valori mediani di età erano: età 70 anni, BMI 37, NTproBNP 451 pg/ml, EF 57%, proteina C reattiva (PCR) 3.8 mg/L. Oltre la metà dei pazienti (52%) era in fibrillazione atriale e l’81% dei pazienti era in terapia diuretica. Il cambiamento medio del KCCQ-CSS era di 16.6 punti con semaglutide e 8.7 punti con placebo (differenza 7.8%; 95% confidence interval [CI], da 4.8 a 10.9; P<0.001), e il cambiamento di peso era −13.3% con semaglutide e −2.6% con placebo (differenza, −10.7%; 95% CI, da −11.9 a −9.4; P<0.001). I dati relativi a un endpoint secondario composito confermatorio valutato con la tecnica statistica del “win-ratio” (ospedalizzazione o visita urgente con necessità di terapia infusiva, variazioni di almeno 15 punti nel KCCQ-CSS e di 30 metri nel 6m-WTD), oltre alle variazioni a 1 anno di follow-up del 6m-WT e di PCR sono presentate nella Tabella.
Take home message
Nei pazienti con scompenso cardiaco a FE preservata e obesità, il trattamento con semaglutide (2.4 mg) ha prodotto, rispetto al placebo, una maggior riduzione dei sintomi, un miglioramento della capacità di esercizio e una maggior perdita di peso.
Interpretazione dei dati
L’obesità non solo è molto frequente nei pazienti con HFpEF, ma sembra anche giocare un ruolo patogenetico in questa condizione clinica. L’adiposità, soprattutto addominale, rappresenta uno stimolo infiammatorio (testimoniato da un incremento di indici quali la PCR) che si associa a resistenza all’insulina, elevati valori pressori, ipertrofia ventricolare sinistra, disfunzione diastolica[2]Kitzman DW, Nicklas BJ. Pivotal role of excess intra-abdominal adipose in the pathogenesis of metabolic/obese HFpEF.JACC Heart Fail 2018;6:1008-10.. L’obesità comporta anche una riduzione di produzione di peptide natriuretico e conseguente riduzione della natriuresi. La semaglutide, in questo studio, ha migliorato notevolmente la qualità di vita e la distanza percorsa al 6-minute walking test, parallelamente a una riduzione del peso. Questo studio sembra confutare il cosiddetto “obesity paradox”, un fenomeno che consisterebbe in un peggioramento clinico e prognostico quando si riduce il peso in pazienti obesi scompensati[3]Zamora E, Díez-López C, Lupón J, et al. Weight loss in obese patients with heart failure. J Am Heart Assoc 2016; 5(3):e002468..
Tuttavia, queste osservazioni non hanno spesso distinto tra un’intenzionale perdita di peso e un dimagramento non-intenzionale. Quest’ultimo può essere dovuto a un aggravarsi della patologia al punto da determinare una fase di cachessia, che conduce a una fase avanzata e spesso irreversibile di scompenso. Il meccanismo d’azione della semaglutide, che conduce agli effetti clinicamente rilevanti documentati in questo studio, suggerisce una riduzione della componente infiammatoria (evidenziato dalla discesa dei valori di PCR) oltre a un miglioramento emodinamico (evidenziato dalla riduzione di NTproBNP). Rilevante anche la diminuzione significativa di eventi avversi, tra cui le infezioni e i parossismi di fibrillazione atriale. Se questi benefici dipendano dalla sola riduzione del peso o da effetti diretti del farmaco, indipendenti dalla perdita di peso, non è al momento noto. Infine, è da osservare che una limitazione importante dello studio consiste in un modesto utilizzo di inibitori di SGLT2 nella popolazione arruolata (3.5%): il programma STEP-HFpEF include, tuttavia, anche uno studio (anch’esso concluso e i cui dati saranno resi noti a breve) analogo a quello qui analizzato, ma condotto in pazienti diabetici, di cui circa un terzo trattati con inibitori di SGLT2.
Editoriale: “Semaglutide nello scompenso cardiaco, il dato è tratto. Commento dello studio STEP-HFpEF”
A cura di: Claudio Cimminiello, Fondazione “Arianna Anticoagulazione”, Bologna
Presentato lo scorso agosto al congresso ESC 2023 e pubblicato simultaneamente su New England Journal of Medicine[4]Kosiborod MN, Abildstrøm SZ, Borlaug BA, Butler J, Rasmussen S, Davies M, Hovingh GK, Kitzman DW, Lindegaard ML, Møller DV, Shah SJ, Treppendahl MB, Verma S, Abhayaratna W, Ahmed FZ, Chopra V, … Continua a leggere, lo studio STEP-HFpEF ha valutato gli effetti di un Glucagon-Like Peptide 1 receptor agonist (GLP-1 RA), semaglutide, somministrato a soggetti obesi non diabetici affetti da insufficienza cardiaca con frazione di eiezione (FE) preservata. I dettagli dello studio sono presentati nell’articolo che precede e qui basterà ricordare che semaglutide determinava il significativo miglioramento dei sintomi valutati mediante il punteggio Kansas City Cardiomyopathy Questionnaire Clinical Summary Score (KCCQCSS) e una significativa perdita di peso, centrando entrambi gli endpoint primari. La sicurezza del trattamento è stata buona, con una percentuale di eventi avversi più elevata nel gruppo placebo rispetto a quello semaglutide. I risultati dello studio potrebbero avere una lettura molto semplice (che è in sostanza quella proposta dagli ideatori del trial): indurre il calo di peso nei pazienti obesi con scompenso e con frazione di eiezione preservata migliora i sintomi dell’insufficienza cardiaca. Semaglutide, diversamente dagli SGLT2i, non emerge come “aggiunta” alle terapie cardine dello scompenso. Ma le domande restano ugualmente, a partire da quali siano le basi fisiopatologiche/emodinamiche alla base dell’osservato miglioramento dei sintomi. Qui i dati sembrano incoraggianti: la distanza percorsa nel test del cammino di 6 minuti era significativamente più elevata nei trattati con semaglutide, i livelli di NT-proBNP si riducevano maggiormente nel trattamento attivo e l’endpoint gerarchicorelativo allo scompenso cardiaco, valutato con la metodica del win-ratio mostrava più win nel braccio semaglutide. Ci si chiede allora se anche semaglutide non debba essere testato in ampi studi clinici in pazienti con scompenso – non solo negli obesi – che vedano rappresentati tutti i fenotipi dell’insufficienza cardiaca e quindi anche i pazienti con FE ridotta e includendo anche i diabetici in trial dagli end point hard (morte e ricovero per scompenso). Questa prospettiva è da valutare alla luce di quanto già conosciamo e dei dati che si stanno accumulando. Nell’ottobre 2023 è stata pubblicata una sottoanalisi prespecificata dello STEP-HFpEF che valutava il vantaggio di semaglutide in funzione dei diversi valori di FE (da 45% a 49%, da 50% a 59% e dal 60% in su)[5]Butler J, Abildstrøm SZ, Borlaug BA, Davies MJ, Kitzman DW, Petrie MC, Shah SJ, Verma S, Abhayaratna WP, Chopra V, Ezekowitz JA, Fu M, Ito H, Lelonek M, Núñez J, Perna E, Schou M, Senni M, van der … Continua a leggere. I benefici in termini dei due endpoint primari erano indipendenti dal valore di FE. Di certo mancano i dati sulla FE ridotta, ma semaglutide sembra promettere un’azione simile a quella degli SGLT2i, con uno spettro d’azione che abbraccia tutti i fenotipi; evento inedito se guardiamo alle terapie “storiche” come betabloccanti, ACEi/ARB e MRA. Nel recente studio SELECT[6]Lincoff AM, Brown-Frandsen K, Colhoun HM, Deanfield J, Emerson SS, Esbjerg S, Hardt-Lindberg S, Hovingh GK, Kahn SE, Kushner RF, Lingvay I, Oral TK, Michelsen MM, Plutzky J, Tornøe CW, Ryan DH; … Continua a leggere condotto in pazienti obesi e con storia di eventi aterosclerotici, semaglutide, oltre a ridurre l’endpoint cardiovascolare primario del 20% ha mostrato un favorevole effetto anche sullo scompenso cardiaco. Tale end point non è stato valutato dal punto di vista statistico perché gerarchicamente subordinato alla mortalità cardiovascolare che non era apparsa significativamente ridotta da semaglutide. Si tratta di indizi incoraggianti che dovrebbero essere confermati in studi ad hoc. Accanto alle speranze devono, tuttavia, essere ricordati gli aspetti controversi. La classe dei GLP-1 RA (compresa semaglutide) valutata in una metanalisi di 7 studi per complessivi 56.000 pazienti, ha fornito una prova di modesta efficacia, nei diabetici, in termini di rischio di ricovero per scompenso[7]Kristensen SL, Rørth R, Jhund PS, Docherty KF, Sattar N, Preiss D, Køber L, Petrie MC, McMurray JJV. Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with … Continua a leggere e, soprattutto, nel già citato studio SELECT, la tollerabilità di semaglutide ha posto problemi. Nei pazienti del SELECT gli eventi avversi che hanno portato all’interruzione definitiva dello studio si sono verificati nel 16,6% dei soggetti in semaglutide e nell’8,2% nel gruppo placebo (P<0,001). Nausea, vomito e diarrea erano le più frequenti tra tali reazioni avverse, ma significativamente più frequenti in semaglutide erano anche i disturbi delle vie biliari. Appare chiaro che, nonostante il setting clinico diverso, questi dati osservati nella popolazione di oltre 17.000 pazienti del SELECT sembrano decisamente più affidabili di quelli, apparentemente rassicuranti, raccolti nei 529 pazienti dello studio STEP-HFpEF. Il dado per semaglutide nei pazienti con insufficienza cardiaca è tratto, ma non ci si può fermare allo studio STEP-HFpEF. Servono più informazioni sui pazienti non obesi, sui diabetici, sui diversi fenotipi dello scompenso circa l’efficacia e la sicurezza clinica testata in migliaia di pazienti, valutando i classici hard end point nell’ambito della terapia raccomandata dalle Linee Guida, anche in associazione con gli SGLT2i.
Bibliografia[+]
| ↑1 | Obokata M, Reddy YNV, Pislaru SV, Melenovsky V, Borlaug BA. Evidence supporting the existence of a distinct obese phenotype of heart failure with preserved ejection fraction. Circulation 2017;136:6-19 |
|---|---|
| ↑2 | Kitzman DW, Nicklas BJ. Pivotal role of excess intra-abdominal adipose in the pathogenesis of metabolic/obese HFpEF.JACC Heart Fail 2018;6:1008-10. |
| ↑3 | Zamora E, Díez-López C, Lupón J, et al. Weight loss in obese patients with heart failure. J Am Heart Assoc 2016; 5(3):e002468. |
| ↑4 | Kosiborod MN, Abildstrøm SZ, Borlaug BA, Butler J, Rasmussen S, Davies M, Hovingh GK, Kitzman DW, Lindegaard ML, Møller DV, Shah SJ, Treppendahl MB, Verma S, Abhayaratna W, Ahmed FZ, Chopra V, Ezekowitz J, Fu M, Ito H, Lelonek M, Melenovsky V, Merkely B, Núñez J, Perna E, Schou M, Senni M, Sharma K, Van der Meer P, von Lewinski D, Wolf D, Petrie MC; STEP-HFpEF Trial Committees and Investigators. Semaglutide in Patients with Heart Failure with Preserved Ejection Fraction and Obesity. N Engl J Med. 2023;389:1069-1084. |
| ↑5 | Butler J, Abildstrøm SZ, Borlaug BA, Davies MJ, Kitzman DW, Petrie MC, Shah SJ, Verma S, Abhayaratna WP, Chopra V, Ezekowitz JA, Fu M, Ito H, Lelonek M, Núñez J, Perna E, Schou M, Senni M, van der Meer P, von Lewinski D, Wolf D, Altschul RL, Rasmussen S, Kosiborod MN, Semaglutide Effects According to Ejection Fraction in Heart Failure with Preserved Ejection Fraction and Obesity. JACC 2023;82:2087-2096. |
| ↑6 | Lincoff AM, Brown-Frandsen K, Colhoun HM, Deanfield J, Emerson SS, Esbjerg S, Hardt-Lindberg S, Hovingh GK, Kahn SE, Kushner RF, Lingvay I, Oral TK, Michelsen MM, Plutzky J, Tornøe CW, Ryan DH; SELECT Trial Investigators. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med. 2023. doi:10.1056/NEJMoa2307563. |
| ↑7 | Kristensen SL, Rørth R, Jhund PS, Docherty KF, Sattar N, Preiss D, Køber L, Petrie MC, McMurray JJV. Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. Lancet Diabetes Endocrinol. 2019;7:776-785. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

