Inquadramento
Nei pazienti con sindrome coronarica acuta (ACS), la de-escalation è una strategia di terapia antipiastrinica che consiste in un trattamento iniziale con ASA associata a un inibitore potente del recettore P2Y12 (ticagrelor o prasugrel fulldose) seguita da uno “switch” a un inibitore meno potente (clopidogrel o prasugrel lowdose). Essa si basa sull’osservazione che il rischio ischemico in questi pazienti è elevato nel periodo immediatamente successivo alla fase acuta, per diminuire progressivamente nelle fasi successive, mentre il rischio emorragico resta costante[1]Barnathan ES, Schwartz JS, Taylor L, Laskey WK, Kleaveland JP, Kussmaul WG, Hirshfeld JW Jr. Aspirin and dipyridamole in the prevention of acute coronary thrombosis complicating coronary angioplasty. … Continua a leggere. L’efficacia e la sicurezza di questa strategia è stata oggetto di alcune metanalisi, basate sui risultati globali dei vari studi inclusi (study-level analyses), i cui esiti sono tuttavia inficiati dall’eterogeneità delle casistiche e dall’impossibilità di approfondire il rischio ischemico ed emorragico dei pazienti inseriti. Le metanalisi basate, invece, sui dati di tutti i pazienti (patient-level analyses) permettono di ottenere maggiori informazioni e di individuare gruppi di pazienti che potrebbero meglio rispondere clinicamente a questa strategia terapeutica.
Lo studio in esame
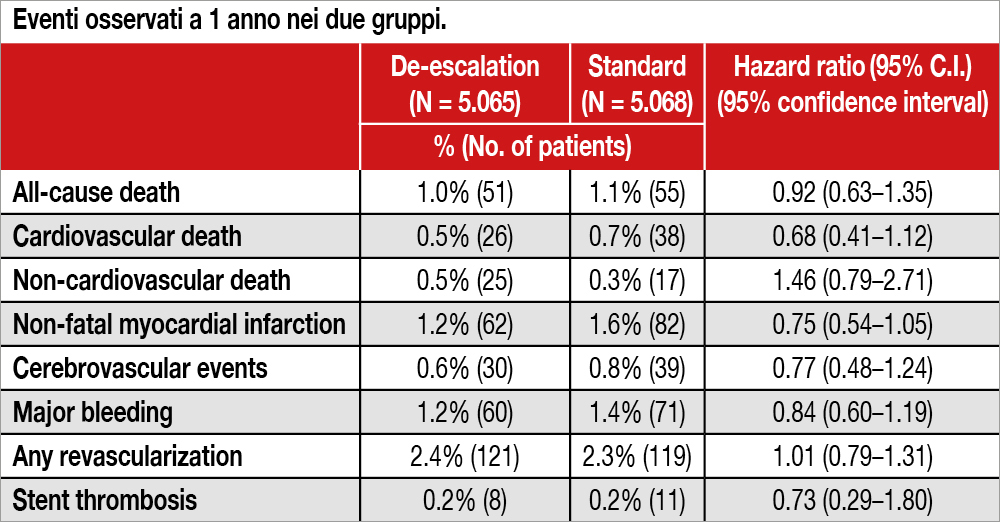
Analisi di quattro trial che hanno confrontato una strategia di de-escalation con una doppia terapia antipiastrinica (DAPT) standard di 12 mesi in pazienti ACS trattati con PCI: TROPICAL-ACS (de-escalation guidata da test di funzionalità piastrinica con switch da prasugrel a clopidogrel), POPular Genetics (de-escalation guidata da test genetico con uno switch da prasugrel/ticagrelor a clopidogrel), HOST-REDUCE-POLYTECH-ACS (de-escalation non guidata con switch da prasugrel 10 mg a prasugrel 5 mg), TALOS (de-escalation non guidata da ticagrelor a clopidogrel). Globalmente sono stati inclusi 10.133 pazienti (5.065 trattati con strategia di de-escalation e 5.068 con DAPT standard) i cui singoli dati sono stati messi a disposizione degli Autori (età mediana 57.8 anni, 86% con infarto miocardico pregresso, 25% diabetici e il 15% con una coronaropatia trivasale). L’endpoint ischemico (morte cardiovascolare, infarto miocardico ed eventi cerebrovascolari) e quello emorragico (bleeding maggiore e minore) a 1 anno sono risultati inferiori nel gruppo de-escalation rispetto a standard DAPT (2.3% vs 3.0%, hazard ratio [HR] 0.761, 95% confidence interval [CI] 0.597-0.972, log rank p=0.029; 6.5% vs 9.1%, HR 0.701, 95% CI 0.606-0.811, log rank p<0.001). Tra i due gruppi non veniva osservata alcuna differenza per mortalità per ogni causa e per bleeding maggiore (Tabella). Una de-escalation non guidata ha avuto un maggior effetto sulla riduzione di bleeding (HR 0.50, 95% CI 0.38–0.67, p<0.001), rispetto a una de-escalation guidata (HR 0.79, 95% CI 0.67–0.94, p=0.008, p for interaction = 0.007), ma non sull’endpoint ischemico.
Take home message
In questa metanalisi basata sui dati individuali dei pazienti ACS trattati con PCI, la strategia di de-escalation, rispetto a una DAPT standard di 12 mesi, è risultata associata a una riduzione dell’endpoint ischemico ed emorragico a 1 anno di follow-up. La riduzione del bleeding era più evidente nei pazienti randomizzati a una de-escalation non guidata, rispetto a quelli assegnati a una de-escalation guidata.
Interpretazione dei dati
I risultati di questo studio sono in linea con quelli di precedenti metanalisi (benchè eseguite sui dati globali degli studi inclusi) che hanno mostrato come la strategia di de-escalation riduca il bleeding “con rilevanza clinica”, rispetto a una standard DAPT, con un trend di riduzione degli eventi cardiaci avversi (MACE)[2] Laudani C, Greco A, Occhipinti G, et al. Short duration of DAPT versus de-escalation after percutaneous coronary intervention for acute coronary syndromes. JACC Cardiovasc Interv 2022; 15:268–277.. Nel presente studio si è osservata una riduzione significativa anche dell’endpoint ischemico, un dato apparentemente paradossale perché con la strategia di de-escalation si utilizza per un periodo maggiore di follow-up un inibitore del recettore piastrinico P2Y12 meno potente rispetto a una strategia di DAPT standard. Gli Autori spiegano questo dato “controintuivo” come una conseguenza della riduzione del bleeding ottenuta con la de-escalation: infatti, si può ipotizzare che i pazienti assegnati alla DAPT standard, che sperimentino con maggior frequenza episodi emorragici anche minori, abbiano una minore compliance ai farmaci antipiastrinici loro assegnati. Un altro dato intrigante dello studio consiste nella maggiore riduzione degli eventi emorragici grazie all’utilizzo di una strategia di de-escalation non guidata rispetto a una guidata. Questo potrebbe dipendere dal fatto che, nel gruppo di pazienti assegnati a una strategia di de-escalation guidata, sono compresi anche quei pazienti che continuano a utilizzare farmaci più potenti perchè risultati essere “poor metabolizers” di clopidogrel. Verosimilmente, anche la diversa etnia dei pazienti randomizzati (sono stati inseriti solo asiatici negli studi di de-escalation non guidata) potrebbe avere giocato un ruolo nella genesi di questa differenza.
Editoriale: “Sfida al dogma della doppia terapia antiaggregante fissa dopo sindrome coronarica acuta: verso una nuova era”
A cura di: Ovidio De Filippo, A.O.U. “Città della Salute e della Scienza”, Torino
Il contesto storico
La raccomandazione di una doppia terapia antiaggregante (dual antiplatelet therapy, DAPT) dopo una sindrome coronarica acuta (SCA), trattata con angioplastica percutanea (PCI) è stata suggerita per la prima volta oltre tre decadi fa[3]Barnathan ES, Schwartz JS, Taylor L, Laskey WK, Kleaveland JP, Kussmaul WG, Hirshfeld JW Jr. Aspirin and dipyridamole in the prevention of acute coronary thrombosis complicating coronary angioplasty. … Continua a leggere, ma è diventata il gold standard durante l’epoca dei bare metal stent, dal momento che questi device si associavano a tassi significativi di restenosi e trombosi di stent. La successiva introduzione degli stent a rilascio di farmaco (DES), con il relativo incremento dei tassi di trombosi di stent tardiva dovuta al rallentamento del processo di re-endotelizzazione causata dal farmaco, ha supportato la necessità di una DAPT estesa fino al dodicesimo mese dopo la rivascolarizzazione percutanea[4]Palmerini T, Biondi-Zoccai G, Della Riva D, Stettler C, Sangiorgi D, D’Ascenzo F, Kimura T, Briguori C, Sabatè M, Kim HS, De Waha A, Kedhi E, Smits PC, Kaiser C, Sardella G, Marullo A, Kirtane AJ, … Continua a leggere. La ricerca clinica e industriale ha fortunatamente spinto un miglioramento continuo delle caratteristiche dei DES, portando all’introduzione di device caratterizzati da spessori ridotti, un migliorato profilo di rilascio del farmaco e allo sviluppo di polimeri biocompatibili e temporanei. Tali innovazioni, che si associano a una ridotta risposta infiammatoria locale e a un processo di re-endotelizzazione più efficace, hanno contribuito a una drastica riduzione dei tassi di trombosi di stent e restenosi[5]de Filippo O, Bruno F, Pinxterhuis TH, et al. ULTRA Collaborators. Predictors of target lesion failure after treatment of left main, bifurcation, or chronic total occlusion lesions with … Continua a leggere. Questo ha fatto sì che la DAPT, peraltro con inibitori del recettore piastrinico P2Y12 più potenti del capostipite clopidogrel (ticagrelor e prasugrel) abbia subito uno shift concettuale, passando dall’essere una strategia capace di prevenire eventi trombotici associati allo stent a essere considerata una terapia preventiva globale nei confronti di eventi aterotrombotici successivi alla SCA. Tuttavia, l’enorme mole di ricerca sulle modalità e durata della DAPT ha portato alla luce l’inevitabile conseguenza del potenziamento delle strategie antitrombotiche, ovvero un aumento significativo degli eventi emorragici e l’evidenza che questi ultimi hanno un impatto sulla prognosi almeno uguale agli eventi aterotrombotici[6]Valgimigli M, Costa F, Lokhnygina Y, Clare RM, Wallentin L, Moliterno DJ, et al. Trade-off of myocardial infarction vs. bleeding types on mortality after acute coronary syndrome: lessons from the … Continua a leggere. Tra le evidenze più interessanti emerse dalla letteratura sul tema, va certamente annoverata la differente distribuzione temporale del rischio emorragico e ischemico dopo la procedura di rivascolarizzazione e l’evento acuto. Se quest’ultimo, infatti, anche conseguentemente alle suddette migliorie dei device, appare concentrarsi nel primo mese dopo la rivascolarizzazione per poi diminuire progressivamente, il rischio emorragico risulta sostanzialmente stabile dal momento dell’evento indice e per tutta la durata della DAPT[7]Giustino G, Mehran R, Dangas GD, Kirtane AJ, Redfors B, Généreux P, Brener SJ, Prats J, Pocock SJ, Deliargyris EN, Stone GW. Characterization of the Average Daily Ischemic and Bleeding Risk After … Continua a leggere. In questo contesto, una strategia di “DAPT de-escalation”, ovvero il passaggio da una DAPT più intensiva a un regime meno potente dopo il primo mese dalla rivascolarizzazione, appare una scelta intuitivamente ottimale per mitigare il rischio di eventi ischemici precoci senza significativamente aumentare il rischio di sanguinamenti a lungo termine.
Lo studio
In un recente numero dell’European Heart Journal, Kang J e collaboratori hanno presentato una meta-analisi patient-level di quattro studi controllati e randomizzati, pubblicati tra il 2017 e il 2021 con la quale affrontano il tema dell’efficacia e sicurezza di una strategia di DAPT de-escalation basata sul passaggio da ASA e inibitori potenti del recettore P2Y12 (prasugrel o ticagrelor) ad ASA e clopidogrel in pazienti con SCA. Complessivamente, lo studio ha incluso 10.133 pazienti con SCA[8]Kang J, Rizas KD, Park KW, Chung J, van den Broek W, Claassens DMF, Choo EH, Aradi D, Massberg S, Hwang D, Han JK, Yang HM, Kang HJ, Chang K, Ten Berg JM, Sibbing D, Koo BK, Kim HS. Dual antiplatelet … Continua a leggere. I due endpoint principali erano rappresentati da:
- un combinato di eventi ischemici (morte cardiaca, infarto miocardico o eventi cerebrovascolari);
- eventi emorragici, entrambi analizzati fino a 1 anno dopo l’evento indice. In breve, l’incidenza dell’endpoint ischemico combinato è risultata significativamente inferiore nei pazienti assegnati alla strategia di deescalation rispetto ai pazienti assegnati alla strategia di standard DAPT (2,3% vs 3,0%; p=0,029).
Gli eventi emorragici maggiori e minori sono risultati anch’essi significativamente inferiori nei pazienti assegnati alla strategia di DAPT deescalation (6,2% vs 8,6%; p<0,001). Tuttavia, l’incidenza di sanguinamenti maggiori (1,2% vs 1,4%) e di mortalità per tutte le cause (1,0% vs 1,1%) o mortalità cardiovascolare (0,5% vs 0,7%) non è risultata significativamente diversa tra le due strategie. A un’analisi di sensibilità, la riduzione degli eventi emorragici è risultata più evidente nei pazienti assegnati a una strategia di de-escalation della DAPT non guidata da test di funzionalità piastrinica o da genotipizzazione rispetto a una strategia guidata. Sebbene lo studio riconosca il limite di una disponibilità solo parziale di dati sulla complessità procedurale delle rivascolarizzazioni eseguite e il raggruppamento di popolazioni asiatiche ed europee, caratterizzate da un trade-off tra rischio ischemico ed emorragico profondamente diverso, va riconosciuto agli Autori il merito di aver confermato la sicurezza della DAPT de-escalation in termini di rischio ischemico. L’inattesa riduzione degli eventi ischemici nel gruppo di DAPT de-escalation rappresenta forse il risultato più stimolante del lavoro di Kang. Sebbene un bias relativo alla definizione di mortalità cardiovascolare come endpoint ischemico (sebbene possa originare sia da episodi ischemici che emorragici) non può essere escluso, ulteriori meccanismi quali una migliore aderenza alla DAPT e un ridotto tasso di interruzione della duplice terapia nel gruppo di de-escalation possono essere ipotizzati alla base di questo risultato. Merita un commento anche il riscontro di una differenza non significativa nei tassi di mortalità tra i due gruppi, che emerge a scapito del noto impatto prognostico, sia degli eventi ischemici che emorragici. Questo, infatti, sembrerebbe rafforzare l’evidenza che la riduzione degli eventi emorragici nel gruppo di DAPT de-escalation sia sostanzialmente attribuibile alla riduzione di eventi emorragici minori.
Lo studio in prospettiva
Alla luce delle evidenze disponibili, appare probabile l’ipotesi che la strategia di DAPT de-escalation rappresenterà il futuro standard of care dei pazienti con SCA sottoposti a rivascolarizzazione percutanea. Anche grazie allo studio di Kang è infatti verosimile che questa strategia subisca un upgrade di raccomandazione da parte delle prossime Linee Guida europee sulla gestione dei pazienti con SCA. Va tuttavia sottolineato che il termine “de-escalation” sottenda in realtà un ventaglio di possibilità più ampio di quelle suggerite dal gruppo coreano, che limita questa strategia al passaggio da una DAPT con ASA e un inibitore potente del recettore P2Y12 alla terapia con ASA e clopidogrel. Infatti, la possibilità di “scalare” l’intensità della DAPT includerebbe per definizione anche la conversione da ASA + inibitori potenti del recettore P2Y12 a una monoterapia con ticagrelor o prasugrel. Questa ipotesi, che condivide lo stesso razionale della de-escalation come definita dagli Autori dello studio in oggetto, è stata testata in diversi trial che ne hanno confermato la sicurezza e l’efficacia in termini di riduzione degli eventi emorragici[9]Baber U, Dangas G, Angiolillo DJ, Cohen DJ, Sharma SK, Nicolas J, et al. Ticagrelor alone vs. ticagrelor plus aspirin following percutaneous coronary intervention in patients with non-ST-segment … Continua a leggere[10]Franzone A, McFadden E, Leonardi S, Piccolo R, Vranckx P, Serruys PW, et al. GLASSY Investigators. Ticagrelor Alone Versus Dual Antiplatelet Therapy From 1 Month After Drug-Eluting Coronary Stenting. … Continua a leggere. Al momento non è possibile prevedere se le prossime Linee Guida daranno delle indicazioni specifiche su come eseguire il depotenziamento della DAPT dopo i primi mesi di terapia (ovvero da ASA + ticagrelor/prasugrel ad ASA + clopidogrel o da ASA + ticagrelor/prasugrel a monoterapia con ticagrelor o prasugrel) o se indicheranno la strategia di depotenziamento come un unico grande insieme. A oggi si registra la mancanza di un confronto diretto tra le due possibilità, che sarebbe invece auspicabile. Infine, i risultati dello studio di Kang sembrano imporre l’ennesimo chiodo sulla bara della gestione della DAPT guidata da test genetici e test di aggregabilità piastrinica. L’implementazione clinica di queste strategie, già storicamente condizionata dai costi e dalle difficoltà logistiche, sembra ancora una volta allontanarsi alla luce dell’assenza di un beneficio constatato dalla prova scientifica.
Bibliografia[+]
| ↑1 | Barnathan ES, Schwartz JS, Taylor L, Laskey WK, Kleaveland JP, Kussmaul WG, Hirshfeld JW Jr. Aspirin and dipyridamole in the prevention of acute coronary thrombosis complicating coronary angioplasty. Circulation 1987;76:125-134 |
|---|---|
| ↑2 | Laudani C, Greco A, Occhipinti G, et al. Short duration of DAPT versus de-escalation after percutaneous coronary intervention for acute coronary syndromes. JACC Cardiovasc Interv 2022; 15:268–277. |
| ↑3 | Barnathan ES, Schwartz JS, Taylor L, Laskey WK, Kleaveland JP, Kussmaul WG, Hirshfeld JW Jr. Aspirin and dipyridamole in the prevention of acute coronary thrombosis complicating coronary angioplasty. Circulation 1987;76:125-134. |
| ↑4 | Palmerini T, Biondi-Zoccai G, Della Riva D, Stettler C, Sangiorgi D, D’Ascenzo F, Kimura T, Briguori C, Sabatè M, Kim HS, De Waha A, Kedhi E, Smits PC, Kaiser C, Sardella G, Marullo A, Kirtane AJ, Leon MB, Stone GW. Stent thrombosis with drug-eluting and bare-metal stents: evidence from a comprehensive network meta-analysis. Lancet 2012;379:1393-402. |
| ↑5 | de Filippo O, Bruno F, Pinxterhuis TH, et al. ULTRA Collaborators. Predictors of target lesion failure after treatment of left main, bifurcation, or chronic total occlusion lesions with ultrathin-strut drug-eluting coronary stents in the ULTRA registry. Catheter Cardiovasc Interv. 2023 May 26. doi: 10.1002/ccd.30696. Epub ahead of print. |
| ↑6 | Valgimigli M, Costa F, Lokhnygina Y, Clare RM, Wallentin L, Moliterno DJ, et al. Trade-off of myocardial infarction vs. bleeding types on mortality after acute coronary syndrome: lessons from the thrombin receptor antagonist for clinical event reduction in acute coronary syndrome (TRACER) randomized trial. Eur Heart J 2017;38:804–810. |
| ↑7 | Giustino G, Mehran R, Dangas GD, Kirtane AJ, Redfors B, Généreux P, Brener SJ, Prats J, Pocock SJ, Deliargyris EN, Stone GW. Characterization of the Average Daily Ischemic and Bleeding Risk After Primary PCI for STEMI. J Am Coll Cardiol 2017;70:1846-1857. |
| ↑8 | Kang J, Rizas KD, Park KW, Chung J, van den Broek W, Claassens DMF, Choo EH, Aradi D, Massberg S, Hwang D, Han JK, Yang HM, Kang HJ, Chang K, Ten Berg JM, Sibbing D, Koo BK, Kim HS. Dual antiplatelet therapy de-escalation in acute coronary syndrome: an individual patient meta-analysis. Eur Heart J. 2023 Apr 17;44(15):1360-1370. |
| ↑9 | Baber U, Dangas G, Angiolillo DJ, Cohen DJ, Sharma SK, Nicolas J, et al. Ticagrelor alone vs. ticagrelor plus aspirin following percutaneous coronary intervention in patients with non-ST-segment elevation acute coronary syndromes: TWILIGHT-ACS. Eur Heart J. 2020 Oct 1;41(37):3533-3545. |
| ↑10 | Franzone A, McFadden E, Leonardi S, Piccolo R, Vranckx P, Serruys PW, et al. GLASSY Investigators. Ticagrelor Alone Versus Dual Antiplatelet Therapy From 1 Month After Drug-Eluting Coronary Stenting. J Am Coll Cardiol. 2019 Nov 5;74(18):2223-2234. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.


Una risposta
PER CAMBIARE PROCEDURE TERAPEUTICHE BISOGNA ASPETTARE PIU’ FACILI TEST GENETICI E DI FUNZIONATITA’PIASTRINICA