Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Le donne sono poco rappresentate nei trial condotti in pazienti TAVI, essendo circa il 30-40% delle popolazioni arruolate[1]Mack MJ, Leon MB, Thourani VH, et al. PARTNER 3 Investigators. Transcatheter aortic-valve replacement with a balloon- expandable valve in low-risk patients. N Engl J Med. 2019;380:1695-1705. … Continua a leggere. Eppure, frequentemente presentano alcune caratteristiche anatomiche, come un anulus valvolare aortico piccolo, che possono porre una serie di problematiche di mismatch protesi-paziente. In questi casi il rischio di una emodinamica non ottimale è alto e può avere una influenza importante sull’outcome clinico dei pazienti[2]Freitas-Ferraz AB, Tirado-Conte G, Dagenais F, et al. Aortic stenosis and small aortic annulus. Circulation. 2019;139:2685- 2702. doi:10.1161/CIRCULATIONAHA.118.03840.. Recentemente, è stato presentato lo studio SMART (Small Annuli Randomized to Evolut or SAPIEN Trial) che ha mostrato migliori parametri emodinamici e una minore incidenza di disfunzione della bioprotesi a 1 anno, utilizzando protesi auto-espandibili con impianto sopravalvolare (SEV), rispetto alle protesi anulari “balloon-expandable” (BEV)[3]Herrmann HC, Mehran R, Blackman DJ, et al. Self-expanding or balloon-expandable TAVR in patients with a small aortic annulus. N Engl J Med. 2024;390:1959-1971. doi:10.1056/NEJMoa2312573.. In quel trial le donne rappresentavano l’87% dell’intera casistica: lo studio qui presentato si riferisce ai risultati ottenuti nella popolazione femminile arruolata nello SMART trial.
Lo studio in esame
Globalmente sono state incluse nel trial 621 donne (312 randomizzate a SEV e 309 a BEV) sottoposte a TAVI e con area dell’anulus ≤30 mm2 allo studio TC. L’età media era di 80.2 anni, l’STS score era 3.4%. Tra le SEV, Evolut PRO+ è stata impiantata nel 78.5% delle pazienti, mentre una SAPIEN 3 Ultra è stata usata nell’80.8% dei casi. La procedura è stata più prolungata nell’impianto di SEV per la maggior frequenza di pre-dilatazione (45.5%vs 17.5%; P<.001) e post-dilatazione (23.4% vs 13.6%, P=0.002). Anche la quantità di contrasto utilizzato è stato maggiore nell’impianto di SEV che di BEV (120.4 vs 96.0 cc, P<.001). A 12 mesi non ci sono state differenze tra i due gruppi (9.4% vs 11.8%, differenza assoluta di rischio −2.3%; 95% CI da −7.2 a 2.5, P=.35) per quanto riguarda l’endpoint primario (morte, stroke, ospedalizzazione per scompenso). L’endpoint funzionale a 12 mesi (incidenza di disfunzione protesica sia strutturale – cioè un gradiente medio ≥20 mmHg – che non-strutturale – cioè un severo mismatch protesi-paziente, rigurgito aortico almeno moderato, trombosi della valvola, endocardite, reintervento) è risultato più elevato nel gruppo BEV che nei pazienti SEV (41.8% vs 8.4%, differenza assoluta di rischio −33.4%; 95% CI, da −40.4 a −26.4; P<.001), così come il mismatch protesi-paziente, vedi Tabella. A 12 mesi non vi era differenza nella distribuzione della classe NYHA tra i due gruppi, mentre il KCCQ (Kansas City Cardiomyopathy Questionnaire) mostrava una migliore qualità di vita nei pazienti sottoposti a impianto di SEV.
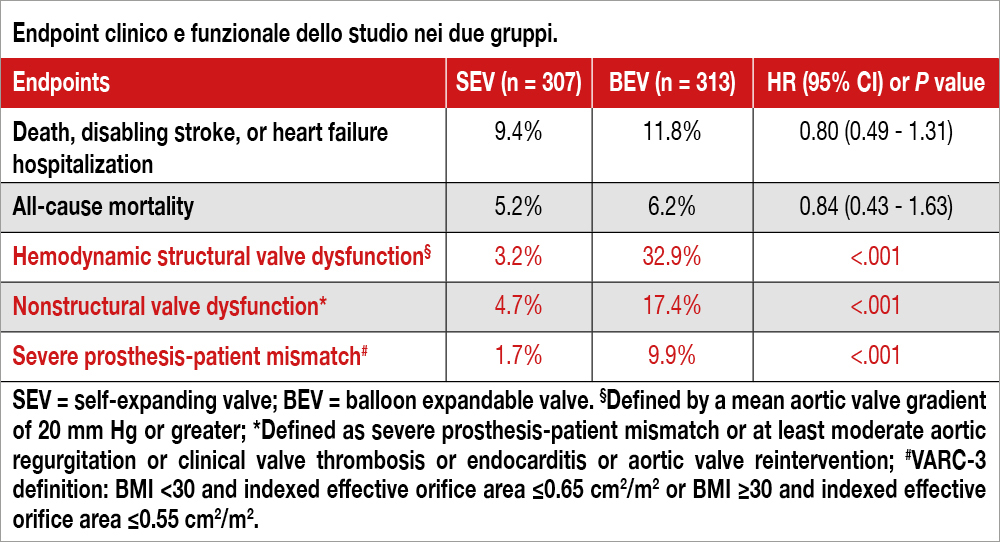
Take home message
Nelle donne con anulus piccolo sottoposte a TAVI per stenosi aortica severa, l’outcome clinico a 1 anno non sembra dipendere dal tipo di protesi impiantata. Tuttavia, l’utilizzo di una protesi “balloon expandable” comporta una maggiore probabilità di disfunzione protesica sia strutturale che non strutturale.
Interpretazione dei dati
Un anulus piccolo è una caratteristica della popolazione femminile sottoposta a TAVI. La sua presenza dà spesso origine al “mismatch protesi-paziente (PPM)”, una condizione in cui l’area effettiva di una valvola protesica impiantata è relativamente piccola rispetto alla superficie corporea del paziente trattato. Ne consegue una emodinamica alterata con gradienti elevati e un outcome a distanza sfavorevole. In 62.125 pazienti sottoposti a TAVI negli Stati Uniti tra il 2014 e il 2017 e che sono stati inclusi nel registro della Society of Thoracic Surgeons/American College of Cardiology/Transcatheter Valve Therapy Registry, era presente un PPM severo nel 12% dei pazienti che presentavano, nel follow-up, una più alta mortalità e un rischio maggiore di scompenso rispetto a pazienti con adeguata area valvolare[4]Herrmann HC, Daneshvar SA, Fonarow GC, et al. Prosthesis–patient mismatch in patients undergoing transcatheter aortic valve replacement: from the STS/ACC TVT Registry. J Am Coll Cardiol. … Continua a leggere. Una metanalisi di 23 studi in oltre 80.000 pazienti TAVI ha mostrato un significativo aumento della mortalità a 5 anni nei pazienti con PPM severo[5]Sá MP, Jacquemyn X, Van den Eynde J, et al. Impact of prosthesis-patient mismatch after transcatheter aortic valve replacement: meta-analysis of Kaplan-Meier–derived individual patient data. JACC … Continua a leggere. È noto che la tipologia di bioprotesi impiantata ha un ruolo importante nel determinare una inadeguatezza dell’area valvolare: è stato infatti osservato che l’impianto intra-anulare utilizzando una protesi “balloon- expandable” comporta una emodinamica meno favorevole, soprattutto in presenza di un anulus piccolo, rispetto all’impianto sopravalvolare di una protesi “self-expanding”, ma non era stato ancora eseguito uno studio di confronto randomizzato dotato di numerosità e potenza adeguate. Lo studio ha quindi il merito di aver affrontato una problematica che ha riflessi importanti nella pratica quotidiana nei centri cui affluiscono i pazienti da trattare con TAVI. Il limite principale riguarda il fatto che i dati, ovviamente, non si discostano da quelli dello studio globale[6]Herrmann HC, Mehran R, Blackman DJ, et al. Self-expanding or balloon-expandable TAVR in patients with a small aortic annulus. N Engl J Med. 2024;390:1959-1971. doi:10.1056/NEJMoa2312573., visto che le donne rappresentavano la larga maggioranza dei pazienti arruolati.
Editoriale: “Quale protesi valvolare aortica impiantare nella popolazione femminile con stenosi aortica severa e anulus piccolo: verso una tavi sempre più smart”
A cura di: Francesco Cardaioli, Chiara Fraccaro – Interventional Cardiology Unit, Department of Cardiac,Thoracic, Vascular Sciences and Public Health, University of Padua Medical School, Padova.
Negli ultimi due decenni, l’introduzione nella pratica clinica dell’intervento di sostituzione transcatetere della valvola aortica (TAVI) ha rivoluzionato il trattamento della stenosi aortica severa sintomatica, offrendo una valida alternativa alla chirurgia tradizionale soprattutto nei pazienti anziani e ad alto rischio operatorio(1-3). Tuttavia, nonostante questi importanti progressi tecnologici, la gestione di questa patologia presenta ancora importanti discrepanze di genere, a partire dalla sua diagnosi fino al trattamento(4-6). Infatti, la popolazione femminile affetta da stenosi aortica severa presenta spesso caratteristiche anatomiche peculiari (anelli aortici più piccoli e una predominanza di fibrosi rispetto alla calcificazione), riceve sovente una diagnosi più tardiva, ed è classicamente meno rappresentata nei più importanti trial clinici(2,3,6). Inoltre, classicamente, la popolazione femminile affetta da stenosi valvolare aortica sottoposta a correzione è gravata da una più alta incidenza di specifici pattern emodinamici post-procedurali, come il mismatch protesi-paziente (PPM), specialmente quando trattata per via chirurgica(7-9). In questo contesto, è stata recentemente pubblicata una sotto-analisi pre-specificata dello studio SMART (Small Annuli Randomized to Evolut or SAPIEN Trial), riguardante, nello specifico, i risultati ottenuti nella compagine femminile del trial(10). Questo nuovo tassello rappresenta un importante contributo scientifico, utile ad ampliare la mole di dati disponibili e a dettagliare più approfonditamente gli outcome della procedura di TAVI nei soggetti di genere femminile. Lo studio principale, pubblicato ad Aprile 2024 nel New England Journal of Medicine, è stato uno studio randomizzato multicentrico, condotto tra aprile 2021 e ottobre 2022, che ha incluso 716 pazienti affetti da stenosi aortica severa e caratterizzati da anatomie aortiche native di piccole dimensioni (area anulare minore o uguale a 430 mm2)(11). Lo studio si è proposto di confrontare l’uso di valvole auto-espandibili (SEV, Medtronic Evolut PRO, PRO+ o FX) o di valvole espandibili con pallone (BEV, Edwards Life Sciences SAPIEN 3 o Ultra) valutando a 12 mesi dalla procedura un endpoint composito clinico (mortalità per tutte le cause, stroke e re-ospedalizzazioni per scompenso cardiaco) e un endpoint emodinamico (presenza di disfunzione di bioprotesi, BVD). Prendendo in considerazione le 621 pazienti di sesso femminile incluse nella sotto-analisi, a 12 mesi non sono state osservate differenze significative nell’endpoint primario clinico (9.4% per SEV contro 11.8% per BEV, P=0.35). Tuttavia, il gruppo di pazienti trattate con SEV ha dimostrato una chiara superiorità emodinamica rispetto al gruppo BEV, con un’incidenza significativamente inferiore di BVD (8.4% vs 41.8%, P<0.001) e di PPM moderato o severo (11.2% vs 37.4%, P<0.001). Inoltre, l’utilizzo di SEV è stato associato a gradienti transvalvolari post-procedurali minori, ad aree valvolari effettive (EOA) più ampie e a una migliore qualità di vita (valutata attraverso il Kansas City Cardiomyopathy Questionnaire) a scapito di un maggiore utilizzo di contrasto intra-procedurale e una più alta necessità di pacing permanente (11.8% vs 7.6%, P=0.07). I risultati riportati ricalcano fedelmente quelli già precedentemente dimostrati dallo studio principale(11). A tal proposito, questa somiglianza non è sorprendente, considerando l’elevata percentuale di pazienti di sesso femminile arruolata nello SMART trial e quindi successivamente inclusa nella sotto-analisi (85%, 621 pazienti su 716 totali). Questo dato fa chiaramente emergere l’alta prevalenza di soggetti di sesso femminile tra i pazienti affetti da stenosi aortica severa e caratterizzati da anatomie di piccole dimensioni, sottendendo quindi la peculiarità di questa specifica popolazione, che deve ovviamente essere tenuta in considerazione in tutte le fasi del trattamento(6,8). Infatti, come analizzato elegantemente da Van Mieghem e colleghi(12), la popolazione femminile sottoposta a TAVI differisce significativamente da quella maschile sia in termini di caratteristiche baseline (ridotte comorbilità e tassi inferiori di precedenti cardiovascolari) che di outcome peri-procedurali (maggior rischio di sanguinamenti, complicanze vascolari e tamponamento cardiaco). Questi fattori devono ovviamente essere tenuti in considerazione nelle fasi di planning pre-procedurale e durante la procedura. A tal proposito, i risultati favorevoli riportati dalla sotto-analisi dello studio SMART riguardo l’utilizzo della TAVI in questo specifico sottogruppo di pazienti, sia in termini di efficacia che di sicurezza, sono rassicuranti e confermano quelli già precedentemente pubblicati in altri studi sempre focalizzati sulla popolazione femminile (registro WIN-TAVI e sotto-analisi del SURTAVI trial(7,8,12), dimostrando, inoltre, una sostanziale parità in termini di outcome clinici tra le due tipologie di device, principali global leader nel settore. Tuttavia, l’apparente peggior performance emodinamica delle BEV necessita ovviamente di particolare attenzione e riflessione, specialmente considerando il più alto tasso di BVD riscontrato, che potrebbe esporre queste pazienti a un aumentato rischio di eventi avversi o di necessità di nuovi interventi correttivi (particolarmente rischiosi in anatomie native di piccolo calibro). Analizzando criticamente i dati pubblicati, vanno però notati alcuni aspetti, che potrebbero aver potenzialmente influito sui risultati ottenuti. Primo fra tutti, una certa discrepanza in termini di taglie dei dispositivi utilizzati nei due bracci, a dispetto di valori medi di aree anulari native comparabili. Infatti, nel gruppo di pazienti trattate con SEV, più di una su quattro (26% del totale) è stata trattata con un device di taglia 29 mm, mentre solo l’1.8% delle pazienti trattate con BEV ha ricevuto la corrispondente protesi di taglia 26 mm (che, teoricamente, nel processo di planning pre-procedurale è sovrapponibile in termini di dimensioni all’anulus nativo(13)). Questo dato potrebbe ovviamente aver influito notevolmente sugli outcome emodinamici riscontrati al follow-up, e andrebbe inquadrato avendo a disposizione un più accurato dettaglio delle anatomie native delle pazienti arruolate, non disponibile al momento fra i dati consultabili. Un secondo importante aspetto da considerare è la possibile discrepanza tra i valori emodinamici riscontrati ecograficamente e i valori reali, potenzialmente misurabili invasivamente. È noto infatti come possa esistere una certa differenza, anche significativa, tra i valori di gradiente trans-valvolare ecografico vs invasivo, specialmente nelle aorte di piccole dimensioni (prevalentemente per fenomeni di pressure recovery (14,15)) e nei pazienti sottoposti a impianto di BEV (probabilmente per la presenza di flusso turbolento dovuto allo specifico design del frame valvolare(16)). Pertanto, prima di ricavare conclusioni definitive a riguardo, sarebbe opportuno poter confermare i dati qui ottenuti anche misurando invasivamente i gradienti transvalvolari post-procedurali, così da evitare errori di misura e sovra o sotto-stime dei valori. L’ultimo aspetto da considerare è l’effettivo impatto clinico dei risultati emodinamici qui riscontrati. Sebbene sia noto come, nei pazienti sottoposti a sostituzione valvolare aortica per via chirurgica (SAVR), la presenza di PPM moderato-severo post-procedurale sia significativamente associata a un aumentato rischio di eventi clinici avversi al follow-up(17), questo dato non è ancora stato chiaramente confermato nei pazienti sottoposti a procedura di TAVI(18–20). Infatti, come dimostrato da una recente analisi pubblicata sul JACC: Cardiovascular Interventions(20), la presenza di PPM post-TAVI (a prescindere dalla severità) non sembra essere clinicamente impattante a distanza di due anni dalla procedura. Inoltre, la stessa analisi ha sottolineato come un differente approccio diagnostico possa ridurre significativamente la quota di pazienti catalogati con PPM rilevante, ponendo quindi un giustificato riserbo riguardo la più corretta definizione di questa particolare condizione e il suo effettivo impatto clinico. Al momento attuale, pertanto, risulta difficile esporsi sulla scelta di uno specifico dispositivo sulla base dei dati emodinamici fin qui riscontrati, almeno fino a quando non vi sarà una chiara correlazione tra quanto dimostrato ecograficamente e gli outcome clinici di queste pazienti. In conclusione, sebbene sia ancora presto per trarre conclusioni definitive, i dati pubblicati confermano l’ottima performance della procedura di TAVI condotta con dispositivi di ultima generazione anche in pazienti di genere femminile e con anatomie aortiche più piccole, rafforzando l’importanza di una valutazione pre-procedurale multidisciplinare e caso per caso. Sarà ovviamente da valutare l’impatto clinico delle differenze fin qui rilevate in termini di performance emodinamica, anche nel follow- up a lungo termine. Tuttavia, in un contesto storico di disparità di genere nella ricerca cardiovascolare, lo SMART Trial rappresenta un passo avanti verso una medicina più inclusiva e personalizzata, ponendo le basi per ulteriori progressi nella gestione di questa complessa patologia.
Bibliografia[+]
| ↑1 | Mack MJ, Leon MB, Thourani VH, et al. PARTNER 3 Investigators. Transcatheter aortic-valve replacement with a balloon- expandable valve in low-risk patients. N Engl J Med. 2019;380:1695-1705. doi:10.1056/NEJMoa1814052. |
|---|---|
| ↑2 | Freitas-Ferraz AB, Tirado-Conte G, Dagenais F, et al. Aortic stenosis and small aortic annulus. Circulation. 2019;139:2685- 2702. doi:10.1161/CIRCULATIONAHA.118.03840. |
| ↑3, ↑6 | Herrmann HC, Mehran R, Blackman DJ, et al. Self-expanding or balloon-expandable TAVR in patients with a small aortic annulus. N Engl J Med. 2024;390:1959-1971. doi:10.1056/NEJMoa2312573. |
| ↑4 | Herrmann HC, Daneshvar SA, Fonarow GC, et al. Prosthesis–patient mismatch in patients undergoing transcatheter aortic valve replacement: from the STS/ACC TVT Registry. J Am Coll Cardiol. 2018;72:2701-2711. doi:10.1016/j. jacc.2018.09.001. |
| ↑5 | Sá MP, Jacquemyn X, Van den Eynde J, et al. Impact of prosthesis-patient mismatch after transcatheter aortic valve replacement: meta-analysis of Kaplan-Meier–derived individual patient data. JACC Cardiovasc Imaging. 2023;16:298- 310. doi:10.1016/j.jcmg.2022.07.013. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

