Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Il trattamento delle stenosi coronariche calcifiche rappresenta una sfida per il cardiologo interventista, sia per la difficoltà di esecuzione della PCI che per le complicanze procedurali e a distanza[1]Généreux P, Madhavan MV, Mintz GS, et al. Ischemic outcomes after coronary intervention of calcified vessels in acute coronary syndromes. Pooled analysis from the HORIZONS-AMI (Harmonizing Outcomes … Continua a leggere. Il recente documento di consenso dell’European Association of Percutaneous Cardiovascular Interventions (EAPCI) sottolinea la necessità di preparare adeguatamente le stenosi (rotablator, litotripsia intravascolare) e di utilizzare tecniche di imaging per guidare le strategie di PCI[2]Barbato E, Gallinoro E, Abdel-Wahab M, et al. Management strategies for heavily calcified coronary stenoses: an EAPCI clinical consensus statement in collaboration with the EURO4C-PCR group. Eur … Continua a leggere. L’OCT ben si presta a tale scopo, per la sua eccellente risoluzione spaziale, la capacità di misurare accuratamente la minimal stent area (MSA), correlata ai successivi eventi ischemici. Tuttavia, non ci sono studi di confronto tra OCT e guida angiografica in questo ambito.
Lo studio in esame
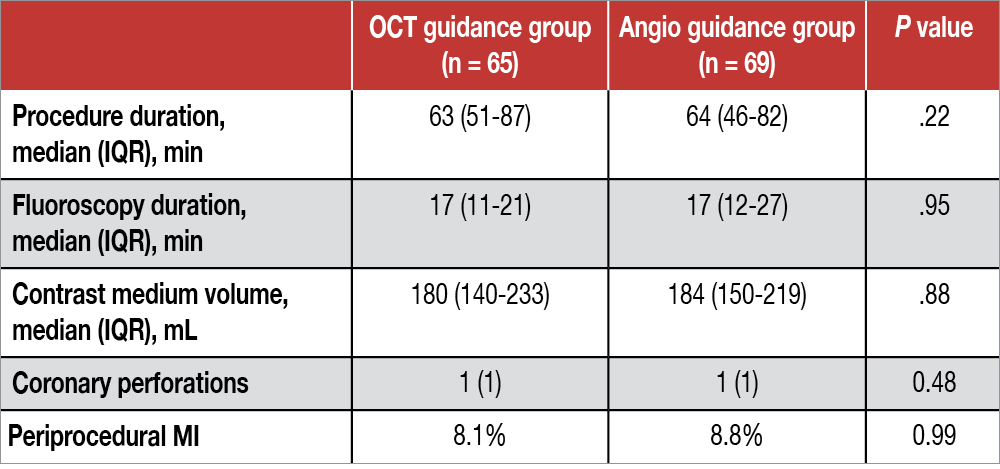
Lo studio CALIPSO (Calcified Lesion Intervention Planning Steered by OCT) è uno studio prospettico, multicentrico, randomizzato, condotto in 12 centri francesi, che ha paragonato OCT versus angiografia come guida alle procedure di PCI delle lesioni calcifiche di 134 pazienti stabili. Erano incluse le stenosi moderatamente/severamente calcifiche (secondo la classificazione di Mintz)[3]Mintz GS, Popma JJ, Pichard AD, et al. Patterns of calcification in coronary artery disease: a statistical analysis of intravascular ultrasound and coronary angiography in 1155 lesions. … Continua a leggere che potessero essere indagate con catetere OCT. Lo studio era basato su una ipotesi di superiorità di OCT (MSA inferiore del 20% nei pazienti del gruppo OCT versus gruppo angio) per la cui dimostrazione sarebbero stati necessari 63 pazienti per gruppo. Anche in quelli del gruppo angio era previsto un “run” di OCT al termine della procedura di PCI con eventuale ottimizzazione dell’impianto di stent (step obbligato per disposizione del Comitato Etico), ma il valore di MSA considerato per lo studio di confronto era comunque quello precedente alla eventuale ottimizzazione suggerita dall’OCT. Un’altra differenza procedurale tra i due gruppi consisteva nella preparazione della lesione che era lasciata a discrezione dell’operatore nel gruppo angio mentre seguiva un protocollo preciso suggerito dall’OCT (uso di litotripsia o rotablator in base all’ampiezza della calcificazione) nel gruppo OCT. Ne è conseguito un più frequente uso di rotablator nel gruppo angio (26% versus 19%, P non signifcativa) e un utilizzo maggiore di litotripsia nel gruppo OCT (46% versus 12%, P<.001). L’endpoint primario (ampiezza MSA) è risultato maggiore nel gruppo OCT (6.5 [5.5-8.1] mm2 vs 5.0 [4.1-6.1] mm2; P<.001). Non è stata individuata alcuna differenza tra i due gruppi per quanto riguarda i dati e le complicanze procedurali (vedi Tabella).
Take home message
Una strategia OCT-guidata delle PCI eseguite su lesioni calcifiche ha prodotto una maggiore espansione dello stent rispetto alla sola guida angiografica. Sarà da verificare se questo dato si tradurrà in un outcome clinico migliore.
Interpretazione dei dati
Lo studio ha il merito di mostrare gli effetti di una guida OCT nelle procedure di PCI di lesioni calcifiche, un argomento per il quale i dati della letteratura sono modesti. La scarsa numerosità della casistica e il follow-up molto breve non permettono di trasporre il dato ottenuto (maggiore espansione dello stent con OCT rispetto alla sola angiografia) in equivalenti clinici. Tuttavia, l’ampia differenza in termini di area luminale minima al termine della procedura tra le due strategie di guida della PCI fa presagire un migliore outcome per i pazienti assegnati alla guida OCT rispetto a quelli randomizzati all’utilizzo dei soli dati angiografici. Infatti in quest’ultimo gruppo, un’area luminale minima finale >4.5 mm2, raccomandata dai documenti di consenso[4]Räber L, Mintz GS, Koskinas KC, et al. ESC Scientific Document Group. Clinical use of intracoronary imaging. part 1: guidance and optimization of coronary interventions. an expert consensus document … Continua a leggere, non è stata raggiunta in una discreta percentuale di pazienti (essendo il valore mediano 5 mm2 e il valore del 25% percentile 4.1 mm2). La maggiore perplessità riguardo allo studio (e che ne inficia notevolmente il valore) concerne il diverso pre-trattamento delle stenosi, caratterizzato da un ampio utilizzo della litotripsia nel gruppo OCT (46%), rispetto a un limitato uso nel gruppo “angio” (12%). A fronte di questa ampia differenza, statisticamente significativa, vi era invece un maggior utilizzo del rotablator nei pazienti randomizzati alla guida angiografica (26% versus 19%). Globalmente, quindi, sono state attuate tecniche ablative (raccomandate dai documenti di consenso) nel 65% dei pazienti assegnati alla strategia OCT e nel 38% dei pazienti assegnati alla strategia angiografica. Gli autori sostengono che il pretrattamento delle stenosi con tali dispositivi era suggerito proprio dall’analisi OCT basale e dalla ampiezza dell’arco calcifico, mentre nel gruppo a guida angiografica l’utilizzo di rotablator, litotripsia o pallone non compliante era lasciata alla discrezione degli operatori. Inoltre, l’analisi multivariata mostrerebbe l’assenza di un ruolo significativo dell’utilizzo della litotripsia nell’ottenimento di una adeguata espansione dello stent; osservazioni che non dissipano, tuttavia i dubbi che il risultato dello studio sia stato influenzato da un ingiustificato differente pre-trattamento delle stenosi nei due gruppi.
Bibliografia[+]
| ↑1 | Généreux P, Madhavan MV, Mintz GS, et al. Ischemic outcomes after coronary intervention of calcified vessels in acute coronary syndromes. Pooled analysis from the HORIZONS-AMI (Harmonizing Outcomes With Revascularization and Stents in Acute Myocardial Infarction) and ACUITY (Acute Catheterization and Urgent Intervention Triage Strategy) trials. J Am Coll Cardiol.2014;63:1845-1854. doi:10.1016/j.jacc.2014.01.034; Bourantas CV, Zhang YJ, Garg S, et al. Prognostic implications of coronary calcification in patients with obstructive coronary artery disease treated by percutaneous coronary intervention: a patient-level pooled analysis of 7 contemporary stent trials. Heart 2014;100:1158-1164. doi:10.1136/heartjnl-2013-305180. |
|---|---|
| ↑2 | Barbato E, Gallinoro E, Abdel-Wahab M, et al. Management strategies for heavily calcified coronary stenoses: an EAPCI clinical consensus statement in collaboration with the EURO4C-PCR group. Eur Heart J. 2023;44:4340-4356. doi:10.1093/ eurheartj/ehad342. |
| ↑3 | Mintz GS, Popma JJ, Pichard AD, et al. Patterns of calcification in coronary artery disease: a statistical analysis of intravascular ultrasound and coronary angiography in 1155 lesions. Circulation.1995;91:1959-1965. doi:10.1161/01.CIR.91.7.1959 |
| ↑4 | Räber L, Mintz GS, Koskinas KC, et al. ESC Scientific Document Group. Clinical use of intracoronary imaging. part 1: guidance and optimization of coronary interventions. an expert consensus document of the European Association of Percutaneous Cardiovascular Interventions. Eur Heart J. 2018;39(35):3281-3300. doi:10.1093/eurheartj/ehy285. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

