Le linee guida raccomandano di proseguire con la terapia anticoagulante per prevenire gli eventi tromboembolici nei pazienti con fibrillazione atriale anche dopo un intervento di ablazione efficace[1]Tzeis S, Gerstenfeld EP, Kalman J, et al. 2024 European Heart Rhythm Association/ Heart Rhythm Society/Asia Pacific Heart Rhythm Society/Latin American Heart Rhythm Society expert consensus statemen … Continua a leggere. Lo studio ALONE AF, presentato al congresso ESC 2025[2]Kim D, Shim J, Choi E-K, et al. Longterm anticoagulation discontinuation after catheter ablation for atrial fibrillation: the ALONE-AF randomized clinical trial. JAMA 2025;334:1246-54, ha iniziato a scalfire questo dogma. Tuttavia, sono necessarie ulteriori evidenze in proposito.
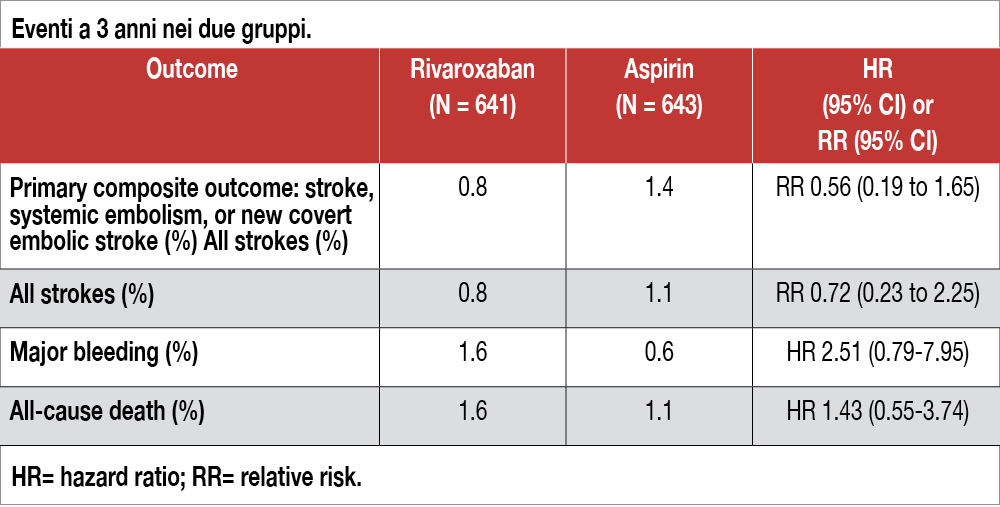
Lo studio è stato intrapreso dall’Ottawa Heart Institute in collaborazione con 56 centri di 6 Paesi in 1.284 pazienti sottoposti con successo, almeno 1 anno prima, ad ablazione della fibrillazione atriale (AF). L’età media era 66 anni, più di 1 ablazione era stata eseguita nel 25% dei casi e AF era parossistica in due terzi dei pazienti. Il CHA2DS2VASc score medio era 2.2±1.1, con valori ≥3 nel 32% dei casi. Tutti i pazienti hanno effettuato una indagine di risonanza magnetica (MRI) cerebrale in basale e a 3 anni per individuare stroke embolici silenti (con dimensione di ≥15 mm alla MRI). I criteri di esclusione erano rappresentati da età >85 anni e clearance della creatinina <30 ml/ min, così come erano esclusi i pazienti portatori di valvola meccanica. I pazienti sono stati randomizzati in due gruppi: 641 hanno assunto rivaroxaban 15 mg, mentre 643 hanno assunto ASA (dosaggio variabile tra 80 e 120 mg). Lo studio aveva un disegno di superiorità per rivaroxaban (40% di riduzione dell’endpoint primario, ipotizzando una incidenza annuale nel gruppo ASA di 3.5% di stroke, sia manifesto che silente). L’endpoint primario di efficacia (stroke ischemico incluso quello silente ed embolismo arterioso) è stato raggiunto nello 0.31% per anno nel gruppo rivaroxaban e nello 0.66% per anno nel gruppo ASA (rischio relativo 0.56; 95% CI, 0.19-1.65; P= 0.28). Si sono verificati nuovi infarti cerebrali di ampiezza < 15 mm nel 3.9% del gruppo rivaroxaban e nel 4.4% del gruppo ASA (rischio relativo, 0.89; 95% CI, 0.51-1.55). L’endpoint primario di sicurezza (bleeding fatale e maggiore, secondo definizione ISTH) si è verificato nell’1.6% con rivaroxaban e nello 0.6% con ASA a 3 anni (hazard ratio, 2.51; 95% CI, 0.79 -7.95). Il bleeding minore è risultato invece significativamente più elevato nel gruppo rivaroxaban (HR 3.71,95% CI 2.29–6.01).
Take home message
Nei pazienti sottoposti ad ablazione efficace per fibrillazione atriale, un trattamento con rivaroxaban non ha ridotto significativamente lo stroke (anche silente) rispetto all’ASA. Anche il bleeding maggiore o fatale è apparso non differente tra i due gruppi.
Interpretazione dei dati
Il dato più rilevante (e inatteso) dello studio risiede nella bassa incidenza di eventi tromboembolici e stroke registrati nella popolazione studiata. Infatti, il composito annualizzato di stroke (incluso quello silente) ed embolismo sistemico è stato pari a 0.31 eventi per 100 pazienti/anno nel gruppo rivaroxaban e pari a 0.66 nel gruppo ASA. Invece, le incidenze osservate in una popolazione analoga (per valori di CHA2DS2-VASc) a quella arruolata nell’OCEAN, ma non sottoposta ad ablazione, risultano superiori (1.6% per la terapia anticoagulante e 3.7% per l’ASA)[3]Connolly SJ, Eikelboom J, Joyner C, et al. Apixaban in patients with atrial fibrillation.N Engl J Med 2011; 364: 806-17.. Gli eventi nel trial sono risultati inferiori anche a quelli rilevati nella fibrillazione atriale subclinica (0.85% con terapia anticoagulante, 0.97% per l’ASA)[4]Lopes RD, Granger CB, Wojdyla DM, et al. Apixaban vs aspirin according to CHA2DS2-VASc score in subclinical atrial fibrillation: insights from ARTESiA. J Am Coll Cardiol 2024;84: 354-64. e simili a quelli riscontrati in pazienti con analogo CHA2DS2-VASc score ma senza storia di fibrillazione atriale[5]Kaplan RM, Koehler J, Ziegler PD, Sarkar S, Zweibel S, Passman RS. Stroke risk as a function of atrial fibrillation duration and CHA2DS2-VASc score. Circulation 2019;140:1639-46.. Secondo gli autori questi dati possono essere dovuti al fatto che l’ablazione riduce il burden della fibrillazione atriale e di conseguenza il rischio associato di stroke. È anche possibile che la causa risieda in un “bias di selezione”, in quanto la popolazione studiata era caratterizzata da una bassa prevalenza di stroke in anamnesi. In ogni caso, viste le percentuali riscontrate nei due gruppi, lo studio avrebbe dovuto avere una popolazione di circa 11.000 pazienti per dimostrare la superiorità di rivaroxaban su ASA. Lo studio OCEAN conferma e rafforza i dati dello studio ALONE AF(2), avendo studiato una popolazione più ampia, seguita per un follow-up più lungo (3 anni) e che includeva gli ictus clinicamente silenti grazie all’esecuzione di MRI sistematica. Nei pazienti sottoposti ad ablazione efficace della fibrillazione atriale sono quindi possibili quattro tipi diversi di terapia: anticoagulante, antiaggregante (ASA), nessun farmaco o l’impianto di un dispositivo di occlusione dell’auricola (testato con successo nello studio OPTION che peraltro includeva pazienti a rischio tromboembolico maggiore, essendo il CHA2DS2-VASc score mediano =>3)[6]Wazni OM, Saliba WI, Nair DG, et al. Left atrial appendage closure after ablation for atrial fibrillation. N Engl J Med 2025; 392:1277-87. Nei vari trial l’incidenza annuale di stroke ed embolismo sistemico è stata <1%, attualmente considerata la soglia per intraprendere una terapia anticoagulante[7]Tzeis S, Gerstenfeld EP, Kalman J, et al. 2024 European Heart Rhythm Association/ Heart Rhythm Society/Asia Pacific Heart Rhythm Society/Latin American Heart Rhythm Society expert consensus statemen … Continua a leggere.
Bibliografia[+]
| ↑1, ↑7 | Tzeis S, Gerstenfeld EP, Kalman J, et al. 2024 European Heart Rhythm Association/ Heart Rhythm Society/Asia Pacific Heart Rhythm Society/Latin American Heart Rhythm Society expert consensus statemen on catheter and surgical ablation o atrial fibrillation. Europace 2024;26:euae043 |
|---|---|
| ↑2 | Kim D, Shim J, Choi E-K, et al. Longterm anticoagulation discontinuation after catheter ablation for atrial fibrillation: the ALONE-AF randomized clinical trial. JAMA 2025;334:1246-54 |
| ↑3 | Connolly SJ, Eikelboom J, Joyner C, et al. Apixaban in patients with atrial fibrillation.N Engl J Med 2011; 364: 806-17. |
| ↑4 | Lopes RD, Granger CB, Wojdyla DM, et al. Apixaban vs aspirin according to CHA2DS2-VASc score in subclinical atrial fibrillation: insights from ARTESiA. J Am Coll Cardiol 2024;84: 354-64. |
| ↑5 | Kaplan RM, Koehler J, Ziegler PD, Sarkar S, Zweibel S, Passman RS. Stroke risk as a function of atrial fibrillation duration and CHA2DS2-VASc score. Circulation 2019;140:1639-46. |
| ↑6 | Wazni OM, Saliba WI, Nair DG, et al. Left atrial appendage closure after ablation for atrial fibrillation. N Engl J Med 2025; 392:1277-87 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

