Inquadramento
Il prolasso della valvola mitrale (MVP), la più frequente patologia valvolare nei Paesi occidentali, è generalmente a prognosi benigna, ma può complicarsi con una progressiva insufficienza valvolare[1]Delling FN, Rong J, Larson MG, et al. Evolution of mitral valve prolapse: insights from the Framingham Heart Study Circulation 2016;133: 1688–95. https://doi.org/10.1161/CIRCULATIONAHA.115.020621. Vi è poi un sottogruppo di pazienti che sviluppano aritmie ventricolari minacciose[2]Basso C, Perazzolo Marra M, Rizzo S, et al. Arrhythmic mitral valve prolapse and sudden cardiac death. Circulation 2015;132: 556–66. https://doi.org/10.1161/CIRCULATIONAHA.115.016291. Questi pazienti possono presentare alcune caratteristiche distintive, quali una disgiunzione anulo-mitralica (distacco dell’anulus dalla giunzione atrioventricolare postero-laterale), prolasso di entrambi i lembi, extrasistolia ventricolare frequente, inversione delle onde T ed un “late-gadolinium enhancement” della parete infero-laterale o dei muscoli papillari all’indagine MRI. Non è chiaro se questi pazienti presentino un rischio aritmico elevato anche dopo un intervento di chirurgia valvolare riparativa o sostitutiva. Infatti tale rischio potrebbe persistere soprattutto in presenza di una disgiunzione mitro-anulare, in quanto l’eccessiva mobilità dell’anulus e la trazione esercitata in sistole possono determinare con il passare del tempo una fibrosi dei muscoli papillari che sarebbe permanente e quindi costituire un substrato aritmogeno anche dopo un intervento chirurgico apparentemente efficace[3]Han Y, Peters DC, Salton CJ, Bzymek D, Nezafat R, Goddu B, et al. Cardiovascular magnetic resonance characterization of mitral valve prolapse. JACC Cardiovasc Imaging 2008; 1:294–303. … Continua a leggere.
Lo studio in esame
La casistica è composta da 599 pazienti con MVP moderato o severo operati tra il 2010 ed il 2022 al Karolinska University Hospital di Stoccolma di sostituzione o riparazione valvolare mitralica. Venivano esclusi i pazienti con cardiopatia ischemica associata, precedente intervento chirurgico, endocardite, cardiomiopatia primitiva. Una disgiunzione anulo-mitralica (MAD), misurata in telesistole all’ecocardiogramma transtoracico (definita come la distanza tra il punto di inserzione del foglietto posteriore mitralico e la giunzione atrio-ventricolare sinistra) era presente in 96 (16%) pazienti e la sua lunghezza mediana di 8 mm. I pazienti con MAD erano più giovani (55 ± 15 vs 63 ± 11 anni), maggiormente di sesso femminile (31% vs 17%), e avevano più frequentemente una malattia di Barlow (70% vs 27%). Avevano anche una classe funzionale NYHA più bassa. Dei 599 pazienti, 485 (81%) sono stati sottoposti a riparazione valvolare mitralica, mentre 114 (19%) a sostituzione valvolare, con percentuali non dissimili tra pazienti con MAD e quelli non- MAD. L’outcome primario era rappresentato da aritmie ventricolari (TV sostenute e non sostenute o burden aritmico >5%, presenti durante l’ospedalizzazione, ai controlli successivi o che abbiano richiesto ablazione) ad un follow-up mediano di 5.4 (IQR 2.8–7.5) anni.
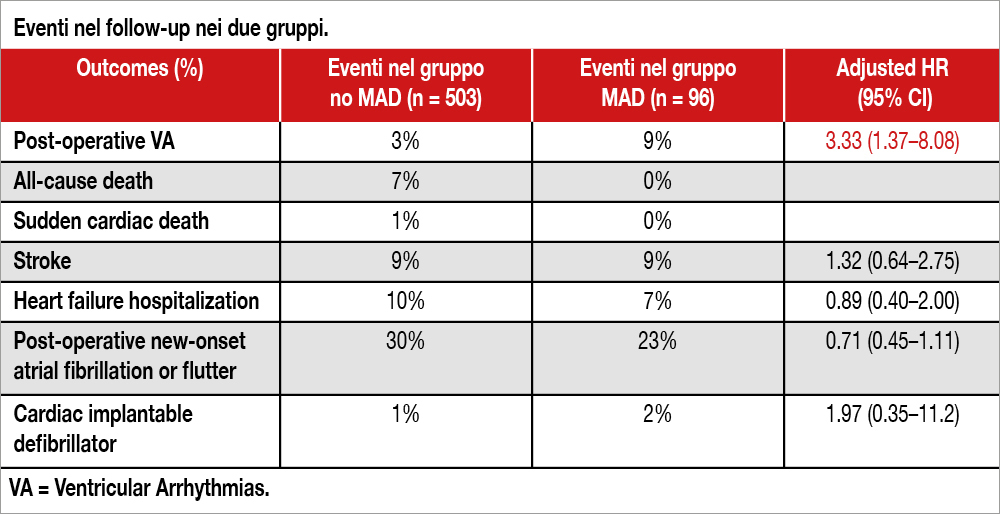
I pazienti con MAD pre-operatorio avevano un rischio più elevato di aritmie ventricolari (9% vs 3%,hazard ratio aggiustato per età e sesso: 3.33, 95% CI 1.37–8.08) indipendentemente dal tipo di intervento subito. Più ampio il MAD, maggiore il rischio aritmico (per ogni mm di maggior ampiezza di MAD il rischio aritmico cresceva del 35%). I dati erano confermati utilizzando, per l’aggiustamento delle variabili diversamente distribuite tra i due gruppi, la tecnica dell’inverse probability treatment weigthing. A fronte di questa maggiore suscettibilità aritmica nei pazienti MAD, non vi era alcuna differenza tra i due gruppi per quanto riguardava la mortalità (inclusa la morte improvvisa), le ospedalizzazioni per scompenso, l’impianto di defibrillatore (vedi Tabella).
Take home message
I pazienti con prolasso valvolare mitralico che presentino all’ecocardiogramma una disgiunzione mitro-anulare, una volta operati di riparazione o sostituzione valvolare, mostrano un rischio di aritmie ventricolari tre volte superiore rispetto ai pazienti senza disgiunzione mitro-anulare.
Interpretazione dei dati
Gli autori sottolineano i tre messaggi principali dello studio:
- I pazienti con prolasso mitralico e disgiunzione mitro-anulare sottoposti a chirurgia valvolare sono più giovani (di circa 8 anni) e hanno un rischio di aritmie ventricolari nel follow-up tre volte maggiore rispetto ai pazienti senza evidenza di MAD;
- più ampio il MAD, maggiore il rischio aritmico;
- l’esito dell’intervento è stato tuttavia simile per i pazienti con e senza evidenza di MAD e la presenza di MAD non ha comportato una maggiore necessità di reintervento o di scompenso cardiaco a distanza.
Vi è spesso una “over-diagnosi” di disgiunzione mitro-anulare che, ad una indagine di popolazione generale, inclusa nel progetto UK Biobank e sottoposta a risonanza magnetica, sarebbe presente addirittura nel 76% dei casi e quindi essere una variante frequente della normalità[4]Zugwitz D, Fung K, Aung N, et al. Mitral annular disjunction assessed using CMR imaging: insights from the UK Biobank Population Study. JACC Cardiovasc Imaging 2022;15:1856–66. … Continua a leggere. Gli autori in proposito rilevano l’importanza di diagnosticare solo la disgiunzione a sede infero-laterale, l’unica che si associ ad un rischio aritmico aumentato.
Nella Discussione si ipotizza che il meccanismo attraverso il quale il rischio aritmico permanga aumentato nonostante la correzione chirurgica del vizio mitralico (e quindi l’assenza postoperatoria della disgiunzione mitro-anulare) possa consistere in una fibrosi miocardica, risultante dallo stress esercitato sui muscoli papillari prima dell’intervento. Il maggior pregio dello studio risiede nell’aver focalizzato l’attenzione su un subset di pazienti prevalentemente di sesso femminile, con prolasso mitralico, MAD e malattia di Barlow, caratteristiche che definiscono la sindrome del prolasso mitralico aritmogeno[5]Sabbag A, Essayagh B, Barrera JDR, et al. EHRA expert consensus statement on arrhythmic mitral valve prolapse and mitral annular disjunction complex in collaboration with the ESC Council on valvular … Continua a leggere.
Tuttavia l’analisi è molto debole, soffre di una retrospettività priva di un progetto che permettesse di fornire dati adeguati allo scopo del lavoro. C’è da domandarsi come sia possibile determinare un burden aritmico senza prevedere una registrazione ecg continua di almeno 24 ore, ipotizzare la presenza di un substrato anatomico (fibrosi) per l’eventuale aritmogenicità senza avere almeno un gruppo di pazienti studiati con risonanza magnetica. Le stesse conclusioni non convincono: dichiarare che esista un rischio aritmico aumentato nei pazienti con MAD anche dopo un intervento efficace (in base ad una metodologia molto lacunosa) collide con la prognosi buona di questi pazienti ad oltre 5 anni di follow-up, come mostrano i dati della Tabella. Non vi sono stati infatti decessi in quel gruppo, un solo paziente ha necessitato di terapia ablativa e non vi è stata differenza significativa nell’impianto di defibrillatore rispetto al gruppo di controllo.
Editoriale: Mitral annular disjunction nel prolasso mitralico: la chirurgia corregge l’anatomia, ma non il rischio aritmico
A cura di: Michele Ricci, Federico Fortuni, SC Cardiologia e Fisiopatologia Cardiovascolare, Azienda Ospedaliera di Perugia e Università degli Studi di Perugia
Il prolasso della valvola mitrale (MVP) rappresenta una delle cause più frequenti di insufficienza mitralica nei paesi occidentali. In circa il 75% dei casi l’MVP si associa a un’insufficienza valvolare non significativa ed ha una prognosi favorevole. Tuttavia, in circa un quarto dei pazienti l’insufficienza mitralica progredisce nel tempo, determinando dilatazione e disfunzione del ventricolo sinistro, scompenso cardiaco, peggioramento della qualità di vita e un aumento del rischio di ospedalizzazioni e di mortalità.
Negli ultimi anni è emerso un sottogruppo di pazienti con MVP caratterizzato da un fenotipo più maligno, associato a un rischio aumentato di aritmie ventricolari anche in assenza di insufficienza mitralica significativa. Questo rischio aritmico è stato correlato a specifiche caratteristiche anatomiche dell’apparato valvolare mitralico, tra cui la mitral annular disjunction (MAD), la malattia di Barlow e il prolasso bileaflet, oltre a elementi cardiaci extra-valvolari come la presenza di fibrosi visualizzabile come aree di late gadolinium enhancement alla risonanza magnetica cardiaca a livello della parete inferolaterale del ventricolo sinistro o dei muscoli papillari. Il rischio aritmico in questi pazienti può essere stratificato anche in base ad altri esami quali ad esempio l’elettrocardiogramma (ECG) a 12 derivazioni a riposo che può presentare delle onde T negative in sede inferolaterale, frequenti extrasistoli ventricolari al monitoraggio ECG Holter come pure tachicardia ventricolari sostenute o meno che possono essere evidenziate anche al test da sforzo. Dal punto di vista clinico, la presenza di cardiopalmo, sincopi e/o lipotimie senza altra causa apparente rappresentano altri elementi importanti per la stratificazione del rischio aritmico in questi pazienti[6]Miller MA, Dukkipati SR, Turagam M, Liao SL, Adams DH, Reddy VY. Arrhythmic Mitral Valve Prolapse: JACC Review Topic of the Week. J Am Coll Cardiol. 2018;72:2904-2914. La MAD è definita come il distacco dell’anello mitralico dalla giunzione atrioventricolare inferolaterale. Durante la sistole, la contrazione del miocardio inferolaterale determina uno scivolamento dell’anello mitralico, che risulta disaccoppiato dal miocardio ventricolare e rende la MAD in genere maggiormente evidente rispetto alla diastole. Recentemente, la MAD è stata distinta in una forma “vera”, visibile sia in sistole sia in diastole, e in una forma “pseudo”, apprezzabile esclusivamente in sistole. Questa distinzione ha contribuito a una definizione più rigorosa e a una maggiore precisione diagnostica.
In questo contesto si inserisce lo studio di Lodin et al[7]Essayagh B, Sabbag A, El-Am E, Cavalcante JL, Michelena HI, Enriquez-Sarano M. Arrhythmic mitral valve prolapse and mitral annular disjunction: pathophysiology, risk stratification, and management. … Continua a leggere che rappresenta una delle analisi più solide disponibili sul rischio aritmico a lungo termine nei pazienti con MVP e MAD sottoposti a chirurgia mitralica per la presenza di una insufficienza valvolare mitralica significativa.
La coorte comprende pazienti con MVP e insufficienza mitralica moderata o severa, con o senza MAD, sottoposti a riparazione o sostituzione valvolare tra il 2010 e il 2022 presso il Karolinska University Hospital di Stoccolma. Su 599 pazienti operati, la MAD è stata identificata nel 16% dei casi. Sebbene questa prevalenza sia inferiore rispetto ad altre casistiche, il dato assume particolare rilevanza clinica poiché deriva da criteri morfologici stringenti, che escludono pseudo-dislocazioni e artefatti. Rispetto ai pazienti senza MAD, quelli con MAD preoperatoria risultavano più giovani, prevalentemente di sesso femminile e presentavano una netta predominanza di malattia di Barlow e prolasso bileaflet. Mostravano inoltre una minore prevalenza di fibrillazione o flutter atriale, punteggi EuroSCORE II più bassi e una classe funzionale NYHA inferiore. Dal punto di vista ecocardiografico, la frazione di eiezione ventricolare sinistra e le dimensioni ventricolari risultavano sovrapponibili, così come il volume atriale sinistro indicizzato, mentre la pressione sistolica polmonare e la velocità massima del rigurgito tricuspidale erano inferiori. La presenza di MVP e MAD definisce un fenotipo peculiare, noto come prolasso mitralico aritmogeno, in cui un difetto anatomico si associa a un potenziale aritmico intrinseco. Uno degli aspetti più rassicuranti per il cardiochirurgo che emerge dallo studio è la dimostrazione che la MAD si risolve completamente dopo l’intervento chirurgico, indipendentemente dalla tecnica utilizzata, sia essa riparativa o sostitutiva. Tuttavia, il risultato più rilevante e al tempo stesso più problematico è che la presenza di MAD preoperatoria si associa a un rischio triplicato di aritmie ventricolari nel follow-up a lungo termine, indipendentemente dal tipo di procedura eseguita e dalla sua correzione chirurgica (Figura).

Questo dato mette in discussione l’idea che la MAD rappresenti esclusivamente un difetto anatomico correggibile. Al contrario, suggerisce che essa sia il marker di un substrato aritmico sottostante, potenzialmente legato a fibrosi dei muscoli papillari, rimodellamento ventricolare, predisposizione genetica o forme iniziali di cardiomiopatia. In altre parole, la chirurgia corregge il difetto anatomico e l’emodinamica valvolare, ma non elimina il rischio aritmico associato. È verosimile che, in presenza di MAD, lo stress meccanico cronico esercitato dall’eccessiva mobilità dell’apparato valvolare acceleri la degenerazione dei lembi, favorisca la fibrosi miocardica e contribuisca alla creazione di un substrato aritmogeno che persiste anche dopo la correzione chirurgica[8]van Wijngaarden AL, de Riva M, Hiemstra YL, et al. Parameters associated with ventricular arrhythmias in mitral valve prolapse with significant regurgitation. Heart. 2021;107:411-418.
Le implicazioni pratiche per il cardiochirurgo sono rilevanti. Innanzitutto, la MAD deve entrare stabilmente nel linguaggio e nella valutazione preoperatoria, non tanto per modificare la tecnica chirurgica, che si è dimostrata sicura ed efficace, quanto per identificare un sottogruppo di pazienti che necessita di un follow-up aritmologico dedicato. In secondo luogo, il counseling preoperatorio deve essere aggiornato (Figura): i pazienti con MAD devono essere informati che, anche dopo una chirurgia tecnicamente riuscita, il rischio residuo di aritmie ventricolari rimane più elevato rispetto ai pazienti senza MAD. Ne consegue la necessità di una collaborazione più stretta con l’aritmologo. Alla dimissione, questi pazienti non possono essere gestiti secondo i percorsi standard, ma richiedono strategie condivise che includano monitoraggi ECG prolungati, followup ravvicinati nei primi anni postoperatori, valutazione precoce del burden aritmico e, nei casi selezionati, l’impiego di loop recorder o la discussione dell’indicazione a defibrillatore impiantabile in base ad una valutazione olistica del loro rischio aritmico[9]Van der Bijl P, Stassen J, Haugaa KH, et al. Mitral Annular Disjunction in the Context of Mitral Valve Prolapse: Identifying the At-Risk Patient. JACC Cardiovasc Imaging. 2024;17:1229-12459. Inoltre, la presenza di MAD solleva interrogativi sul timing chirurgico: se da un lato questi pazienti tendono a presentarsi più precocemente, dall’altro suggerisce che lo sviluppo del substrato aritmogeno possa avvenire indipendentemente dalla severità del rigurgito mitralico, aprendo il dibattito su un possibile intervento anticipato in sottogruppi selezionati. È importante sottolineare cosa non deve preoccupare il cardiochirurgo. Lo studio dimostra che la MAD non complica la riparazione mitralica, non aumenta il rischio di reintervento, non compromette il sizing o la stabilità dell’anello e non richiede tecniche chirurgiche dedicate. Il chirurgo può quindi affrontare questi pazienti con la stessa sicurezza tecnica riservata al MVP senza MAD. Tuttavia, il messaggio chiave è che l’anomalia anatomica rappresenta solo la punta dell’iceberg: la MAD è un marcatore di una patologia che coinvolge non solo la valvola, ma anche il miocardio[10]Fortuni F, Bax JJ, Delgado V. Changing the Paradigm in the Management of Valvular Heart Disease: In Addition to Left Ventricular Ejection Fraction, Focus on the Myocardium. Circulation. … Continua a leggere (Figura).
In conclusione, la chirurgia mitralica corregge efficacemente l’insufficienza valvolare e ripristina l’anatomia, ma non normalizza il rischio aritmico nei pazienti con MAD. Per il cardiochirurgo questo significa, da un lato, continuare a considerare l’intervento un’opzione valida e sicura e, dall’altro, integrare il successo chirurgico con una strategia postoperatoria multidisciplinare che includa il monitoraggio aritmico a lungo termine. La MAD non deve quindi allarmare il cardiochirurgo, ma guidarlo verso una gestione più completa e moderna del paziente con prolasso mitralico, una patologia che è al tempo stesso valvolare e miocardica.
Bibliografia[+]
| ↑1 | Delling FN, Rong J, Larson MG, et al. Evolution of mitral valve prolapse: insights from the Framingham Heart Study Circulation 2016;133: 1688–95. https://doi.org/10.1161/CIRCULATIONAHA.115.020621 |
|---|---|
| ↑2 | Basso C, Perazzolo Marra M, Rizzo S, et al. Arrhythmic mitral valve prolapse and sudden cardiac death. Circulation 2015;132: 556–66. https://doi.org/10.1161/CIRCULATIONAHA.115.016291 |
| ↑3 | Han Y, Peters DC, Salton CJ, Bzymek D, Nezafat R, Goddu B, et al. Cardiovascular magnetic resonance characterization of mitral valve prolapse. JACC Cardiovasc Imaging 2008; 1:294–303. https://doi.org/10.1016/j.jcmg.2008.01.013. |
| ↑4 | Zugwitz D, Fung K, Aung N, et al. Mitral annular disjunction assessed using CMR imaging: insights from the UK Biobank Population Study. JACC Cardiovasc Imaging 2022;15:1856–66. https://doi.org/10.1016/j.jcmg.2022.07.015 |
| ↑5 | Sabbag A, Essayagh B, Barrera JDR, et al. EHRA expert consensus statement on arrhythmic mitral valve prolapse and mitral annular disjunction complex in collaboration with the ESC Council on valvular heart disease and the European Association of Cardiovascular Imaging endorsed cby the Heart Rhythm Society, by the Asia Pacific Heart Rhythm Society, and by the Latin American Heart Rhythm Society. Europace 2022;24:1981–2003. https://doi.org/10.1093/europace/euac125. |
| ↑6 | Miller MA, Dukkipati SR, Turagam M, Liao SL, Adams DH, Reddy VY. Arrhythmic Mitral Valve Prolapse: JACC Review Topic of the Week. J Am Coll Cardiol. 2018;72:2904-2914 |
| ↑7 | Essayagh B, Sabbag A, El-Am E, Cavalcante JL, Michelena HI, Enriquez-Sarano M. Arrhythmic mitral valve prolapse and mitral annular disjunction: pathophysiology, risk stratification, and management. Eur Heart J. 2023;44:3121-3135. Lodin K, Da Silva CO, Wang Gottlieb A, et al. Mitral annular disjunction and mitral valve prolapse: long-term risk of ventricular arrhythmias after surgery. Eur Heart J. 2025;46:2795-2805 |
| ↑8 | van Wijngaarden AL, de Riva M, Hiemstra YL, et al. Parameters associated with ventricular arrhythmias in mitral valve prolapse with significant regurgitation. Heart. 2021;107:411-418 |
| ↑9 | Van der Bijl P, Stassen J, Haugaa KH, et al. Mitral Annular Disjunction in the Context of Mitral Valve Prolapse: Identifying the At-Risk Patient. JACC Cardiovasc Imaging. 2024;17:1229-12459 |
| ↑10 | Fortuni F, Bax JJ, Delgado V. Changing the Paradigm in the Management of Valvular Heart Disease: In Addition to Left Ventricular Ejection Fraction, Focus on the Myocardium. Circulation. 2021;143:209-211. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

