Inquadramento
L’ematopoiesi clonale a potenziale indeterminato (CHIP) è un fenomeno comune negli anziani (10%-20%), e consiste in mutazioni di alcuni geni di cellule staminali del midollo osseo deputati alla regolazione epigenetica (come DNMT3A, TET2, ASXL1) o alla riparazione del DNA (come TP53 e PPM1D) che conducono alla formazione di un clone per la produzione di cellule ematopoietiche senza causare una patologia ematologica conclamata, ma associato a un aumentato rischio di sviluppare malattie cardiovascolari[1]Jaiswal S, Fontanillas P, Flannick J, et al. Age-related clonal hematopoiesis associated with adverse outcomes. N Engl J Med. 2014;371:2488-2498. doi:10.1056/NEJMoa1408617. Recentemente, CHIP è emerso come un fattore di rischio per lo sviluppo di scompenso cardiaco (HF), soprattutto a frazione di eiezione conservata[2]Schuermans A, Honigberg MC, Raffield LM, et al. Clonal hematopoiesis and incident heart failure with preserved ejection fraction. JAMA Netw Open.2024;7:e2353244-e2353244. … Continua a leggere. Esistono tuttora incertezze sul ruolo specifico di alcuni geni meno comuni nel determinare il rischio di HF, così come non risulta chiaro se tale rischio venga mediato da alcune comorbilità quali la malattia coronarica, il diabete tipo 2, la fibrillazione atriale, la nefropatia cronica, anch’esse correlate alla CHIP.
Lo studio in esame
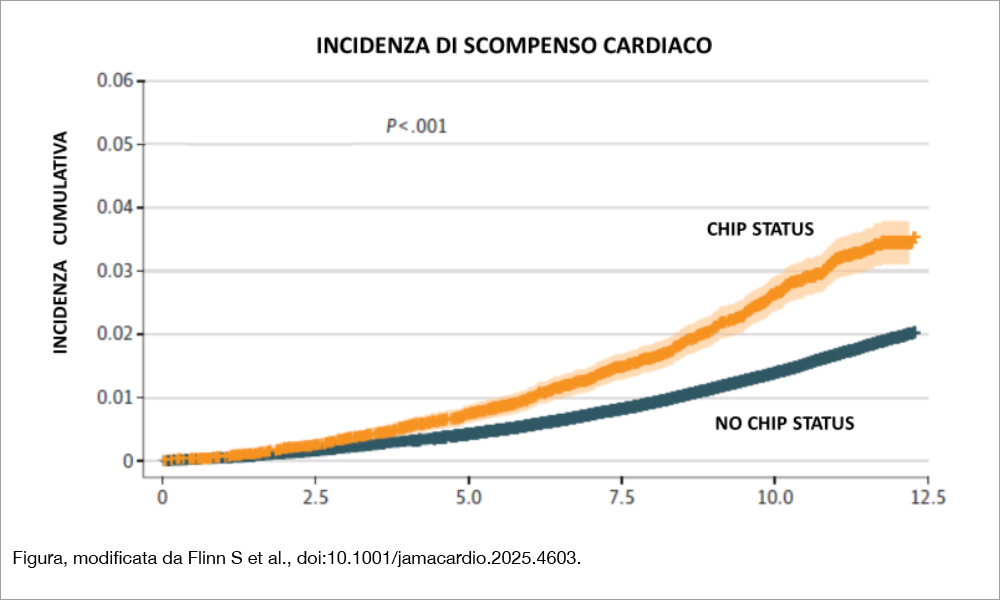
Lo scopo del lavoro è stato quello di testare quali varianti genetiche di CHIP si correlino con lo sviluppo di HF e se l’eventuale associazione osservata sia mediata da alcune comorbilità. A tal fine sono stati studiati 417.616 individui inclusi nel database UK Biobank tra il 2006 e il 2010 e seguiti sino al 2020 (età media 56.1 anni, il 56.2% erano donne). I partecipanti, al momento dell’inclusione non erano affetti da HF, nè da altre patologie correlate con CHIP e potenziale successivo sviluppo di HF (quali coronaropatia, fibrillazione atriale, diabete tipo 2, nefropatia cronica). Tutti erano stati sottoposti a sequenziamento dell’intero esoma (Whole Exome Sequencing -WES-), con analisi di tutte le regioni codificanti (esoni) del DNA per identificare la frequenza delle mutazioni genetiche associate a CHIP. Complessivamente in 13.836 individui (3.3%) sono state individuate varianti genetiche associate a CHIP: le più frequenti sono DNMT3A (osservata nel 63.5% dei casi) seguita da TET2 (14.4%) e ASXL1 (10.3%), varianti deputate alla regolazione epigenetica. Meno rappresentati i geni deputati alla riparazione del DNA (4.3%), quelli del spliceosoma (essenziale nel processo di formazione dell’RNA messaggero, 3.0%), e JAK2 (codifica per la proteina omonima e controlla la crescita e la proliferazione delle cellule emopoietiche, 0.8%). I soggetti “CHIP carriers” avevano un profilo cardiovascolare peggiore, una PA più elevata e uno status socio-economico più basso rispetto ai non portatori.Ad un follow-up mediano di 11.1 anni, si è sviluppato HF nell’1.7% della popolazione. CHIP è risultato associato, all’analisi multivariata, con HF (HR aggiustato -a- 1.27; 95% CI,1.15-1.40; P<.001).Tale associazione era piuttosto debole per DNMT3A (aHR, 1.15; 95% CI, 1.00-1.31; P=.04), mentre è risultata più significativa per le altre varianti, cioè quelle non-DNMT3A (aHR, 1.52; 95% CI, 1.33-1.75; P<.001, vedi Figura). L’analisi di mediazione ha permesso di verificare se lo sviluppo di HF fosse mediato dalle comorbilità (lo sviluppo di coronaropatia, fibrillazione atriale, diabete di tipo 2 e nefropatia cronica), oppure dipendente dalle varianti genetiche. È stata utilizzata un’analisi con propensity matching tra soggetti con ognuna delle 4 comorbilità e gli individui con varianti CHIP e si è osservata l’incidenza di HF nel tempo. La percentuale di mediazione di tutti 4 fattori combinati sullo sviluppo di HF è risultata del 28.2%.
Take home message
I risultati di questo studio di coorte suggeriscono che CHIP, soprattutto se correlato alle varianti non-DNMT3A, si associa allo sviluppo di scompenso cardiaco. Alcune comorbilità, anch’esse associate a CHIP, spiegano solo poco più di un quarto di tale associazione. CHIP è pertanto un fattore di rischio per scompenso e rappresenta un nuovo target terapeutico.
Interpretazione dei dati
L’argomento è di grande rilevanza clinica anche se appare piuttosto insolito per i cardiologi. In effetti, la ricerca clinica sui CHIP ha inizialmente riguardato gli ematologi per individuare le origini delle leucemie, ma si è sorprendentemente estesa ai cardiologi, allorchè è emersa la relazione tra la presenza di varianti genetiche che inducono l’ematopoiesi clonale e lo sviluppo di alcune patologie cardiache. Gli sviluppi clinici sono ancora poco noti, essendo la ricerca clinica in fase iniziale. La popolazione cui si rivolge è quella dei soggetti anziani, che manifestano la presenza di CHIP in percentuali piuttosto alte (10%-20% dopo i 70 anni). I contributi in questo ambito si stanno arricchendo rapidamente di nuove osservazioni, talune sorprendenti e dalle conseguenze cliniche interessanti. Un’analisi dello studio ASPREE[3]McQuilten ZK, Thao LTP, Bick AG, et al. Clonal hematopoiesis and cardiovascular disease and bleeding risk and the effectiveness of aspirin. JAMA Cardiol. 2025. doi:10.1001/jamacardio.2025.3756 ha notato come pazienti CHIP inclusi in quello studio di prevenzione primaria avessero un rischio aumentato di bleeding, un’osservazione che potrebbe avere notevoli riflessi terapeutici, soprattutto nella popolazione coronaropatica in prevenzione secondaria. Sono state avanzate ipotesi di trattamento anti-infiammatorio in pazienti CHIP. Infatti, alcune varianti genetiche attivano l’inflammasoma NLRP3 con conseguente secrezione da parte dei macrofagi di interleuchina (IL) 1-beta e IL-6, successiva infiammazione miocardica e rimodellamento fibrotico. Lo studio HERMES, attualmente in corso, sta valutando gli effetti di ziltivekimab, un inibitore di IL-6, in pazienti con HFpEF e con HFmrEF. È interessante l’osservazione che alcuni farmaci, come la metformina, riducano l’espansione di una variante DNMT3A, mentre la colchicina ridurrebbe l’espansione clonale di CHIP non-DNMT3A. Dobbiamo ancora conoscere molto di questa patologia prima di poterne derivare delle conseguenze pratiche sul piano clinico. Come scrivono Chiu e Libby, CHIP è un fattore di rischio alla ricerca di una “roadmap”, una definizione diagnostica senza un chiaro percorso terapeutico davanti a sè[4]Chiu N, Libby P. New Bleeding Signal in Clonal Hematopoiesis-White Cells, Red Flags. JAMA Cardiol 2025; 10:1235-1237. doi:10.1001/jamacardio.2025.3744.
Editoriale: “CREST-2: una svolta necessaria nel trattamento della stenosi carotidea asintomatica”
A cura di: Alberto Bramucci, Diego Moniaci – S.C. Chirurgia Vascolare, Dipartimento Area Chirurgica, Azienda Sanitaria Locale Città di Torino “Ospedale San Giovanni Bosco”, Torino
Il recente trial pubblicato sul New England Journal of Medicine, CREST-2[5]Brott TG, Howard G, Lal BK, et al. Medical management and revascularization for asymptomatic carotid stenosis. NEJM. Published online November 21, 2025. doi:10.1056/NEJMoa2508800, riporta al centro del dibattito scientifico una delle questioni più controverse della moderna medicina cardiovascolare: il reale beneficio della rivascolarizzazione carotidea nei pazienti asintomatici nell’era della Best Medical Therapy. A distanza di decenni dagli studi che hanno guidato la pratica clinica (ACAS, ACST-1, EVA-3S, SPACE e CREST), CREST-2 rappresenta una revisione critica dei presupposti su cui si fonda la prevenzione primaria di un evento cerebrovascolare, secondario a stenosi carotidea significativa[6]Naylor AR. Time to rethink management strategies in asymptomatic carotid artery disease. Nat Rev Cardiol 2011; 9:116-24.
Per lungo tempo, la stenosi carotidea asintomatica severa è stata considerata una condizione “silenziosa ma pericolosa”, tale da giustificare strategie più o meno invasive come l’endoarteriectomia carotidea (CEA) o lo stenting carotideo (CAS). Tuttavia, tali indicazioni derivavano da studi condotti in un contesto terapeutico profondamente diverso dall’attuale[7]Halliday A, Harrison M, Hayter E, et al. Asymptomatic Carotid Surgery Trial (ACST) Collaborative Group. 10-year stroke prevention after successful carotid endarterectomy for asymptomatic stenosis … Continua a leggere.
Negli ultimi anni, il progresso della terapia medica con farmaci antiaggreganti più efficaci, statine ad alta intensità, nuove classi di farmaci ipolipemizzanti, un controllo più stringente dei fattori di rischio cardiovascolare e una maggiore attenzione agli stili di vita, ha contributo in modo sostanziale alla riduzione dell’incidenza di eventi cerebrovascolari nei pazienti asintomatici. È su questo mutato scenario che si fonda il razionale di CREST-2, uno studio multicentrico che ha coinvolto 155 centri in Australia, Canada, Israele, Spagna e Stati Uniti, arruolando complessivamente 2.485 pazienti con stenosi carotidea asintomatica significativa. Il trial è strutturato come due studi paralleli randomizzati: nel primo, la migliore terapia medica (BMT) è confrontata con BMT associata a CAS; nel secondo, BMT è confrontata con BMT associata a CEA. Nel braccio CAS sono stati randomizzati 1.245 pazienti (età media 69 anni, 62% uomini), mentre nel braccio CEA 1.240 pazienti (età media 70 anni, 63% uomini). L’endpoint primario era un composito di ictus o morte peri-procedurale entro 44 giorni, mentre l’endpoint secondario principale era l’insorgenza di ictus ischemico ipsilaterale fino a quattro anni di follow-up. Nel confronto CAS + BMT versus BMT da sola, l’aggiunta della procedura endovascolare ha determinato una riduzione significativa dell’endpoint primario a quattro anni (2,8% vs 6,0%; P= 0,02), con una riduzione assoluta del rischio del 3,2%.
Al contrario, nel confronto CEA + BMT versus BMT, non è emersa una differenza statisticamente significativa (3,7% vs 5,3%; P=0,24). In sintesi, nei pazienti con stenosi carotidea asintomatica di alto grado, solo la rivascolarizzazione endovascolare ha mostrato un beneficio statisticamente significativo rispetto alla sola terapia medica intensiva, mentre la rivascolarizzazione chirurgica non ha dimostrato un vantaggio netto. Dal punto di vista metodologico, CREST-2 rappresenta un esempio di trial pragmatico contemporaneo. La rigorosa selezione dei centri, la standardizzazione delle procedure e l’attenzione alla riduzione delle complicanze peri-procedurali, rispondono alle principali criticità sollevate nei precedenti studi comparativi tra CEA e CAS. Tuttavia, il valore più rilevante dello studio non risiede nella superiorità di una tecnica sull’altra, bensì nelle domande che esso solleva: come interpretare questi risultati nell’era della terapia medica ottimale? Ha ancora senso intervenire in pazienti che non hanno mai manifestato un evento neurologico?
I risultati di CREST-2 appaiono coerenti con quelli di altri studi randomizzati più recenti, quali SPACE-2[8]Reiff T, Eckstein H-H, Mansmann U, et al. Carotid endarterectomy or stenting or best medical treatment alone for moderateto-severe asymptomatic carotid artery stenosis: 5-year results of a … Continua a leggere ed ECST-2[9]Donners SJA, van Velzen TJ, Cheng SF, et al. Optimised medical therapy alone versus optimised medical therapy plus revascularisation for asymptomatic or low-to-intermediate risk symptomatic carotid … Continua a leggere, che hanno progressivamente ridimensionato il ruolo della rivascolarizzazione routinaria nella stenosi carotidea asintomatica. Nel loro insieme, questi dati suggeriscono una riduzione del beneficio assoluto dell’intervento, in particolare della CEA, rispetto alla gestione medica ottimizzata. L’apparente vantaggio osservato con CAS in CREST-2 deve tuttavia essere interpretato con cautela[10]Brown MM, Bonati LH. Managing Asymptomatic Carotid Stenosis. N Engl J Med. 2026 Jan 15;394(3):296-297. doi:10.1056/NEJMe2515725. Epub 2025 Nov 21. PMID:41269202.
In primo luogo, il basso tasso di eventi nel gruppo CAS riflette una selezione rigorosa dei pazienti e l’elevata expertise degli operatori, condizioni non sempre riproducibili nella pratica clinica quotidiana. Studi precedenti, incluso ACST-27, hanno riportato un rischio peri-procedurale di ictus o morte superiore di circa l’1% con CAS rispetto alla CEA.
In secondo luogo, la significatività statistica del beneficio dello stenting si basa su un numero relativamente esiguo di eventi; gli autori riferiscono che se si fossero verificati solo tre eventi in più nel gruppo dello stenting, la differenza non avrebbe raggiunto la significatività statistica. Non sorprende, dunque, che nello studio SPACE-2, in cui il numero di pazienti sottoposti a CAS era limitato, non sia emerso alcun vantaggio rispetto alla sola terapia medica. In effetti, guardando i tassi cumulativi di eventi in tutti e quattro i gruppi del CREST-2, vi sono più somiglianze che differenze tra CEA e CAS. Un elemento di particolare rilevanza di CREST-2 è il ruolo centrale attribuito alla terapia medica intensiva. Essa non è più considerata un semplice braccio di controllo, ma un intervento strutturato, monitorato e attivo, posto sullo stesso piano concettuale delle strategie di rivascolarizzazione. Questo approccio sottolinea come la prevenzione dell’ictus nei pazienti asintomatici richieda tempo, aderenza terapeutica e una relazione continuativa tra paziente e sistema sanitario. Alla domanda se sia ancora giustificato intervenire in pazienti asintomatici, CREST-2 non fornisce risposte definitive, né potrebbe farlo data la complessità del problema. Tuttavia, contribuisce in modo sostanziale a spostare il baricentro del dibattito verso una medicina sempre più personalizzata.
La decisione terapeutica dovrebbe derivare da una valutazione multidisciplinare che consideri non solo il grado di stenosi, ma anche l’aspettativa di vita, la fragilità, l’aderenza alla terapia e le preferenze del paziente. Va inoltre sottolineato che, anche nel contesto di un trial controllato come CREST-2, l’aderenza ai target terapeutici non è stata ottimale: solo il 60– 70% dei pazienti ha raggiunto i valori pressori raccomandati, meno dell’80% i target di LDL <70 mg/dL e circa la metà dei pazienti diabetici un adeguato controllo glicemico. L’introduzione di nuove terapie ipolipemizzanti e target di LDL ancora più stringenti potrebbero modificare ulteriormente il rapporto rischio-beneficio della rivascolarizzazione. Infine, CREST-2 potrebbe avere un impatto rilevante sulle future Linee Guida. Qualora i risultati finali confermassero un beneficio marginale della rivascolarizzazione nella maggior parte dei pazienti asintomatici, le indicazioni all’intervento verrebbero probabilmente ristrette a sottogruppi altamente selezionati. Ciò non segnerebbe la fine della chirurgia carotidea, ma una sua più appropriata e razionale collocazione. Anche le implicazioni etiche ed economiche non sono trascurabili: dimostrare che strategie meno invasive sono altrettanto efficaci avrebbe conseguenze importanti sulla sostenibilità dei sistemi sanitari e sulla qualità delle cure.
In conclusione, CREST-2 non è soltanto un aggiornamento scientifico, ma un invito a riconsiderare dogmi consolidati alla luce dell’evidenza contemporanea. In attesa dei risultati definitivi, lo studio ha già raggiunto un obiettivo fondamentale: ricordarci che la migliore medicina non è necessariamente quella che interviene di più, ma quella che sceglie meglio, ponendo il paziente, e non la procedura, al centro delle decisioni cliniche.
Bibliografia[+]
| ↑1 | Jaiswal S, Fontanillas P, Flannick J, et al. Age-related clonal hematopoiesis associated with adverse outcomes. N Engl J Med. 2014;371:2488-2498. doi:10.1056/NEJMoa1408617 |
|---|---|
| ↑2 | Schuermans A, Honigberg MC, Raffield LM, et al. Clonal hematopoiesis and incident heart failure with preserved ejection fraction. JAMA Netw Open.2024;7:e2353244-e2353244. doi:10.1001/jamanetworkopen.2023.53244 |
| ↑3 | McQuilten ZK, Thao LTP, Bick AG, et al. Clonal hematopoiesis and cardiovascular disease and bleeding risk and the effectiveness of aspirin. JAMA Cardiol. 2025. doi:10.1001/jamacardio.2025.3756 |
| ↑4 | Chiu N, Libby P. New Bleeding Signal in Clonal Hematopoiesis-White Cells, Red Flags. JAMA Cardiol 2025; 10:1235-1237. doi:10.1001/jamacardio.2025.3744 |
| ↑5 | Brott TG, Howard G, Lal BK, et al. Medical management and revascularization for asymptomatic carotid stenosis. NEJM. Published online November 21, 2025. doi:10.1056/NEJMoa2508800 |
| ↑6 | Naylor AR. Time to rethink management strategies in asymptomatic carotid artery disease. Nat Rev Cardiol 2011; 9:116-24 |
| ↑7 | Halliday A, Harrison M, Hayter E, et al. Asymptomatic Carotid Surgery Trial (ACST) Collaborative Group. 10-year stroke prevention after successful carotid endarterectomy for asymptomatic stenosis (ACST-1): a multicentre randomised trial. Lancet. 2010 Sep 25;376(9746):1074-84. doi:10.1016/S0140-6736(10)61197-X. |
| ↑8 | Reiff T, Eckstein H-H, Mansmann U, et al. Carotid endarterectomy or stenting or best medical treatment alone for moderateto-severe asymptomatic carotid artery stenosis: 5-year results of a multicentre, randomised controlled trial. Lancet Neurol 2022; 21:877-88 |
| ↑9 | Donners SJA, van Velzen TJ, Cheng SF, et al. Optimised medical therapy alone versus optimised medical therapy plus revascularisation for asymptomatic or low-to-intermediate risk symptomatic carotid stenosis (ECST-2): 2-year interim results of a multicentre randomised trial. Lancet Neurol 2025;24:389-99. |
| ↑10 | Brown MM, Bonati LH. Managing Asymptomatic Carotid Stenosis. N Engl J Med. 2026 Jan 15;394(3):296-297. doi:10.1056/NEJMe2515725. Epub 2025 Nov 21. PMID:41269202 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

