Inquadramento
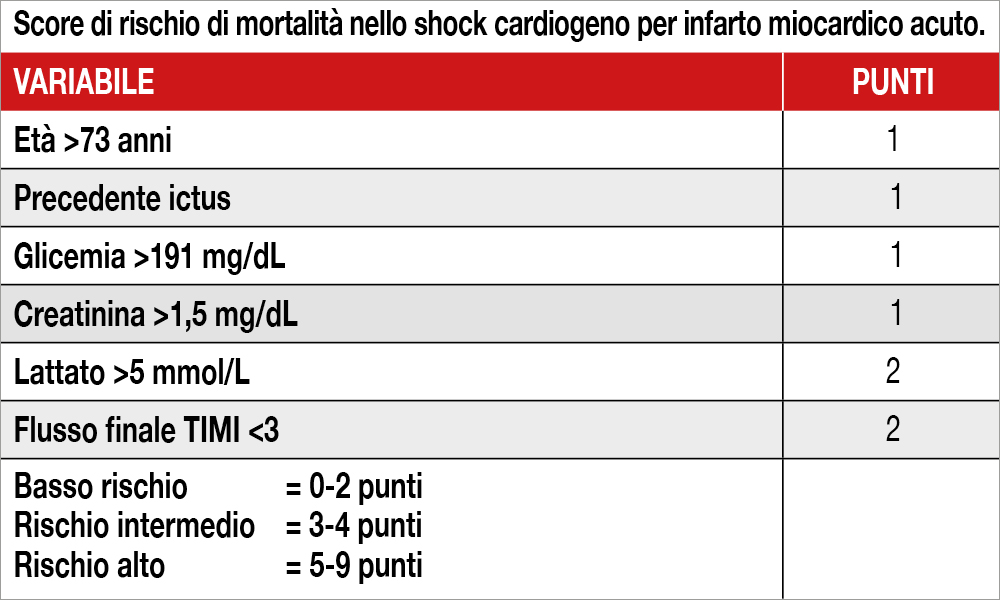
La misurazione del lattato da prelievo arterioso è divenuto routine nelle nostre terapie intensive e rappresenta una variabile prognostica di grande valore nel paziente in shock cardiogeno per infarto miocardico. Lo score di rischio di mortalità, derivato dallo studio Intraaortic Balloon Pump in Cardiogenic Shock II (IABP-SHOCK II)[1]Poss J, Koster J, Fuernau G, et al. Risk stratification for patients in cardiogenic shock after acute myocardial infarction. J Am Coll Cardiol 2017;69: 1913–20., lo include attribuendogli un punteggio simile al mancato raggiungimento di un flusso TIMI 3 dopo una procedura riperfusiva di angioplastica primaria (Tabella). Tuttavia, non è chiaro se misurazioni addizionali, rispetto a quella iniziale di ingresso, possano essere utili e in particolare se la clearance del lattato possa migliorarne la capacità predittiva prognostica, come segnalato per lo shock settico[2]Nguyen HB, Rivers EP, Knoblich BP, et al. Early lactate clearance is associated with improved outcome in severe sepsis and septic shock. Crit Care Med 2004;32:1637–42..
Lo studio in esame
Questo studio è una sub-analisi dello IABP-SHOCK II trial e annesso registro che ha come scopo quello di valutare se il valore di lattato a 8 ore e la sua clearance diano informazioni prognostiche superiori rispetto al valore di lattato basale.
Nei 671 pazienti inclusi, l’area sotto la curva ROC dava un valore significativamente superiore (p<.001) per la misurazione a 8 ore (0.76) rispetto al valore basale (0.69) e alla clearance (0.59). Nell’analisi multivariata un valore del lattato di 3.1 mmol/L (HR 2.89, 95% CI da 2.10 a 3.97) e un valore di clearance ≤3.45%/h risultavano predittori indipendenti di mortalità a 30 giorni.
Take home message
Il valore del prelievo arterioso di lattato a 8 ore dalla prima determinazione ha un valore predittivo superiore al prelievo inizale e alla sua clearance. Un valore di cutoff di 3.1 mmol/L dopo 8 ore ha mostrato il miglior valore discriminativo per stabilire la prognosi nello shock cardiogeno ed è da considerare un nuovo goal terapeutico.
Interpretazione dei dati
Il punto di forza dello studio risiede nell’ampia casistica di riferimento e nei rigorosi criteri di arruolamento nel trial e registro da cui proviene la serie di pazienti considerata per questa analisi. Benchè sia da tempo nota la validità prognostica del valore di lattato da prelievo arterioso nello shock cardiogeno, non esiste molta letteratura di riferimento. Valori elevati di lattato sono espressione di attivazione del sistema nervoso simpatico, con aumentata glicolisi per shift metabolico come risposta a una situazione di stress. Non stupisce il maggior rilievo prognostico di un prelievo più tardivo rispetto a quello della presentazione clinica del paziente.
Infatti, il primo valore può essere troppo dipendente dal quadro iniziale, spesso drammatico e accompagnato da arresto cardiaco, mentre il valore successivo è espressione di un quadro clinico più definito a terapia medica ottimizzata e con procedura di riperfusione meccanica eseguita.
Tuttavia, come commentano nell’editoriale di accompagnamento Roberta Rossini e Marco Ferlini, il rilievo tardivo del valore di lattato sembra fungere più da marker prognostico fine a se stesso che da indicatore decisionale[3]Rossini R, Ferlini M. Arterial Lactate Assessment in Cardiogenic Shock: It Is High Time to Beat the Clock. JACC Cardiovasc Interv. 2020. PMID: 33032709..
L’opinione di Guido Tavazzi
Department of Clinical-Surgical, Diagnostic and Paediatric Sciences, University of Pavia; Anaesthesia and Intensive Care, Fondazione Policlinico San Matteo IRCCS, Pavia.
Il processo di definizione della fisiopatologia dello shock cardiogeno include l’identificazione di parametri clinici facilmente misurabili e riproducibili, che permettano una affidabile stratificazione di rischio al fine di impostare una terapia che sia efficace per lo specifico fenotipo clinico. L’aumento del livello di lattati è generalmente considerato un marcatore di stress metabolico, sebbene allo stesso tempo rappresenti un importante substrato energetico per le cellule, incluso il miocardio. L’aumento della produzione nel contesto dello shock cardiogeno è prevalentemente da attribuire alla disossia cellulare, conseguente alla ipoperfusione d’organo relata al deficit di portata cardiaca, sebbene la stimolazione adrenergica endogena o esogena può contribuire alla iperproduzione degli stessi[4]Brooks GA. Cell-cell and intracellular lactate shuttles. J Physiol. 2009;587(Pt 23):5591-600.visth V, Hagstrom-Toft E, Enoksson S, Bolinder J. Catecholamine regulation of local lactate production in … Continua a leggere.
Inoltre, la risultante del delicato bilancio tra produzione e clearance dei lattati in contesti di ipoperfusione tissutale è un processo tuttora non del tutto chiaro ma, sicuramente, multifattoriale[5]Hernandez G, Bellomo R, Bakker J. The ten pitfalls of lactate clearance in sepsis. Intensive Care Med. 2019;45(1):82-5.. Per questo motivo, la singola determinazione dei lattati ha una minore sensibilità nell’identificazione del meccanismo fisiopatologico sottostante, rispetto alla loro variazione in un arco di tempo.
In generale, la riduzione dei lattati in ambito di shock circolatorio è considerata un target terapeutico a breve termine, in quanto associata a un miglioramento dell’outcome [6]Vincent JL, Quintairos ESA, Couto L Jr., Taccone FS. The value of blood lactate kinetics in critically ill patients: a systematic review. Crit Care. 2016;20(1):257.. Tuttavia, la paucità di dati riguardo al ruolo dei lattati nella stratificazione di rischio e treatment strategy, viene sottolineata dalla mancanza di un cutoff validato, con conseguente relativa arbitrarietà nella definizione di severità del grado di alterazione metabolica.
Un valore >2 mmol/L di lattati, quindi molto vicino al cutoff di normalità, è stato definito come parametro biochimico integrato per la diagnosi di Stage -C cardiogenic shock[7]Baran DA, Grines CL, Bailey S, Burkhoff D, Hall SA, Henry TD, et al. SCAI clinical expert consensus statement on the classification of cardiogenic shock: This document was endorsed by the American … Continua a leggere. Nei due trial randomizzati in corso sull’efficacia e sicurezza di supporto meccanico in pazienti con shock cardiogeno relato a infarto miocardico[8]Thiele H, Freund A, Gimenez MR, de Waha-Thiele S, Akin I, Poss J, et al. Extracorporeal life support in patients with acute myocardial infarction complicated by cardiogenic shock – Design and … Continua a leggere o indipendente dalla diagnosi eziologica [9]Ostadal P, Rokyta R, Kruger A, Vondrakova D, Janotka M, Smid O, et al. Extra corporeal membrane oxygenation in the therapy of cardiogenic shock (ECMO-CS): rationale and design of the multicenter … Continua a leggere, il valore scelto come criterio di inclusione è >3 mmol/L, come indicatore di maggiore severità del profilo emodinamico per definire i pazienti candidabili per il supporto extracoporeo. Tuttavia, il valore basale ≥5.0 mmol/L, lo stesso utilizzato nel presente studio, è stato recentemente introdotto come valore prognostico per la precoce stratificazione di rischio nello score IABP-SHOCK II[10]Poss J, Koster J, Fuernau G, Eitel I, de Waha S, Ouarrak T, et al. Risk Stratification for Patients in Cardiogenic Shock After Acute Myocardial Infarction. J Am Coll Cardiol. 2017;69(15):1913-20.. I dati, riguardo iperlattacidemia nella sindrome coronarica acuta, riflettono prevalentemente esperienze monocentriche o con limitati sample size[11]Lazzeri C, Valente S, Chiostri M, Gensini GF. Clinical significance of lactate in acute cardiac patients. World J Cardiol. 2015;7(8):483-9..
L’analisi svolta da Fuernau sui pazienti arruolati nello studio e nel registro IABP SHOCK- II, sottolinea l’importanza della valutazione dei livelli di lattati ematici nei pazienti con shock cardiogeno relato a infarto miocardico. In particolare, la valutazione degli stessi in diversi punti temporali e la loro variazione (espressa come over time-clearance) in risposta al trattamento, ha dimostrato una maggiore capacità discriminatoria, rispetto al singolo valore basale, per la valutazione della prognosi a breve termine.
Bibliografia[+]
| ↑1 | Poss J, Koster J, Fuernau G, et al. Risk stratification for patients in cardiogenic shock after acute myocardial infarction. J Am Coll Cardiol 2017;69: 1913–20. |
|---|---|
| ↑2 | Nguyen HB, Rivers EP, Knoblich BP, et al. Early lactate clearance is associated with improved outcome in severe sepsis and septic shock. Crit Care Med 2004;32:1637–42. |
| ↑3 | Rossini R, Ferlini M. Arterial Lactate Assessment in Cardiogenic Shock: It Is High Time to Beat the Clock. JACC Cardiovasc Interv. 2020. PMID: 33032709. |
| ↑4 | Brooks GA. Cell-cell and intracellular lactate shuttles. J Physiol. 2009;587(Pt 23):5591-600.visth V, Hagstrom-Toft E, Enoksson S, Bolinder J. Catecholamine regulation of local lactate production in vivo in skeletal muscle and adipose tissue: role of -adrenoreceptor subtypes. J Clin Endocrinol Metab. 2008;93(1):240-6. |
| ↑5 | Hernandez G, Bellomo R, Bakker J. The ten pitfalls of lactate clearance in sepsis. Intensive Care Med. 2019;45(1):82-5. |
| ↑6 | Vincent JL, Quintairos ESA, Couto L Jr., Taccone FS. The value of blood lactate kinetics in critically ill patients: a systematic review. Crit Care. 2016;20(1):257. |
| ↑7 | Baran DA, Grines CL, Bailey S, Burkhoff D, Hall SA, Henry TD, et al. SCAI clinical expert consensus statement on the classification of cardiogenic shock: This document was endorsed by the American College of Cardiology (ACC), the American Heart Association (AHA), the Society of Critical Care Medicine (SCCM), and the Society of Thoracic Surgeons (STS) in April 2019. Catheter Cardiovasc Interv. 2019;94(1):29-37. |
| ↑8 | Thiele H, Freund A, Gimenez MR, de Waha-Thiele S, Akin I, Poss J, et al. Extracorporeal life support in patients with acute myocardial infarction complicated by cardiogenic shock – Design and rationale of the ECLS-SHOCK trial. Am Heart J. 2021;234:1-11. |
| ↑9 | Ostadal P, Rokyta R, Kruger A, Vondrakova D, Janotka M, Smid O, et al. Extra corporeal membrane oxygenation in the therapy of cardiogenic shock (ECMO-CS): rationale and design of the multicenter randomized trial. Eur J Heart Fail. 2017;19 Suppl 2:124-7. |
| ↑10 | Poss J, Koster J, Fuernau G, Eitel I, de Waha S, Ouarrak T, et al. Risk Stratification for Patients in Cardiogenic Shock After Acute Myocardial Infarction. J Am Coll Cardiol. 2017;69(15):1913-20. |
| ↑11 | Lazzeri C, Valente S, Chiostri M, Gensini GF. Clinical significance of lactate in acute cardiac patients. World J Cardiol. 2015;7(8):483-9. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

