Inquadramento
Lo shock cardiogeno rappresenta la più frequente causa di mortalità nei pazienti con infarto acuto del miocardio. Il tasso di mortalità è tuttora molto elevato, tra il 40% e 50% dei casi, e non si è modificato nel corso degli ultimi anni nonostante i progressi ottenuti nel trattamento delle sindromi coronariche acute. Recentemente nella pratica clinica si è sempre più diffuso il ricorso all’ECMO (Venoarterial Extracorporeal Membrane Oxygenation), che fornisce un supporto sia circolatorio che respiratorio al paziente. L’efficacia e la sicurezza di questa procedura, tuttavia, non è stata studiata in un trial randomizzato di ampie dimensioni[1]Becher PM, Schrage B, Sinning CR, et al. Venoarterial extracorporeal membrane oxygenation for cardiopulmonary support. Circulation 2018;138:2298-2300.
Lo studio in esame
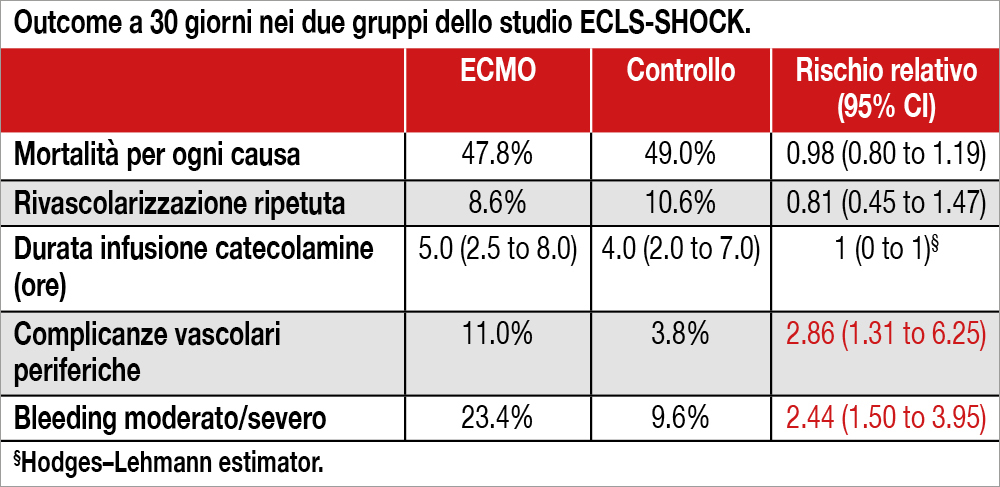
Lo studio ECLS-SHOCK (eseguito prevalentemente in centri tedeschi) ha coinvolto 417 pazienti, di cui 209 nel gruppo ECMO e 208 nel gruppo controllo. La diagnosi di shock cardiogeno doveva includere, oltre ai ben noti parametri clinici (ipotensione, oliguria, segni di alterata perfusione d’organo) anche la determinazione del lattato arterioso che doveva essere >3 mmol/L. L’età media era di 62 anni, due terzi dei pazienti avevano uno STEMI e un terzo NSTEMI; la mediana del lattato arterioso era 6.8 mmol/L. Il 78% dei pazienti aveva avuto un arresto cardiaco ed era stato rianimato. Veniva eseguita una PCI della lesione culprit nella quasi totalità dei pazienti e inserito l’ECMO (nei pazienti del braccio ad esso randomizzato) in sala di Emodinamica prevalentemente dopo la PCI. L’endpoint primario (morte per ogni causa a 30 giorni) è avvenuta in 100 dei 209 pazienti (47.8%) del gruppo ECMO e in 102 dei 208 pazienti (49.0%) del gruppo controllo (rishio relativo 0.98; 95% confidence interval [CI], 0.80 to 1.19; p=0.81). L’endpoint di safety (bleeding moderato severo – BARC 3-5) è stato osservato nel 23.4% dei pazienti del gruppo ECMO e nel 9.6% del gruppo controllo (rischio relativo 2.44; 95% CI, 1.50-3.95), mentre le complicanze periferiche si sono riscontrate nell’11.0% e 3.8%, rispettivamente (rischio relativo 2.86; 95% CI, 1.31- 6.25).
Take home message
Nei pazienti con infarto acuto complicato da shock cardiogeno e sottoposti a rivascolarizzazione precoce, il rischio di morte per ogni causa a 30 giorni non è stato inferiore nei pazienti sottoposti a ECMO rispetto a quelli in sola terapia medica.
Interpretazione dei dati
Lo studio è stato presentato al recente congresso ESC e segue la linea di studi, coordinati da Holger Thiele, su questa patologia ad altissimo rischio clinico la cui prognosi rimane gravissima a breve termine. L’ECMO è stato sempre più utilizzato, quale supporto circolatorio meccanico negli ultimi anni in questi pazienti, il suo uso favorito dalla disponibilità di cannule di calibro tale da permetterne l’introduzione per via percutanea e dai dati di un precedente studio randomizzato dello stesso gruppo che aveva mostrato l’inefficacia della contropulsazione aortica in questa condizione clinica[2]Thiele H, Zeymer U, Neumann F-J, et al. Intraaortic balloon support for myocardial infarction with cardiogenic shock. N Engl J Med 2012; 367:1287-96. Tra le possibili cause del risultato deludente dello studio, gli Autori citano l’alto tasso di complicanze riscontrato nel gruppo ECMO: nonostante siano disponibili cannule e dispositivi di sempre minor calibro, il sanguinamento è tuttora presente in un ampio numero di pazienti e l’ischemia acuta dell’arto inferiore è una evenienza ancora frequente. Non è da dimenticare inoltre il fatto che l’ECMO è un supporto circolatorio che comporta un aumento del post-carico, in quanto il sangue viene reintrodotto nel circolo arterioso per via retrograda. L’efficacia di una strategia di impiego di ECMO in associazione con Impella per ridurre l’afteroload (ECPELLA) è oggetto di uno studio randomizzato tuttora in corso (REVERSE trial). Nonostante i risultati deludenti di questo trial, le recenti Linee Guida ESC 2023 sulle sindromi coronariche acute assegnano una classe di raccomandazione IIb all’uso dell’ECMO nei pazienti in shock cardiogeno, mentre resta la classe III per l’utilizzo del contropulsatore aortico in assenza di complicanze meccaniche[3]Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Aug 25:ehad191. doi:10.1093/eurheartj/ehad191.
Bibliografia[+]
| ↑1 | Becher PM, Schrage B, Sinning CR, et al. Venoarterial extracorporeal membrane oxygenation for cardiopulmonary support. Circulation 2018;138:2298-2300 |
|---|---|
| ↑2 | Thiele H, Zeymer U, Neumann F-J, et al. Intraaortic balloon support for myocardial infarction with cardiogenic shock. N Engl J Med 2012; 367:1287-96 |
| ↑3 | Byrne RA, Rossello X, Coughlan JJ, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023 Aug 25:ehad191. doi:10.1093/eurheartj/ehad191 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

