Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Lo shock cardiogeno è una complicanza molto temibile dell’infarto miocardico, tuttora gravata da una mortalità del 40-50%. I sistemi di assistenza circolatoria, come l’ECMO, determinano un aumento del post-carico del ventricolo sinistro e non hanno mostrato sinora alcun beneficio clinico e un aumento delle complicanze[1]Thiele H, Zeymer U, Akin I, et al. Extracorporeal life support in infarct-related cardiogenic shock. N Engl J Med 2023; 389:1286–97., mentre i sistemi di assistenza tramite pompa microassiale effettuano un “unloading” del ventricolo sinistro: il loro uso è stato associato a una riduzione della mortalità a 6 mesi rispetto alla terapia standard[2]Møller JE, Engstrøm T, Jensen LO, et al. Microaxial flow pump or standard care in infarct-related cardiogenic shock.N Engl J Med 2024 390:1382–93.. Tuttavia, non è chiaro se l’impatto clinico dipenda effettivamente dalla tipologia di assistenza praticata, oppure dalla selezione dei pazienti da sottoporre a tale trattamento.
Lo studio in esame
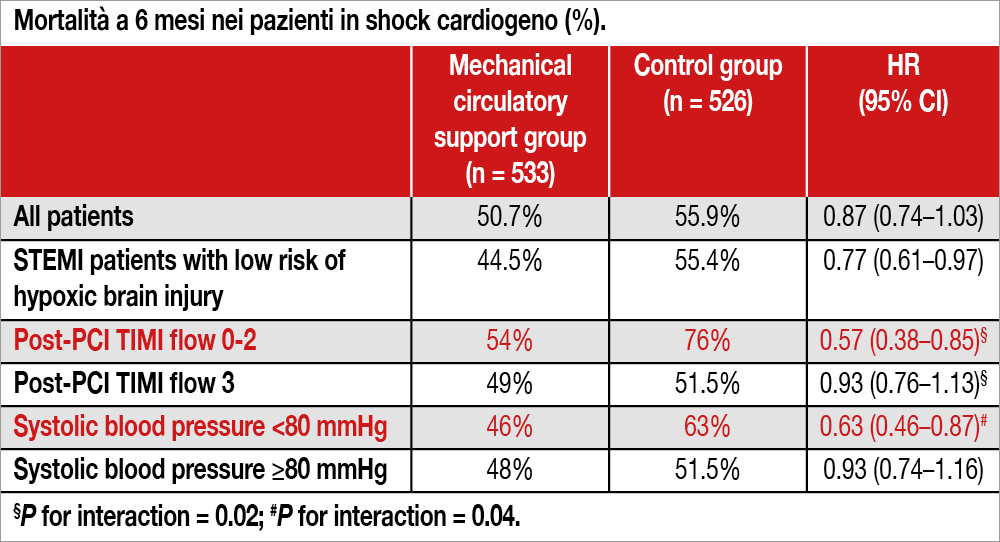
Lo studio consiste in una meta-analisi di 9 trial randomizzati, di cui 4 hanno utilizzato ECMO come supporto circolatorio (n=611) e 5 hanno utilizzato sistemi di “unloading” del ventricolo sinistro (n=503). L’età mediana era 65 anni, 80% erano maschi, 81% STEMI, 64% infarti anteriori, con valori di lattato ≥5.5 mmol/L nel 56% dei casi. Un arresto cardiaco risuscitato prima dell’inclusione negli studi era presente nel 51.5% dei pazienti. La quasi totalità dei pazienti sono stati rivascolarizzati con PCI (95%), l’1.5% con bypass aortocoronarico e il 3.5% non ha ricevuto trattamento interventistico. Alla fine della procedura è stato osservato TIMI 3 nell’83% dei casi. Nell’intera casistica, è stato effettuato ECMO nel 27% dei casi, IMPELLA nel 20% e TANDEM HEART nel 3% dei casi. La mortalità a 6 mesi è stata 50,7% nei pazienti sottoposti a sistemi di supporto e del 55,9% nei pazienti dei gruppi controllo. Globalmente, non vi era differenza nell’outcome primario (mortalità per ogni causa a 6 mesi) tra i pazienti trattati e quelli non trattati (HR 0,87 [95% CI 0,74–1,03]; così pure non vi era alcuna differenza di outcome a vantaggio dei sistemi di supporto sia per ECMO (HR 0.93 [0.75–1.17]; P=0.55) che per “unloading” (HR 0.80 [0.62–1.02]; P=0.075). Considerando solo i pazienti che non avevano avuto arresto cardiaco prima della randomizzazione, oppure un arresto cardiaco di breve durata e quindi a basso rischio di lesioni cerebrali ipossiche, vi era un significativo effetto favorevole sulla mortalità nel gruppo trattato con sistemi di supporto (vedi Tabella). Analogamente, veniva osservato un outcome migliore utilizzando i sistemi di supporto se la PA all’ingresso era <80 mmHg (piuttosto che ≥80 mmHg) e se il flusso TIMI post-PCI era <3 (vedi Tabella). Le complicanze emorragiche (bleeding maggiore: OR 2.64 [95% CI 1.91–3.65]) e vascolari (OR 4.43 [2.37–8.26]) erano più frequenti nei pazienti trattati con sistemi di supporto circolatorio.
Take home message
Nei pazienti con STEMI in shock cardiogeno i sistemi di supporto circolatorio non riducono la mortalità a 6 mesi rispetto al trattamento standard; tuttavia, essi appaiono utili nel paziente con MI senza rischio di lesioni cerebrali. Pertanto, il loro utilizzo dovrebbe essere destinato a pazienti selezionati.
Interpretazione dei dati
Il messaggio principale dello studio è che un beneficio, per quanto limitato, dei sistemi di supporto circolatorio è fornito non tanto da un tipo particolare di supporto (“unloading” versus ECMO) quanto dalla selezione dei pazienti che ne possono beneficiare (in particolare escludendo quelli che, sottoposti a manovre rianimatorie prolungate, possono avere avuto un danno cerebrale che ne pregiudichi il recupero). L’esigenza di un’analisi che tenesse conto dei risultati dei trial in relazione alla popolazione arruolata è sorta dopo la pubblicazione del DanGer Shock trial, il primo e unico studio che abbia dimostrato l’efficacia dell’utilizzo di una pompa microassiale rispetto allo standard of care nel trattamento di questi pazienti[3]Møller JE, Engstrøm T, Jensen LO, et al. Microaxial flow pump or standard care in infarct-related cardiogenic shock.N Engl J Med 2024 390:1382–93.. Da quello studio venivano esclusi i pazienti con un Glasgow coma score <8, cioè quelli con una sofferenza cerebrale già avanzata di tipo ipossico. Questa tipologia di pazienti non rappresentava un criterio di esclusione dagli studi precedenti, che avevano invece dato esito negativo quanto a efficacia dei sistemi di supporto circolatorio. Il miglior risultato ottenuto nei pazienti con ipotensione più marcata (PA sistolica <80 mmHg) riproduce il dato già osservato nello studio DanGer Shock[4]Møller JE, Engstrøm T, Jensen LO, et al. Microaxial flow pump or standard care in infarct-related cardiogenic shock.N Engl J Med 2024 390:1382–93., e conferma che i sistemi di supporto sono meno performanti in presenza di vasocostrizione. Infine, non va dimenticato che l’utilizzo sia di ECMO che, in minor misura, dei sistemi di “unloading”, è associato a frequenti complicanze emorragiche e vascolari secondarie alle dimensioni delle cannule e dei dispositivi da introdurre percutaneamente. Un miglioramento della tecnologia al riguardo, riducendo il rischio di bleeding e di lesioni vascolari, potrebbe ulteriormente migliorare il risultato clinico di questi sistemi di supporto.
Bibliografia[+]
| ↑1 | Thiele H, Zeymer U, Akin I, et al. Extracorporeal life support in infarct-related cardiogenic shock. N Engl J Med 2023; 389:1286–97. |
|---|---|
| ↑2, ↑3 | Møller JE, Engstrøm T, Jensen LO, et al. Microaxial flow pump or standard care in infarct-related cardiogenic shock.N Engl J Med 2024 390:1382–93. |
| ↑4 | Møller JE, Engstrøm T, Jensen LO, et al. Microaxial flow pump or standard care in infarct-related cardiogenic shock.N Engl J Med 2024 390:1382–93. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

