Inquadramento
La TAVI è la modalità di sostituzione valvolare attualmente effettuata con maggiore frequenza nei pazienti con stenosi aortica severa. Tra le tipologie di protesi valvolari utilizzate, quelle “selfexpanding” presentano un comportamento emodinamico superiore rispetto alle protesi “balloon-expandable”[1] Mosleh W, Amer MR, Joshi S, et al. Comparative outcomes of balloon-expandables 3 versus self-expanding evolut bioprostheses for transcatheter aortic valve implantation. Am J Cardiol 2019; 124: 1621-9.. Queste differenze giocano un ruolo importante, particolarmente quando l’annulus aortico è piccolo, evenienza che si verifica in circa un terzo dei pazienti, più frequentemente se di sesso femminile[2]Leone PP, Regazzoli D, Pagnesi M, et al. Predictors and clinical impact of prosthesis-patient mismatch after selfexpandable TAVR in small annuli. JACC Cardiovasc Interv 2021; 14: 1218-28.. Tuttavia, non esistono ampi studi di confronto diretto tra i due tipi di valvole utilizzate in questa tipologia di pazienti.
Lo studio in esame
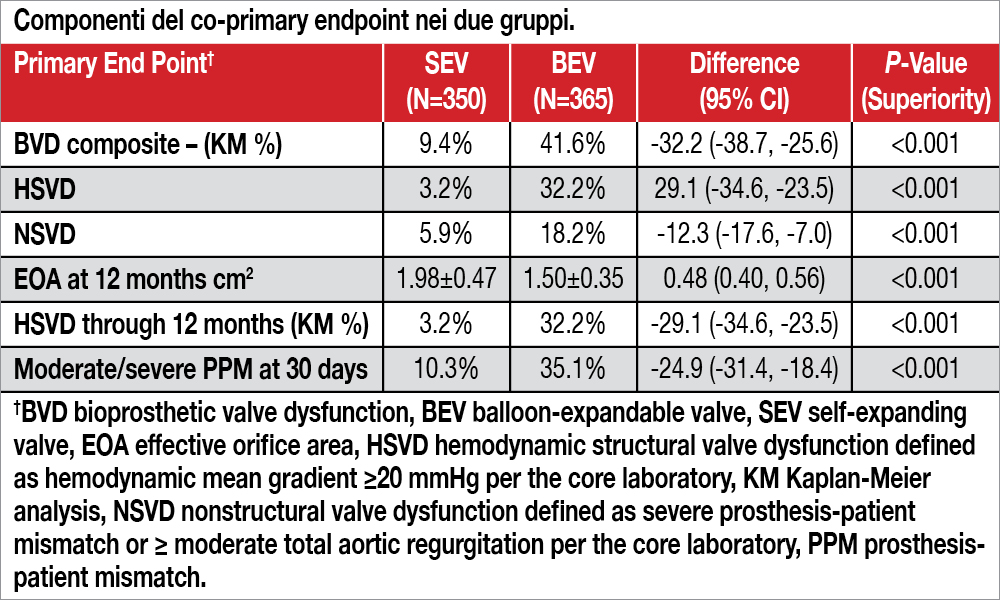
Sono stati inclusi nello studio internazionale SMART (cui hanno partecipato tre centri italiani: Pisa, Verona, Bologna) pazienti (età media 80 anni, 87% di sesso femminile, STS-PROM score medio 3.3%) con stenosi aortica severa (anche con bicuspidia) e un’area valvolare aortica di 430 mm2 o meno all’angio-TC, randomizzati a protesi “self-expanding” (SEV) Evolut PRO/ PRO+/FX, Medtronic, sponsor dello studio (n=361) o a protesi “balloon-expandable” (BEV) SAPIEN 3/3 Ultra, Edwards Lifesciences (n=355). Lo studio aveva due endpoint primari, uno clinico e uno emodinamico. Quello clinico era un composito di morte, stroke invalidante, ospedalizzazione per scompenso, per il quale era attesa un’incidenza del 16% nei due gruppi, valutando le differenze secondo un criterio di non-inferiorità che aveva un margine massimo di 8 punti percentuali. Tale endpoint si è verificato nel 9.4% del gruppo SEV e nel 10.6% del gruppo BEV (differenza, −1.2 punti percentuali; 90% CI, −4.9 a 2.5; P<0.001 for noninferiority; hazard ratio, 0.90; 95% CI, 0.56 -1.43). Non vi era differenza neppure tra le singole componenti dell’endpoint clinico: mortalità 5.1% versus 5.9%, stroke invalidante 3.1% versus 2.6%, riospedalizzazione per scompenso 3.8% versus 3.5%. Il secondo primary endpoint (valutato secondo un criterio di superiorità di SEV rispetto a BEV) riguardava la disfunzione della bioprotesi, distinta in strutturale (gradiente transvalvolare ≥20 mm Hg a un mese dall’intervento) e non-strutturale (severo “mismatch” protesi/paziente, cioè un’area orifiziale di 0.65 cm2/m2 per BMI sino a 30, 0.55 cm2/m2 per BMI >30 oppure presenza di insufficienza aortica almeno moderata, trombosi o endocardite della protesi). Esso si è verificato nel 9.4% del gruppo SEV e nel 41.6% del gruppo BEV (differenza, −32.2 punti percentuali; 95% CI, −38.7 a −25.6; P<0.001). Le varie componenti di questo “co-primary endpoint” e altri endpoint secondari sono riportati nella Tabella. Per quanto riguardava la safety procedurale non si sono osservate differenze tra i due gruppi, tranne che per la necessità di impianto di PM a 30 giorni (maggiore per SEV rispetto a BEV: 12.1% versus 7.8%, hazard ratio, 1.61; 95% CI, 0.98 – 2.65).
Take home messsage
Tra i pazienti con stenosi aortica severa e annulus aortico piccolo, sottoposti a TAVI, l’outcome clinico a 1 anno non è risultato differente tra pazienti in cui era stata impiantata una protesi BEV rispetto a una protesi SEV. Tuttavia, quest’ultimo tipo di protesi si associava a una minore incidenza di disfunzione protesica.
Interpretazione dei dati
I risultati dello studio sono apparentemente contrastanti. Da un lato infatti il primo endpoint principale, su base clinica, non ha mostrato alcuna differenza a 12 mesi per quanto riguardava un composito di mortalità, stroke invalidante, riospedalizzazione per scompenso; al contrario il secondo endpoint principale, su base emodinamica, ha evidenziato una netta superiorità delle valvole “self-expanding” (SEV) rispetto a quelle “balloon-expandable” (BEV). Infatti, la disfunzione della protesi sia strutturale (elevato gradiente trans-protesico a 30 giorni) che non strutturale (severo “mismatch” protesi/paziente) è risultata essere superiore nel gruppo BEV. Alcuni dati della letteratura indicano che la presenza di disfunzione protesica si associa nel tempo a un numero elevato di complicanze cliniche: in particolare, un’entità del gradiente transprotesico superiore a 22.5 mmHg comporta un significativo aumento della mortalità a 5 anni[3]Playford D, Stewart S, Celermajer D, et al. Poor survival with impaired valvular hemodynamics after aortic valve replacement: the National Echo Database Australia study. J Am Soc Echocardiogr … Continua a leggere. È stata inoltre segnalata un’associazione tra severo “mismatch” protesi/paziente e aumentata mortalità a distanza[4]Sá MP, Jacquemyn X, Van den Eynde J, et al. Impact of prosthesis-patient mismatch after transcatheter aortic valve replacement: meta-analysis of Kaplan-Meierderived individual patient data. JACC … Continua a leggere. Lo studio in esame prevede un ulteriore follow-up clinico a 5 anni per verificare se effettivamente queste migliori performance delle protesi valvolari SEV determinino anche un migliore decorso clinico. Va segnalato che un’evoluzione clinicamente sfavorevole a lungo termine, ipotizzata dagli autori dello studio SMART per le protesi BEV, non è condivisa da molti esperti di interventistica strutturale: perciò i dati a un follow-up più prolungato sono attesi con molto interesse.
Bibliografia[+]
| ↑1 | Mosleh W, Amer MR, Joshi S, et al. Comparative outcomes of balloon-expandables 3 versus self-expanding evolut bioprostheses for transcatheter aortic valve implantation. Am J Cardiol 2019; 124: 1621-9. |
|---|---|
| ↑2 | Leone PP, Regazzoli D, Pagnesi M, et al. Predictors and clinical impact of prosthesis-patient mismatch after selfexpandable TAVR in small annuli. JACC Cardiovasc Interv 2021; 14: 1218-28. |
| ↑3 | Playford D, Stewart S, Celermajer D, et al. Poor survival with impaired valvular hemodynamics after aortic valve replacement: the National Echo Database Australia study. J Am Soc Echocardiogr 2020;33: 1077-1086.e1. |
| ↑4 | Sá MP, Jacquemyn X, Van den Eynde J, et al. Impact of prosthesis-patient mismatch after transcatheter aortic valve replacement: meta-analysis of Kaplan-Meierderived individual patient data. JACC Cardiovasc Imaging 2023; 16: 298-310. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

