Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Nei pazienti con sindrome coronarica acuta (ACS) una ampia serie di studi ha dimostrato la fattibilità di una strategia di de-escalation basata su un utilizzo iniziale di una doppia terapia antipiastrinica (DAPT) composta da ASA e da un inibitore del recettore P2Y12 potente come ticagrelor e successivo “switch” ad una DAPT composta da ASA e clopidogrel, un inibitore del recettore P2Y12 meno potente di ticagrelor. Alla base di questa strategia vi è la dimostrazione di una riduzione progressiva del rischio ischemico passando dalla fase acuta e subacuta (il primo mese) alla fase cronica, nella quale il rischio emorragico diviene preminente sul rischio ischemico[1]Rodriguez F, Harrington RA. Management of antithrombotic therapy after acute coronary syndromes. N Engl J Med. 2021; 384:452-460. doi:10.1056/NEJMra1607714.. Lo studio TALOS-AMI ha dimostrato la maggiore sicurezza e pari efficacia di questa strategia rispetto ad una DAPT standard protratta sino a 12 mesi e composta da ASA e ticagrelor[2]Kim CJ, Park MW, Kim MC, et al. TALOS-AMI Investigators. Unguided de-escalation from ticagrelor to clopidogrel in stabilised patients with acute myocardial infarction undergoing percutaneous coronary … Continua a leggere. Tuttavia manca la dimostrazione che analoghi risultati possano essere ottenuti in una popolazione ad elevato rischio ischemico.
Lo studio in esame
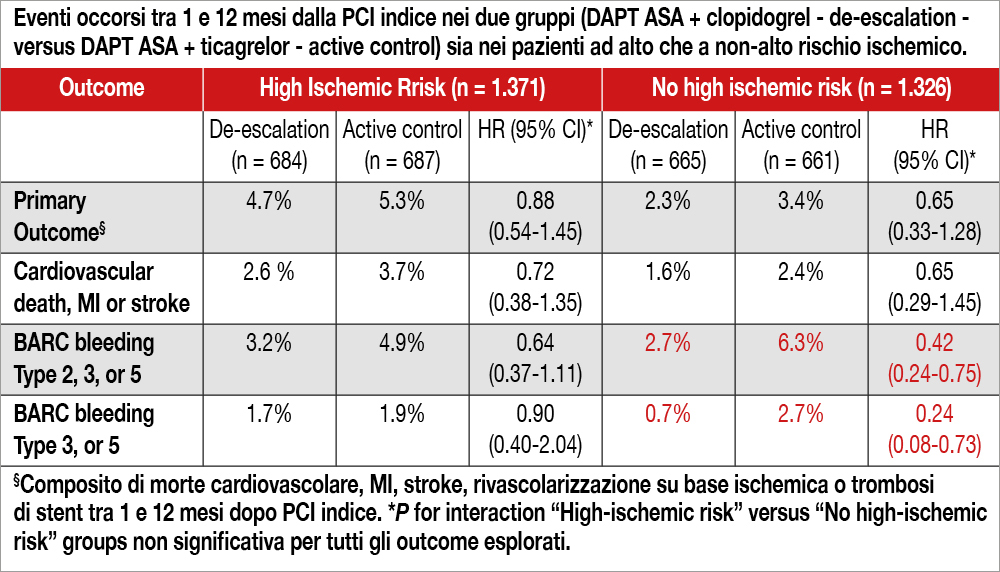
È questa una analisi post-hoc del TALOS-AMI (Ticagrelor vs Clopidogrel in Stabilized Patients With Acute Myocardial Infarction) trial, uno studio che ha randomizzato 2.697 pazienti con infarto miocardico (MI), tutti trattati per il primo mese con DAPT a base di ASA e ticagrelor ben tollerata e senza eventi ischemici ed emorragici, a proseguire tale terapia oppure a “switchare” ad una DAPT composta da ASA e clopidogrel. In questa analisi sono stati considerati 1.371 pazienti ad alto rischio ischemico, 687 in DAPT con ASA e ticagrelor e 684 in DAPT con ASA e clopidogrel. Il rischio ischemico è stato considerato elevato se era presente almeno una delle seguenti caratteristiche cliniche o angiografiche: diabete mellito in trattamento, nefropatia cronica (e GFR<60 mL/min/1.73m2, PCI multivasale, almeno 3 lesioni trattate, lunghezza totale degli stent >60 mm, almeno 3 stent impiantati, PCI del tronco comune, PCI di biforcazione con due stent. L’outcome primario ischemico era un composito di morte cardiovascolare, MI, stroke ischemico, rivascolarizzazione su base ischemica o trombosi dello stent da 1 a 12 mesi dopo la PCI indice. L’outcome secondario chiave era rappresentato dal bleeding secondo BARC 2,3 o 5. I pazienti ad alto rischio ischemico raggiungevano l’endpoint primario più frequentemente dei pazienti non ad alto rischio ischemico (5.0% vs 2.8%, HR, 1.74; 95%CI, 1.15-2.63; P=.01). Non vi era differenza tra le due strategie di DAPT per quanto riguardava l’outcome primario sia nel gruppo ad alto rischio ischemico che nel gruppo non ad alto rischio ischemico (vedi Tabella) mentre il bleeding (BARC 2, 3, o 5) risultava significativamente minore nei pazienti sottoposti a de-escalation solo nel gruppo a non alto rischio ischemico. La P for interaction (tra pazienti ad alto e a non-alto rischio ischemico) risultava non significativa per tutti gli endpoint considerati (vedi Tabella).
Take home message
In pazienti stabilizzati dopo infarto miocardico acuto, una strategia di de-escalation non guidata da DAPT composta da ASA e ticagrelor a DAPT composta da ASA e clopidogrel ha dimostrato pari efficacia ma minor rischio emorragico rispetto ad una DAPT di 12 mesi con ASA e ticagrelor, indipendentemente dal rischio ischemico dei pazienti.
Interpretazione dei dati
L’obbiezione più comune rivolta alle strategie di “short DAPT” o di “de-escalation” risiede nel dubbio che siano poco efficaci nel proteggere il paziente da recidive ischemiche. Particolarmente esposti a tali recidive sono i pazienti nei quali la presenza di alcune variabili cliniche (diabete, infarto pregresso, vasculopatia periferica associata) e procedurali (PCI complesse) comporta la persistenza di un rischio ischemico elevato. Il passaggio ad esempio da “short DAPT” a monoterapia con ASA o clopidogrel ha causato infatti un aumento di eventi trombotici nello studio SMART-DATE[3]Hahn JY, Song YB, Oh JH, et al. SMART-DATE Investigators. 6-Month versus 12-month or longer dual antiplatelet therapy after percutaneous coronary intervention in patients with acute coronary syndrome … Continua a leggere e nello STOPDAPT-2 ACS[4]Watanabe H, Morimoto T, Natsuaki M, et al. STOPDAPT-2 ACS Investigators. Comparison of clopidogrel monotherapy after 1 to 2 months of dual antiplatelet therapy with 12 months of dual antiplatelet … Continua a leggere. Questo timore non appare giustificato” alla luce dello studio TALOS-AMI, nel quale è stata testata tuttavia una strategia di 12 mesi di DAPT, che prevedeva, a partire dal secondo mese dall’evento acuto, lo “switch” da un inibitore potente del recettore P2Y12 come ticagrelor, a clopidogrel. Il braccio di controllo era rappresentato da una DAPT standard sino al dodicesimo mese composta da ticagrelor e ASA. I dati, qui esposti, sono favorevoli a questa strategia di “de-escalation” anche in presenza di un rischio ischemico elevato. Tuttavia, come rilevano gli autori, questa analisi non era pre- specificata e quindi i pazienti non venivano inizialmente randomizzati in base al rischio ischemico; ne consegue che alcune variabili erano differentemente distribuite tra i due gruppi (pur non raggiungendo tali differenze la significatività statistica per alcuna variabile). Inoltre la potenza dello studio è limitata in quanto circa la metà della casistica arruolata per lo studio aveva un rischio ischemico elevato. I risultati vanno quindi considerati “generatori di ipotesi” che attendono conferma da studi ad hoc
Bibliografia[+]
| ↑1 | Rodriguez F, Harrington RA. Management of antithrombotic therapy after acute coronary syndromes. N Engl J Med. 2021; 384:452-460. doi:10.1056/NEJMra1607714. |
|---|---|
| ↑2 | Kim CJ, Park MW, Kim MC, et al. TALOS-AMI Investigators. Unguided de-escalation from ticagrelor to clopidogrel in stabilised patients with acute myocardial infarction undergoing percutaneous coronary intervention (TALOS-AMI): an investigator-initiated, open-label, multicentre, non-inferiority, randomised trial. Lancet. 2021; 398:1305-1316. doi:10.1016/S0140-6736(21)01445-8. |
| ↑3 | Hahn JY, Song YB, Oh JH, et al. SMART-DATE Investigators. 6-Month versus 12-month or longer dual antiplatelet therapy after percutaneous coronary intervention in patients with acute coronary syndrome (SMART-DATE): a randomised, openlabel, non-inferiority trial. Lancet. 2018; 391:1274-1284. doi:10.1016/S0140-6736(18) 30493-8. |
| ↑4 | Watanabe H, Morimoto T, Natsuaki M, et al. STOPDAPT-2 ACS Investigators. Comparison of clopidogrel monotherapy after 1 to 2 months of dual antiplatelet therapy with 12 months of dual antiplatelet therapy in patients with acute coronary syndrome: the STOPDAPT-2 ACS randomized clinical trial. JAMA Cardiol. 2022;7: 407-417. doi:10.1001/jamacardio.2021.5244. |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

