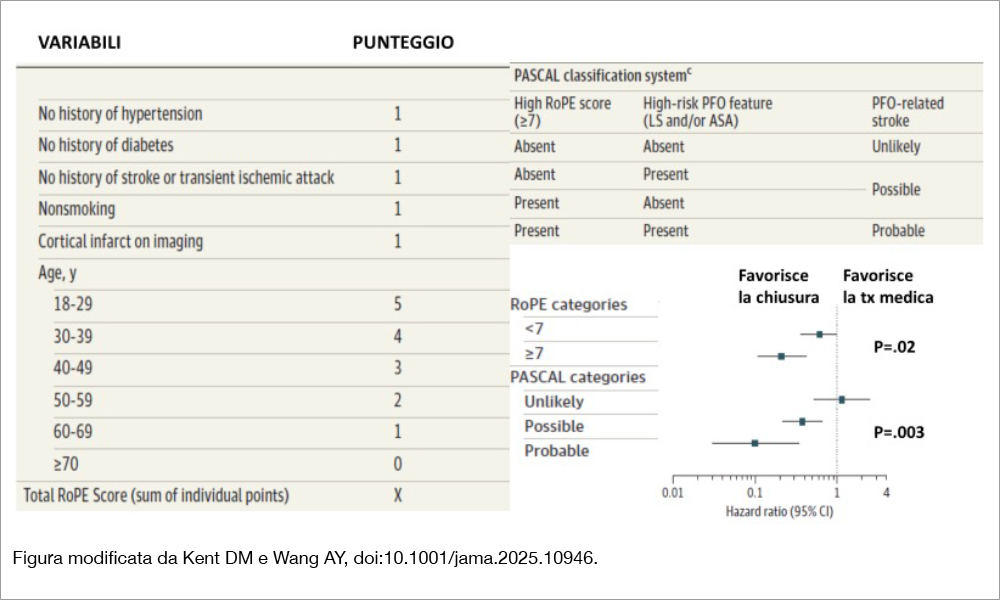
Un forame ovale pervio (PFO) è presente in circa il 25% degli individui. Ciò nonostante è ritenuto una causa non infrequente di stroke criptogenetico. Nei pazienti affetti da tale tipologia di stroke la presenza di PFO è riscontrata nel 50% dei casi e può essere causa di una embolia paradossa. È stato calcolato che un PFO può essere la causa dell’80% degli stroke criptogenetici nei pazienti con età inferiore ai 55 anni, mentre tale percentuale si riduce al 52% nei pazienti più anziani[1]Saver JL, Mattle HP, Thaler D. Patent foramen ovale closure versus medical therapy for cryptogenic ischemic stroke: a topical review. Stroke. 2018;49:1541-1548. doi:10.1161/STROKEAHA.117.018153. Globalmente, tale causa sarebbe alla base del 5% di tutti gli stroke ischemici, salendo al 10% nei pazienti giovani e di mezzà età. La diagnosi di stroke associato a PFO richiede l’esclusione di ogni altra causa nota (stroke criptogenetico), la presenza di PFO all’indagine diagnostica e la connessione causale tra stroke ed evento ischemico cerebrale. Bisogna innanzitutto escludere una origine embolica dagli atri generalmente per fibrillazione atriale (causa di circa il 28% degli stroke ischemici), una patologia dei piccoli vasi (24%), una patologia delle arterie principali (23%) ed altre forme più rare di vasculite (5%)[2]Prabhakaran S, Messé SR, Kleindorfer D, et al. Cryptogenic stroke: contemporary trends,treatments, and outcomes in the United States.Neurol Clin Pract. 2020;10(5):396-405. … Continua a leggere. Nel restante 20% dei casi, l’origine è oscura (stroke criptogenetico). La probabilità che uno stroke criptogenetico origini da un PFO può essere valutata sulla base del Risk of Paradoxical Embolism (RoPE) score (Figura), sviluppato dall’analisi di database che includevano globalmente oltre 3.000 pazienti con stroke criptogenetico[3]Kent DM, Ruthazer R,Weimar C, et al. An index to identify stroke-related vs incidental patent foramen ovale in cryptogenic stroke. Neurology.2013;81:619-6 doi:10.1212/WNL.0b013e3182a08d59. Esso include 6 variabili (età, storia di stroke/TIA, diabete, ipertensione, fumo, infarto corticale all’imaging), variando in punteggio da 0 a 10. Nei pazienti con score <3, la prevalenza di PFO è stata del 23%, simile a quella della popolazione generale, mentre se lo score era 9 o 10 la prevalenza era del 77%, un dato che aumenta la probabilità di una embolia paradossa da PFO. La limitazione principale di questo score è la sua modesta capacità di predire una recidiva di stroke, stimata attorno al 2% nei pazienti con RoPE score di 9 o10.
Per ovviare a questo limite e migliorarne la capacità predittiva è stato proposto di affiancare al RoPE score la classificazione PASCAL (PFO-Associated Stroke Causal Likelihood) che include anche i dati dell’imaging ecocardiografico, come la presenza di ampio shunt (>20 bolle in atrio sinistro all’eco transesofageo) e/o di un aneurisma del setto interatriale (almeno 10 mm) come mostra la Figura. Un PFO è considerato possibile quando vi è un punteggio RoPE di almeno 7 punti in assenza del dato di imaging (o viceversa), probabile se entrambi i criteri RoPE e di imaging sono soddisfatti, improbabile se non vi sono nè i criteri RoPE nè quelli della classificazione PASCAL. La chiusura di PFO è effettuata inserendo un dispositivo di chiusura per via percutanea attraverso una vena femorale. Una metaanalisi di 6 studi (3560 pazienti) ha mostrato un minor rischio di recidiva con l’intervento (2%) che con la terapia medica (4.6%, rischio relativo 0.44 [95% CI, 0.23-0.85]; P=.01) ad un follow-up mediano di 57 mesi[4]Pristipino C, Sievert H, D’Ascenzo F, et al. Evidence Synthesis Team; Eapci Scientific Documents and Initiatives Committee; International Experts. European position paper on the management of … Continua a leggere. Utilizzando la classificazione PASCAL (Figura, pannello in basso a destra), tra i pazienti in cui l’origine dello stroke era definita come “probabile” la recidiva di stroke si riduceva del 90% con la chiusura del PFO (HR, 0.10 [95%CI, 0.03-0.35]; con una riduzione del rischio assoluto del 2.1% [95%CI,0.9%-3.4%], mentre se l’origine è possibile la riduzione è del 62% (HR, 0.38 [95%CI, 0.22-0.65]). Alcontrario, se I pazienti sono nella categoria a origine “improbabile” la chiusura del PFO non offre alcun vantaggio (HR, 1.14 [95%CI, 0.53-2.46])[5]Kent DM, Saver JL, Kasner SE, et al. Heterogeneity of treatment effects in an analysis of pooled individual patient data from randomized trials of device closure of patent foramen ovale after stroke. … Continua a leggere. Non va tuttavia trascurato il rischio di complicanze della procedura: insorgenza di fibrillazione atriale (3.7%), complicanze vascolari che richiedono la chirurgia (3.0%), tamponamento cardiaco/perforazione (0.5%), pneumotorace /emotorace (0.1%), e mortalità (0.3%). Tuttavia il rischio di complicanze appare maggiore nel gruppo a origine “improbabile” che negli altri due gruppi. Tra le Linee Guida più recenti quelle SCAI (Society for Cardiovascular Angiography & Interventions) del 2022 raccomandano la chiusura di PFO nei pazienti sino a 60 anni con RoPE score ≥7[6]Kavinsky CJ, Szerlip M, Goldsweig AM, et al. SCAI Guidelines for the Management of Patent Foramen Ovale. J Soc Cardiovasc Angiogr Interv. 2022 May 19;1:100039. doi:10.1016/j.jscai.2022.100039. … Continua a leggere. Esistono poche evidenze sulla efficacia del trattamento di chiusura del PFO nel paziente anziano; maggiori informazioni saranno fornite da un trial attualmente in corso[7]Mas JLCG. PFO closure, oral anticoagulants or antiplatelet therapy after PFO-associated stroke in patients aged 60 to 80 years (CLOSE-2) [NCT05387954]. ClinicalTrials.gov. Published February 1, 2025.
Bibliografia[+]
| ↑1 | Saver JL, Mattle HP, Thaler D. Patent foramen ovale closure versus medical therapy for cryptogenic ischemic stroke: a topical review. Stroke. 2018;49:1541-1548. doi:10.1161/STROKEAHA.117.018153 |
|---|---|
| ↑2 | Prabhakaran S, Messé SR, Kleindorfer D, et al. Cryptogenic stroke: contemporary trends,treatments, and outcomes in the United States.Neurol Clin Pract. 2020;10(5):396-405. doi:10.1212/CPJ.0000000000000736. |
| ↑3 | Kent DM, Ruthazer R,Weimar C, et al. An index to identify stroke-related vs incidental patent foramen ovale in cryptogenic stroke. Neurology.2013;81:619-6 doi:10.1212/WNL.0b013e3182a08d59 |
| ↑4 | Pristipino C, Sievert H, D’Ascenzo F, et al. Evidence Synthesis Team; Eapci Scientific Documents and Initiatives Committee; International Experts. European position paper on the management of patients with patent foramen ovale: general approach and left circulation thromboembolism. Eur Heart J. 2019;40:3182-3195. doi:10.1093/eurheartj/ehy649 |
| ↑5 | Kent DM, Saver JL, Kasner SE, et al. Heterogeneity of treatment effects in an analysis of pooled individual patient data from randomized trials of device closure of patent foramen ovale after stroke. JAMA. 2021;326(22):2277-2286. doi:10.1001/jama.2021.20956 |
| ↑6 | Kavinsky CJ, Szerlip M, Goldsweig AM, et al. SCAI Guidelines for the Management of Patent Foramen Ovale. J Soc Cardiovasc Angiogr Interv. 2022 May 19;1:100039. doi:10.1016/j.jscai.2022.100039. eCollection 2022 Jul-Aug |
| ↑7 | Mas JLCG. PFO closure, oral anticoagulants or antiplatelet therapy after PFO-associated stroke in patients aged 60 to 80 years (CLOSE-2) [NCT05387954]. ClinicalTrials.gov. Published February 1, 2025 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

