Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Con l’affermarsi della TAVI nel trattamento della stenosi aortica severa e la sua estensione a pazienti con rischio chirurgico intermedio o basso e a età inferiore rispetto alle fasi iniziali di questa procedura, è diventato sempre più importante verificare la tenuta delle protesi nel tempo (“durability”). Inoltre, le prime TAVI venivano eseguite in anestesia generale (GA) mentre in tempi più recenti prevale l’opzione della sedazione cosciente (CS). Il SOLVE trial (comparison of secOnd-generation seLfexpandable vs balloon-expandable Valves and gEneral vs local anesthesia in Transcatheter Aortic Valve Implantation) ha confrontato l’outcome di pazienti TAVI a rischio intermedio-alto, trattati per via femorale, sottoposti a impianto di protesi “selfexpanding” versus protesi “balloon-expandable” così come ha valutato gli effetti di una CS versus una GA. I dati a 1 anno sono già stati presentati[1]Feistritzer HJ, Kurz T, Stachel G, et al. Impact of anesthesia strategy and valve type on clinical outcomes after transcatheter aortic valve replacement. J Am Coll Cardiol. 2021;77:2204–2215., ma è evidente come sia necessario un follow-up più lungo per esaminare i risultati relativi alla “durability” delle differenti protesi.
Lo studio in esame
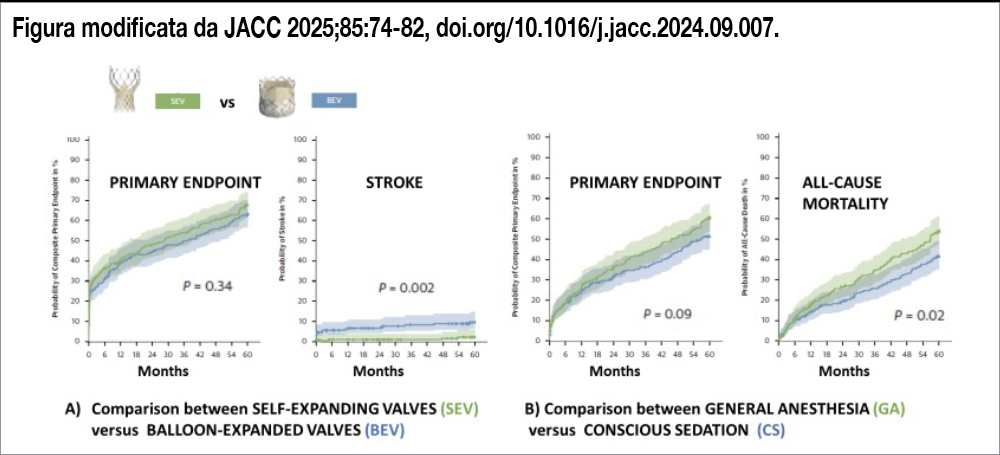
Lo studio (con disegno fattoriale 2×2, condotto in 7 centri tedeschi) ha randomizzato 447 pazienti con età ≥75 anni, sottoposti a TAVI per stenosi aortica severa. L’età media era 82 anni, la metà erano maschi, la presenza di fibrillazione atriale si riscontrava nel 45% dei casi e lo score mediano STS era 5. Per il confronto tra le protesi valvolari (BEV vs SEV) l’endpoint primario predefinito (composito di mortalità per ogni causa, stroke, leak paravalvolare moderato o severo, necessità di impianto PM) a 5 anni di follow-up è stato non significativamente differente nei due gruppi (67.7% nel gruppo SEV e 63.4% nel gruppo BEV, HR: 0.89; 95% CI 0.70- 1.13; P=0.34). Tuttavia, l’incidenza di stroke è stata minore nel gruppo SEV (2.2% vs 9.6%; HR: 4.84; 95% CI: 1.65- 14.18; P=0.002, vedi Figura, pannello A). Un’analisi stratificata per dimensioni dell’anulus aortico ha mostrato una riduzione significativa dello stroke solo nei pazienti con anulus piccolo (≤430 mm2, 1.0% vs 12.7%; P=0.002;), ma non in quelli con anulus >430 mm2 (4.1% vs 6.4%; P=0.36). Anche l’incidenza di infarto miocardico è stata minore nei pazienti SEV (0% vs 2.5%, (P=0.02). Il leak paravalvolare non è risultato significativamente differente tra i due gruppi, anche se numericamente inferiore nel gruppo BEV (5.8% vs 9%, HR 0.64, 95% CI 0.30-1.37) Il gradiente trans-protesico mediano allʼecocardiogramma (eseguito a 5 anni solo nel 15% dei pazienti) è stato inferiore nei pazienti SEV rispetto ai pazienti BEV (7 mm Hg vs 11 mm Hg; P=0.005). La qualità della vita non è risultata differente nei due gruppi. Per il confronto tra modalità di anestesia, GA (eseguita con intubazione tracheale e infusione continua di propofol e remifentanil) versus CS (eseguita con infusione continua di propofol, dexmedetomidina o altri anestetici non benzodiazepinici) l’endpoint primario (rappresentato da un composito di mortalità per ogni causa, stroke, infarto miocardico, nefropatia acuta) a 5 anni è stato osservato nel 51.4% del gruppo CS e nel 61.3% del gruppo GA (HR: 0.80; 95% CI: 0.62-1.04; P=0.09). Per di più la mortalità per ogni causa è apparsa ridotta nel gruppo CS rispetto a GA (41.5% vs 54.3%; HR: 0.70; 95% CI: 0.53-0.94; P=0.02, vedi Figura, pannello B). Non è stata osservata alcuna differenza tra i due gruppi per quanto riguarda le altre componenti dell’endpoint composito e la qualità di vita.
Take home message
Nei pazienti con stenosi aortica severa, sottoposti a TAVI, non è stata riscontrata alcuna differenza nell’endpoint primario a 5 anni sia nel confronto tra protesi valvolari auto-espandibili e quelle espanse dal pallone, che nel confronto del tipo di anestesia praticato.
Interpretazione dei dati
Leggendo le conclusioni dello studio si ha l’impressione che le strategie confrontate, sia per la tipologia di valvola impiantata che per l’anestesia praticata, siano sostanzialmente simili. Tuttavia, sia per il primo confronto tra protesi SEV e BEV, che per il secondo tra anestesia generale (GA) e sedazione cosciente (CS) del paziente, la lettura di tutti i dati dà rilievi di grande interesse non solo per il cardiologo interventista, ma anche per il clinico. Per quanto riguarda il confronto tra protesi (pur non dimenticando che in presenza di un endpoint primario non significativamente differente tra due gruppi, l’esame dei singoli componenti risulta solo “generatore di ipotesi”) la differenza nell’incidenza di stroke risulta il dato più interessante; l’incidenza nel gruppo BEV (11.6% a 5 anni) risulta più elevata che nello studio PARTNER 3[2]Makkar RR, Thourani VH, Mack MJ, et al. Five year outcomes of transcatheter or surgical aortic valve replacement. N Engl J Med. 2020;382(9):799–809, mentre è minore che nello studio PARTNER 2 che tuttavia aveva arruolato pazienti con STS score più alto. Va notato che nello studio SOLVE-TAVI le differenze nell’incidenza di stroke tra BEV e SEV appare già precocemente ed è significativa già a 1 anno di follow-up. Gli stroke precoci potrebbero essere correlati alla predilatazione dell’anello, eseguita, per i pazienti BEV, nel 40% dei casi, una percentuale più elevata che in precedenti studi. Inoltre, la differenza nell’incidenza di stroke tra protesi BEV e SEV appare evidente in presenza di un anulus piccolo, che è una delle situazioni nelle quali si procede alla dilatazione pre-impianto. Per quanto riguarda il confronto tra tipologie di anestesia, pur in presenza di un endpoint primario non significativamente differente, la differenza di mortalità per ogni causa tra i due gruppi non va ignorata. Una differenza a favore di CS compare a partire dai 6 mesi di follow-up e si amplifica nel tempo. Questa relazione temporale rende altresì problematica unʼanalisi delle potenziali cause: una sottoanalisi dello studio ha permesso di evidenziare un vantaggio prevalentemente nei pazienti fragili, ma risulta difficile spiegare una comparsa tardiva del beneficio in questi pazienti a maggior rischio.
Bibliografia[+]
| ↑1 | Feistritzer HJ, Kurz T, Stachel G, et al. Impact of anesthesia strategy and valve type on clinical outcomes after transcatheter aortic valve replacement. J Am Coll Cardiol. 2021;77:2204–2215. |
|---|---|
| ↑2 | Makkar RR, Thourani VH, Mack MJ, et al. Five year outcomes of transcatheter or surgical aortic valve replacement. N Engl J Med. 2020;382(9):799–809 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

