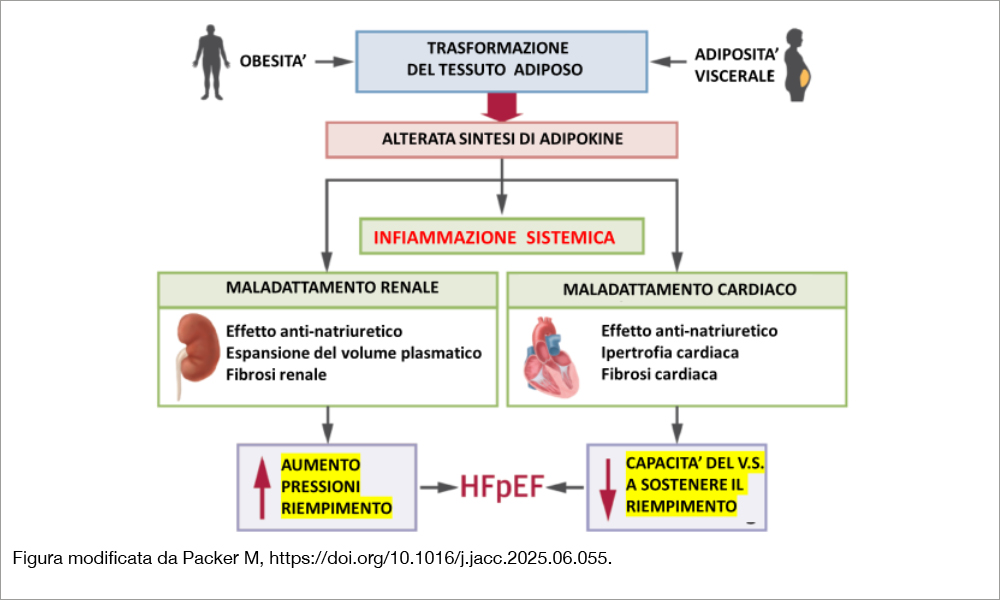
La review sostiene l’ipotesi che la patogenesi dello scompenso a FE conservata (HFpEF) risieda in un eccessivo sviluppo del tessuto adiposo viscerale che subisce una trasformazione disfunzionale che comporta la secrezione di molecole di segnale (adipokine), che causano una infiammazione sistemica e conseguente espansione del volume plasmatico, ipertrofia e fibrosi cardiaca (Figura). Le adipokine sono raggruppate in 3 domini: il primo comprende le adipokine con azione protettiva, secrete dagli adipociti nelle persone magre, mentre sono soppresse quando l’adiposità è eccessiva; il secondo include adipokine cardioprotettive secrete da adipociti in condizioni di obesità per compensare la diminuzione delle adipokine del primo dominio e l’incremento delle adipokine di tipo III. Queste ultime sono secrete in presenza di obesità e soprattutto di obesità viscerale: esse hanno una azione pro-infiammatoria e inducono ipertrofia e fibrosi e hanno effetto antinatriuretico. L’espansione del grasso viscerale quindi trasforma il secretoma degli adipociti che producono molecole che promuovono l’attivazione simpatica a livello splancnico e renale attraverso il sistema renina-angiotensinaaldosterone e conseguente ritenzione di sodio con espansione del volume plasmatico. L’HFpEF è perciò il risultato di uno squilibrio determinato da un’eccessiva adiposità che determina un aumento delle adipokine del terzo dominio e una soppressione di adipokine del primo dominio. Nella review si sottolinea l’importanza del tessuto adiposo viscerale, biologicamente più attivo rispetto al grasso sottocutaneo in quanto esercita maggiori effetti endocrini e paracrini[1]Matsuzawa Y, Shimomura I, Kihara S, Funahashi T. Importance of adipocytokines in obesity-related diseases. Horm Res.2003;60 (Suppl 3):56–59.. Non va dimenticato infatti che tra i pazienti con HFpEF l’obesità (definita come BMI ≥30 kg/m2) è presente nel 60-70% dei casi, mentre un aumento dell’adiposità centrale (definita come rapporto tra circonferenza addominale e altezza ≥0.5) è presente in oltre il 95% dei casi[2]Peikert A, Vaduganathan M, Claggett BL, et al. Near-universal prevalence of central adiposity and its prognostic significance in heart failure with mildly reduced or preserved ejection fraction: the … Continua a leggere. Esiste inoltre una correlazione tra quantità di grasso viscerale ed entità delle manifestazioni cliniche di HFpEF. Questa patologia è più frequente nel sesso femminile, in quanto le donne presentano un aumento sproporzionato delle pressioni di riempimento in conseguenza dell’espansione del volume plasmatico: esse infatti hanno una maggiore rigidità delle pareti ventricolari rispetto agli uomini[3]Packer M, Lam CSP, Lund LH, Maurer MS, Borlaug BA. Characterization of the inflammatory metabolic phenotype of heart failure with a preserved ejection fraction: a hypothesis to explain influence of … Continua a leggere. Inoltre, il tessuto adiposo è più rappresentato nel sesso femminile che in quello maschile. Ne consegue una maggiore vulnerabilità agli squilibri sopra descritti nella secrezione delle adipokine. Il risultato è una infiammazione regionale e sistemica[4]Sorimachi H, Burkhoff D, Verbrugge FH, et al. Obesity, venous capacitance, and venous compliance in heart failure with preserved ejection fraction. Eur J Heart Fail. 2021;23:1648–1658. con distruzione del microcircolo e comparsa di fibrosi miocardica[5]Mohammed SF, Hussain S, Mirzoyev SA, Edwards WD, Maleszewski JJ, Redfield MM. Coronary microvascular rarefaction and myocardial fibrosis in heart failure with preserved ejection fraction. … Continua a leggere e ipertrofia, condizioni che alterano la distensibilità delle pareti ventricolari (Figura). Le linee di evidenza a sostegno di questa ipotesi sono:
- 1) l’obesità è il driver maggiore di HFpEF ottenuta sperimentalmente;
- 2) i cambiamenti che avvengono nell’adiposità viscerale e nelle adipokine circolanti sono osservati anni prima e precedono la diagnosi di HFpEF, ma non di HFrEF;
- 3) l’obesità viscerale è presente in oltre il 95% dei pazienti HFpEF e si correla con la severità della malattia;
- 4) l’obesità e HFpEF mostrano aspetti simili sia molecolari che fisiopatologici e clinici;
- 5) il cambiamento nel profilo delle adipokine è correlato alla severità della malattia;
- 6) gli effetti delle adipokine sulla struttura cardiaca sono quelli che si riscontrano in HFpEF;
- 7) la chirurgia bariatrica o il trattamento medico dell’obesità riducono il grasso viscerale aumentando la secrezione di adipokine del dominio I e diminuendo quelle del dominio III;
- 8) una adiposità eccessiva identifica pazienti che rispondono clinicamente al trattamento raccomandato per HFpEF;
- 9) interventi sperimentali che modulano la secrezione di un certo tipo di adipokine determinano cambiamenti della struttura cardiaca.
Una teoria unificante sulla patogenesi di HFpEF può essere accolta con scetticismo dai ricercatori che pensano che tale condizione clinica può avere una origine eterogenea che coinvolge la patologia coronarica, il diabete, la fibrillazione atriale e la miopatia atriale, le alterazioni del microcircolo, l’infiammazione sistemica e la carenza di peptidi natriuretici. Tuttavia, mancano dati a supporto di queste ipotesi che provengono dall’osservazione che spesso in questi pazienti sono presenti comorbilità, che però possono essere concomitanti ma non hanno provato rilievo patogenetico. I nuovi trattamenti per HFpEF dovrebbero essere tesi non soltanto alla perdita di peso, ma soprattutto a migliorare la biologia del tessuto adiposo disfunzionante che è la base patogenetica di questa patologia.
Bibliografia[+]
| ↑1 | Matsuzawa Y, Shimomura I, Kihara S, Funahashi T. Importance of adipocytokines in obesity-related diseases. Horm Res.2003;60 (Suppl 3):56–59. |
|---|---|
| ↑2 | Peikert A, Vaduganathan M, Claggett BL, et al. Near-universal prevalence of central adiposity and its prognostic significance in heart failure with mildly reduced or preserved ejection fraction: the PARAGON-HF trial. Eur Heart J. 2025:ehaf057. https://doi.org/10.1093/eurheartj/ehaf057 |
| ↑3 | Packer M, Lam CSP, Lund LH, Maurer MS, Borlaug BA. Characterization of the inflammatory metabolic phenotype of heart failure with a preserved ejection fraction: a hypothesis to explain influence of sex on the evolution and potential treatment of the disease. Eur J Heart Fail.2020;22:1551–1567 |
| ↑4 | Sorimachi H, Burkhoff D, Verbrugge FH, et al. Obesity, venous capacitance, and venous compliance in heart failure with preserved ejection fraction. Eur J Heart Fail. 2021;23:1648–1658. |
| ↑5 | Mohammed SF, Hussain S, Mirzoyev SA, Edwards WD, Maleszewski JJ, Redfield MM. Coronary microvascular rarefaction and myocardial fibrosis in heart failure with preserved ejection fraction. Circulation. 2015;131:550–559 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

