Stefano De Servi, Università degli Studi di Pavia
Inquadramento
Alcuni trial di confronto tra ecografia intravascolare (IVUS) e angiografia hanno mostrato la superiorità dell’IVUS come guida alle procedure di PCI[1]Hong S-J, Kim B-K, Shin D-H, et al. Effect of intravascular ultrasound-guided vs angiography-guided everolimus-eluting stent implantation: the IVUS-XPL randomized clinical trial. JAMA … Continua a leggere, soprattutto in quelle complesse[2]Lee JM, Choi KH, Song YB, et al. RENOVATE-COMPLEX-PCI Investigators. Intravascular Imaging-Guided or Angiography-Guided Complex PCI. N Engl J Med 2023 ;388:1668-1679. doi:10.1056/NEJMoa2216607. Tuttavia, tali studi non confrontavano l’IVUS con i dati forniti dalla angiografia coronarica quantitativa (QCA). Il recente GUIDE-DES trial, condotto in 6 centri della Corea del Sud, ha tentato di colmare questo gap conoscitivo.
Lo studio in esame
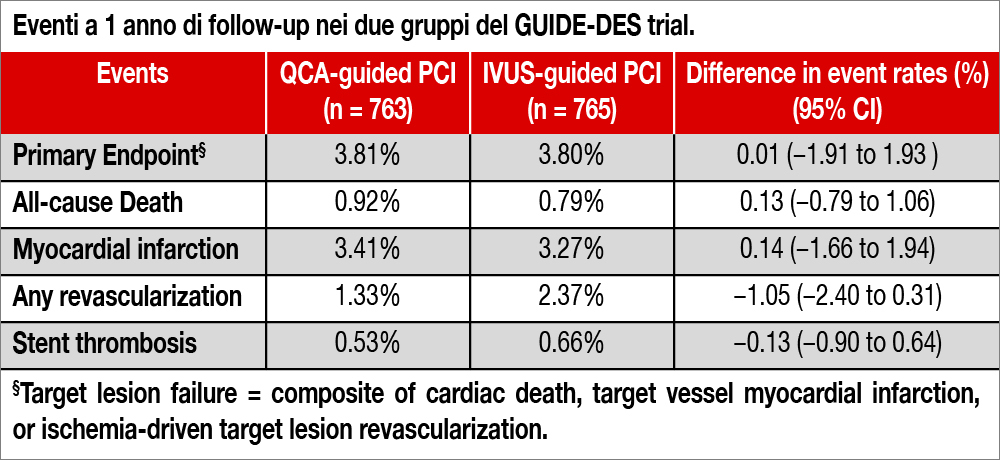
Sono stati inclusi 1.528 pazienti sottoposti a PCI (71% coronaropatia stabile, 29% sindromi coronariche acute; il 13% aveva lesioni sul tronco comune, il 46% su discendente anteriore, 13,6% erano vere biforcazioni, 5,3% occlusioni totali; trattate mediamente 1,2 lesioni per paziente con 1,6 stent con diametro medio di 3,1 mm) escludendo pazienti con lesioni su graft venoso oppure con coronarie con tortuosità tale da impedire l’uso dell’IVUS: 763 sono stati randomizzati a guida QCA (età media 64,1 anni; 75,2% maschi) e 765 a guida IVUS (età media 64,6 anni, 81% maschi). Nel gruppo QCA le misurazioni erano ottenute in “real time” utilizzando un algoritmo di “upsizing” dei diametri vasali (aggiustamento del 10% per diametri ≤3,5 mm e del 5-9% per diametri >3,5 mm onde evitare l’utilizzo di stent o palloni sottodimensionati; inoltre, era obbligatoria la post-dilatazione). Il diametro luminale minimo al termine della procedura era simile nei due gruppi (QCA 2,57 [0,55] vs IVUS 2,60 [0,58] mm, P=.26) con ottimizzazione del risultato post-IVUS ottenuta nel 66% dei casi in entrambi i gruppi. L’ipotesi alla base dello studio era la non-inferiorità di QCA versus IVUS, considerando un’incidenza di eventi dell’8% a 1 anno e un margine di non inferiorità del 3,5%. L’endpoint primario a 12 mesi (target vessel failure, un composito di morte cardiaca, infarto correlato al vaso target, rivascolarizzazione della lesione target) si è verificata in percentuali non statisticamente differenti tra i due gruppi: 3,81% nella PCI QCA-guidata e nel 3,80% delle PCI IVUS-guidata (HR 1,00 [95% CI, 0,60-1,68]; P=.99). Nessuna differenza anche per altri endpoint (vedi Tabella) quali dissezioni all’edge dello stent (1,2%vs 0,7%, P=.25) o perforazione coronarica (0,2%vs 0,4%, P=.41).
Take home message
I risultati del GUIDE-DES trial indicano che la PCI a guida QCA si associa a un numero di “target lesion failure” a 1 anno di follow-up non significativamente differente dalle PCI a guida IVUS. I dati sono da considerare con cautela in quanto gli eventi osservati sono stati molto inferiori rispetto a quelli attesi.
Interpretazione dei dati
I dati della letteratura sono stati sinora concordi nel ritenere superiore una strategia di PCI guidata da IVUS rispetto alla guida solamente angiografica[3]Hong S-J, Kim B-K, Shin D-H, et al. Effect of intravascular ultrasound-guided vs angiography-guided everolimus-eluting stent implantation: the IVUS-XPL randomized clinical trial. JAMA … Continua a leggere, soprattutto nelle procedure complesse. Il successo dell’IVUS si basa su una valutazione più oggettiva dei diametri vasali, superando i limiti dell’angiografia tradizionale, che tende a sottostimarli e quindi a utilizzare palloni e stent sotto-dimensionati. Il protocollo di QCA, seguito nel GUIDE-DES trial, limita la soggettività dei giudizi basati sulle sole immagini angiografiche prive di un valore quantitativo oggettivo; inoltre, fornisce i dati in tempo reale usando un algoritmo che tiene conto della sottovalutazione delle dimensioni dei vasi ottenuta con l’angiografia rispetto all’IVUS e rende obbligatoria la post-dilatazione. Seguendo questo rigoroso protocollo, non vi è da stupirsi se i risultati dell’angiografia migliorino notevolmente colmando il gap con l’ecografia intravascolare. Infatti, il diametro luminale minimo post-PCI è risultato simile tra le due strategie (2,57 vs 2,60 mm), così come il rapporto del diametro luminale minimo rispetto al diametro del vaso di riferimento (reference vessel diameter ratio) non è stato significativamente differente tra i due gruppi (0,81 vs 0,81). Infatti, sono questi i parametri che condizionano il numero di eventi che possono verificarsi nel follow-up[4]Blackman DJ, Porto I, Shirodaria C, Channon KM, Banning AP. Usefulness of high-pressure post-dilatation to optimize deployment of drug-eluting stents for the treatment of diffuse in-stent coronary … Continua a leggere. I risultati di questo studio contrastano con quelli degli studi IVUS-XPL e ULTIMATE[5]Hong S-J, Kim B-K, Shin D-H, et al. Effect of intravascular ultrasound-guided vs angiography-guided everolimus-eluting stent implantation: the IVUS-XPL randomized clinical trial. JAMA … Continua a leggere nei quali l’IVUS risultava superiore all’angiografia tradizionale, proprio sulla base del fatto che permetteva di ottenere un più ampio diametro luminale minimo al termine della procedura. Nonostante le indubbie limitazioni (soprattutto l’ampia differenza tra eventi attesi e osservati che pone la necessità di una riconferma di questi dati in ulteriori analisi) e l’esigenza di verificare i risultati ottenuti in subset di pazienti sottoposti a PCI complesse (stenosi distali del tronco comune e biforcazioni da trattare con due stent, occlusioni totali) è pur vero che il GUIDE-DES trial può rappresentare un cambio di paradigma in grado di modificare la strategia routinaria degli operatori nelle procedure di PCI.
Editoriale: “Lo studio GUIDE-DES non scalfisce l’utilità dell’ecografia intravascolare”
A cura di: Pietro Vandoni, Direttore SC di Cardiologia interventistica; Fondazione IRCCS San Gerardo di Monza
Nella maggior parte dei laboratori di emodinamica la decisione se ricorrere o meno alla valutazione ecografica intravascolare, durante un’angioplastica, è altamente discrezionale e legata alla formazione del singolo operatore e alla sua effettiva capacità interpretativa delle immagini. La necessità di ridurre non solo i costi ma anche i tempi di esecuzione delle procedure, l’assenza di un rimborso specifico, la mancanza di un training sistematico e la difficoltà a traslare le evidenze disponibili nella pratica clinica, e non da ultimo una certa inerzia clinica, vengono invocate come cause del sottoutilizzo della metodica[6]Barbato E, Noc M, Baumbach A, et al. Mapping interventional cardiology in Europe: the European Association of Percutaneous Cardiovascular Interventions (EAPCI) Atlas project. Eur Heart J. … Continua a leggere. Storicamente l’IVUS ha aiutato a comprendere i meccanismi della risposta della parete vascolare all’angioplastica con solo pallone ancora prima dell’introduzione sistematica degli stent[7]Potkin BN, Keren G, Mintz GS, Douek PC, Pichard AD, Satler LF, Kent KM, Leon MB. Arterial responses to balloon coronary angioplasty: an intravascular ultrasound study. J Am Coll Cardiol. … Continua a leggere e ha successivamente supportato l’evoluzione delle tecniche di impianto degli stent non medicati permettendo l’abbandono della scoagulazione dopo impianto di stent come dimostrato dal lavoro pionieristico di Antonio Colombo e coll. [8]Colombo A, Hall P, Nakamura S, Almagor Y, Maiello L, Martini G, et al. Intracoronary stenting without anticoagulation accomplished with intravascular ultrasound guidance. Circulation. 1995 Mar … Continua a leggere inaugurando di fatto l’era della DAPT; in tempi più recenti ha permesso la comprensione dei meccanismi di failure (ristenosi e trombosi intrastent) degli stent medicati[9]Cook S, Ladich E, Nakazawa G, Eshtehardi P, Neidhart M, Vogel R, Togni M, Wenaweser P, Billinger M, Seiler C, Gay S,Meier B, Pichler WJ, Juni P, Virmani R, Windecker S. Correlation of intravascular … Continua a leggere. Tuttavia, a più di trent’anni dalla sua introduzione, nonostante l’enorme impatto conoscitivo e la mole di evidenze cliniche a suo favore, l’utilizzo dell’imaging intravascolare nella pratica clinica resta inferiore alle aspettative: in Europa e negli Stati Uniti le procedure di angioplastica IVUS-guidate restano comprese tra il 10 e il 20% del totale[10]Barbato E, Noc M, Baumbach A, et al. Mapping interventional cardiology in Europe: the European Association of Percutaneous Cardiovascular Interventions (EAPCI) Atlas project. Eur Heart J. … Continua a leggere e, escludendo il Giappone con percentuali di oltre il 60%, il ricorso all’IVUS resta molto variabile non solo tra le diverse aree geografiche ma da centro a centro[11]Koskinas KC, Nakamura M, Räber L, et al. Current use of intracoronary imaging in interventional practice—results of a European Association of Percutaneous Cardiovascular Interventions (EAPCI) and … Continua a leggere. Da questo dato di fatto partono i ricercatori coreani autori del GUIDE-DES trial pubblicato su JAMA in aprile che sottolineano come la disponibilità effettiva dell’IVUS non ricalca la diffusione dei laboratori di emodinamica e che i costi e la formazione, relativi al suo utilizzo, sono tuttora un limite alla sua diffusione. Il GUIDE-DES è il primo trial che mette a confronto una strategia IVUS guidata contro una strategia QCA guidata (Quantitative Coronary Analysis) e non semplicemente “angio-guidata” (visual angiography). Condotto in 6 centri ad alto volume in Corea del sud, lo studio ha previsto che tutti gli operatori coinvolti nell’arruolamento superassero un training dedicato all’utilizzo di un protocollo standardizzato di QCA che guidasse la scelta della misura di palloni e stent sulla base dei diametri prossimale e distale del vaso nelle proiezioni angiografiche migliori e stimando la lunghezza delle lesioni con metodi angiografici comunemente utilizzati quali il riferimento ai 30 mm radiopachi del filo guida o ai marker del pallone utilizzato per la pre-dilatazione. Da notare che nel braccio QCA-guidato (763 pazienti) la post-dilatazione con palloni non complianti era mandatoria e il “sizing” del pallone non compliante deciso sulla base dei diametri di riferimento prossimale e distale misurati con la QCA disponibile di default nel sistema angiografico. Nei pazienti randomizzati a PCI con imaging ecografico (765 pazienti) era invece mandatorio rivalutare con l’IVUS lo stent impiantato per escludere la presenza di dissezioni residue ma soprattutto per eseguire, se necessario, la post-dilatazione con palloni che consentissero di raggiungere un’area minima (in-stent MLA) maggiore dell’area di riferimento del vaso sano distale alla stenosi. Al follow up di 12 mesi, 6% dei pazienti, l’incidenza eseguito in oltre il 9 dell’end-point primario (target lesion failure (TLF), definita dai 3 indicatori morte cardiaca, infarto correlato alla lesione indice e “ischemia-driven TLR”) risultava sovrapponibile nei due gruppi (29 TLF nei 734 pazienti del gruppo QCA (3,81%) e 29 TLF nei 739 pazienti del gruppo IVUS (3,8%). Anche l’incidenza degli end point secondari (morte, infarto, trombosi dello stent, stroke TLR e ulteriori rivascolarizzazioni) non risultavano differenti nei due gruppi e confermavano la bassa incidenza di eventi post-rivascolarizzazione in una popolazione di pazienti arruolati prospetticamente tra il 2017 e il 2021, in prevalenza non acuti (70% circa). La bassa incidenza di eventi al follow-up, come gli stessi autori sottolineano, riduce la robustezza del dato di non inferiorità della strategia di rivascolarizzazione basata sulla QCA rispetto a quella basata sulle immagini ecografiche. A questo proposito è interessante notare che tutte le procedure sono state eseguite con un solo tipo di stent con polimero biodegradabile e a maglie sottili eliminando in questo modo l’influenza del tipo di stent sull’efficacia della rivascolarizzazione. Tra le altre limitazioni dello studio va sottolineata la bassa complessità delle lesioni trattate (Syntax Score medio 13; PCI del Tronco Comune 12%; numero di lesioni trattate per paziente 1,2, n° di stent per paziente 1,7) in una popolazione in prevalenza costituita da sindromi coronariche croniche (STEMI circa 7% equamente rappresentati nei due gruppi) con lesioni in segmenti tortuosi (non facilmente valutabili con IVUS) o marcatamente calcifiche escluse dallo studio per protocollo. Sebbene a prima vista i risultati del GUIDE- DES appaiano in controtendenza rispetto ai più recenti trial randomizzati[12]Hong SJ, MintzGS, Ahn CM,et al; IVUS-XPL Investigators. Effect of intravascular ultrasound–guided drug-eluting stent implantation: 5-year follow-up of the IVUS-XPL randomized trial. JACC … Continua a leggere che confermano la superiorità della strategia di stenting IVUS- guidato su quella basata sulla visualizzazione angiografica, un’analisi più approfondita offre spunti utili per la pratica clinica e coerenti con le robuste evidenze scientifiche più recenti[13]Stone GW, Christiansen EH, Ali ZA, Andreasen LN, Maehara A, Ahmad Y, et al. Intravascular imaging-guided coronary drug-eluting stent implantation: an updated network meta-analysis. Lancet. 2024 Mar … Continua a leggere. È fuori discussione che una buona apposizione dello stent e un’area luminale adeguata al vaso trattato, siano garanzia del buon esito clinico della procedura. Gli studi favorevoli alla PCI IVUS guidata hanno chiaramente messo in luce che la misurazione ecografica intravascolare comportava un cambio di strategia (maggior frequenza di post-dilatazione) e un tendenziale up-sizing dello stent. Di fatto sia nell’ULTIMATE[14]Hong SJ, MintzGS, Ahn CM,et al; IVUS-XPL Investigators. Effect of intravascular ultrasound–guided drug-eluting stent implantation: 5-year follow-up of the IVUS-XPL randomized trial. JACC … Continua a leggere che nel IVUS-XPL study(8) l’MLD post-PCI era significativamente superiore nel gruppo trattato con guida IVUS. Nel GUIDE-DES il diametro minimo post-PCI (MLD), ottenuto con la strategia QCA-guidata che prevedeva la post-dilatazione mandatoria è risultato sovrapponibile a quello dei pazienti sottoposti a stenting IVUS-guidato (2.57 vs 2.6 mm), così come il rapporto tra MLD e diametro di riferimento del vaso (0,81 vs 0,81) e ciò spiega, secondo gli autori, la buona performance della QCA nell’ottenere una MLD adeguata che si traduce in una ridotta incidenza di eventi clinici al follow up. Questo concetto sarebbe stato ancora più attendibile se gli autori avessero previsto una misura IVUS anche nel braccio QCA e se fosse stato disponibile un gruppo di pazienti trattati con la guida della sola angiografia (“visual estimation”). Il GUIDE-DES mette in luce, una volta di più(9,10), i limiti della valutazione soggettiva dell’angiografia che lascia alla discrezionalità dell’operatore la scelta delle misure dello stent, ma anche dei palloni da utilizzare in ogni fase della procedura. In questo senso il GUIDE- DES è coerente con le evidenze più recenti che hanno messo in luce l’impatto clinico del corretto impianto dello stent documentato dalle tecniche di imaging intravascolare[15]Stone GW, Christiansen EH, Ali ZA, Andreasen LN, Maehara A, Ahmad Y, et al. Intravascular imaging-guided coronary drug-eluting stent implantation: an updated network meta-analysis. Lancet. 2024 Mar … Continua a leggere. Di fatto, l’adozione di un protocollo standardizzato per la valutazione del diametro del vaso e la post-dilatazione sistematica con palloni di calibro adeguato, ha permesso di minimizzare la variabilità interindividuale “costringendo” gli operatori a perseguire un tendenziale “upsizing” dei palloni e stent utilizzati, rispetto a quanto avrebbero fatto nella loro pratica abituale. In sintesi, l’utilità clinica dell’imaging intravascolare è fuori discussione e le evidenze che ne supportano l’utilizzo non solo per specifiche lesioni del tronco comune non protetto (classe IIA delle linee guida europee), ma anche per scenari clinici specifici come le Sindromi Coronariche Acute[16]Neumann FJ, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. European Heart Journal. 2019 Jan 7;40(2):87–165; Li X, Ge … Continua a leggere, sono alquanto robuste e si tradurranno nel prossimo futuro nel più elevato livello di raccomandazione scientifica (IA) per un ampio spettro di lesioni e scenari clinici[17]Den Dekker WK. Is intravascular imaging the future of percutaneous coronary intervention? Lancet 2024;403, 10439:1822-1823. Nella pratica quotidiana ogni operatore deve essere consapevole che la chiave per ridurre al minimo la TLF è un impianto ottimale dello stent che può essere ottenuto utilizzando l’imaging intravascolare, ma che va comunque perseguito anche quando IVUS (o OCT) non sia disponibile.
Bibliografia[+]
| ↑1, ↑5 | Hong S-J, Kim B-K, Shin D-H, et al. Effect of intravascular ultrasound-guided vs angiography-guided everolimus-eluting stent implantation: the IVUS-XPL randomized clinical trial. JAMA 2015;314:2155-2163; Gao X-F, Ge Z, Kong X-Q, et al. 3-Year outcomes of the ULTIMATE trial comparing intravascular ultrasound versus angiography-guided drug-eluting stent implantation. JACC Cardiovasc Interv 2021;14:247-257 |
|---|---|
| ↑2 | Lee JM, Choi KH, Song YB, et al. RENOVATE-COMPLEX-PCI Investigators. Intravascular Imaging-Guided or Angiography-Guided Complex PCI. N Engl J Med 2023 ;388:1668-1679. doi:10.1056/NEJMoa2216607 |
| ↑3 | Hong S-J, Kim B-K, Shin D-H, et al. Effect of intravascular ultrasound-guided vs angiography-guided everolimus-eluting stent implantation: the IVUS-XPL randomized clinical trial. JAMA 2015;314:2155-2163; Lee JM, Choi KH, Song YB, et al. RENOVATE-COMPLEX-PCI Investigators. Intravascular Imaging-Guided or Angiography-Guided Complex PCI. N Engl J Med 2023 ;388:1668-1679. doi:10.1056/NEJMoa2216607 |
| ↑4 | Blackman DJ, Porto I, Shirodaria C, Channon KM, Banning AP. Usefulness of high-pressure post-dilatation to optimize deployment of drug-eluting stents for the treatment of diffuse in-stent coronary restenosis. Am J Cardiol. 2004;94:922-925. doi:10.1016/j.amjcard.2004.06.029 |
| ↑6 | Barbato E, Noc M, Baumbach A, et al. Mapping interventional cardiology in Europe: the European Association of Percutaneous Cardiovascular Interventions (EAPCI) Atlas project. Eur Heart J. 2020;41(27):2579-2588 |
| ↑7 | Potkin BN, Keren G, Mintz GS, Douek PC, Pichard AD, Satler LF, Kent KM, Leon MB. Arterial responses to balloon coronary angioplasty: an intravascular ultrasound study. J Am Coll Cardiol. 1992;20:942-51 |
| ↑8 | Colombo A, Hall P, Nakamura S, Almagor Y, Maiello L, Martini G, et al. Intracoronary stenting without anticoagulation accomplished with intravascular ultrasound guidance. Circulation. 1995 Mar 15;91(6):1676–88 |
| ↑9 | Cook S, Ladich E, Nakazawa G, Eshtehardi P, Neidhart M, Vogel R, Togni M, Wenaweser P, Billinger M, Seiler C, Gay S,Meier B, Pichler WJ, Juni P, Virmani R, Windecker S. Correlation of intravascular ultrasound findings with histopathological analysis of thrombus aspirates in patients with very late drug-eluting stent thrombosis.Circulation. 2009;120:391-9 |
| ↑10 | Barbato E, Noc M, Baumbach A, et al. Mapping interventional cardiology in Europe: the European Association of Percutaneous Cardiovascular Interventions (EAPCI) Atlas project. Eur Heart J. 2020;41(27):2579-2588;Smilowitz NR, Mohananey D, Razzouk L, Weisz G, Slater JN. Impact and trends of intravascular imaging in diagnostic coronary angiography and percutaneous coronary intervention in inpatients in the United States. Catheter Cardiovasc Interv. 2018;92(6):E410-E415 |
| ↑11 | Koskinas KC, Nakamura M, Räber L, et al. Current use of intracoronary imaging in interventional practice—results of a European Association of Percutaneous Cardiovascular Interventions (EAPCI) and Japanese Association of Cardiovascular Interventions and Therapeutics (CVIT) clinical practice survey. EuroIntervention. 2018;14(4):e475-e484 |
| ↑12 | Hong SJ, MintzGS, Ahn CM,et al; IVUS-XPL Investigators. Effect of intravascular ultrasound–guided drug-eluting stent implantation: 5-year follow-up of the IVUS-XPL randomized trial. JACC Cardiovasc Interv. 2020;13(1):62-71;Gao XF, Ge Z, Kong XQ, et al. ULTIMATE Investigators. 3-Year outcomes of the ULTIMATE trial comparing intravascular ultrasound versus angiography-guided drug-eluting stent implantation. JACC Cardiovasc Interv. 2021;14(3): 247-257. |
| ↑13, ↑15 | Stone GW, Christiansen EH, Ali ZA, Andreasen LN, Maehara A, Ahmad Y, et al. Intravascular imaging-guided coronary drug-eluting stent implantation: an updated network meta-analysis. Lancet. 2024 Mar 2;403(10429):824–37. |
| ↑14 | Hong SJ, MintzGS, Ahn CM,et al; IVUS-XPL Investigators. Effect of intravascular ultrasound–guided drug-eluting stent implantation: 5-year follow-up of the IVUS-XPL randomized trial. JACC Cardiovasc Interv. 2020;13(1):62-71 |
| ↑16 | Neumann FJ, Sousa-Uva M, Ahlsson A, Alfonso F, Banning AP, Benedetto U, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. European Heart Journal. 2019 Jan 7;40(2):87–165; Li X, Ge Z, Kan J, et al. Intravascular ultrasound-guided versus angiography- guided percutaneous coronary intervention in acute coronary syndromes (IVUS-ACS): a two-stage, multicentre, randomised trial. Lancet 2024; published online April 8; Landi A, Melzi A, Valgimigli M. Intravascular Ultrasound Guidance during Primary Percutaneous Coronary Intervention: No Time for Excuses. Cardiology 2024;149:193–195 |
| ↑17 | Den Dekker WK. Is intravascular imaging the future of percutaneous coronary intervention? Lancet 2024;403, 10439:1822-1823 |
Accedi per leggere tutto l'articolo
Inserisci i dati del tuo account su Cardiotalk per accedere e leggere tutto il contenuto dell'articolo.
Se non hai un account, clicca sul pulsante registrati e verrai reindirizzato al portale Cardiotalk per la registrazione.

